19. 某化学兴趣小组利用铜跟浓硫酸反应,探究SO
2的部分性质,实验装置如图所示。
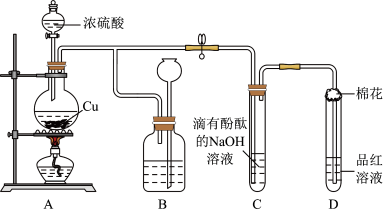
(1)装置A中发生的化学反应的化学方程式为
________________________________(2)装置B的作用是贮存多余的气体,B中广口瓶内应盛放的液体是
________(填序号);
①水
②饱和的NaHSO
3溶液
③NaOH溶液
④酸性KMnO
4(3)装置C和D中产生的现象相同,但原因却不同。C中是由于SO
2与溶液中的NaOH反应使碱性减弱,而D中则是由于SO
2具有
____________性
(4)装置D中试管口塞一团棉花,棉花中应浸有一种液体,其作用是
____________(5)若实验中用一定质量的铜片和25.0 mL 18.0 mol·L
-1的浓硫酸在加热条件充分反应,最终铜片与硫酸均有剩余。假定反应前后溶液的体积不变,设剩余硫酸的浓度为d mol·L
-1,现向反应后溶液中缓慢加入硝酸钾固体,充分搅拌直到剩余铜片恰好完全反应,反应消耗硝酸钾
____________mol(用含d的代数式表示)。