实验室向 0.783g MnO2 中加入 20mL36.5%(ρ=1.18g/cm3 )浓盐酸后,共热制取 Cl2.反应方程式为:MnO2+4HClMnCl2+Cl2+2H2O,若反应后溶液体积仍为 20mL,则下列说法正确的是( )
| A.反应消耗 HCl 物质的量为 0.236mol |
| B.反应生成 Cl2 气体的体积为 201.6mL |
| C.若取 2mL 反应后的溶液,加入足量 AgNO3,可产生沉淀 2.87g |
| D.若取 2mL 反应后的溶液,加入 2.0mol/L 的 NaOH,当沉淀达到最大值时,消耗 NaOH 溶液的体积为10.9mL |
更新时间:2019-08-17 23:52:07
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】为测定含镁3% ~5%的铝镁合金中镁的质量分数,设计了2种实验方案:
方案一:镁铝合金加入足量的氢氧化钠溶液中充分反应后过滤,测定剩余固体质量;
方案二:称量mg铝镁合金粉末,放在图中惰性电热板上,通电使其充分灼烧。测得固体质量增重。

下列说法错误的是
方案一:镁铝合金加入足量的氢氧化钠溶液中充分反应后过滤,测定剩余固体质量;
方案二:称量mg铝镁合金粉末,放在图中惰性电热板上,通电使其充分灼烧。测得固体质量增重。

下列说法错误的是
| A.方案一中若称取5.4g合金粉末样品,投入V mL 2.0 mol· L-1 NaOH溶液中反应,则V≥95 |
| B.方案一中测定剩余固体质量时,过滤后未洗涤固体就干燥、称量,则镁的质量分数偏低 |
| C.方案二中欲计算镁的质量分数,实验中还需测定灼烧后固体的质量 |
| D.方案二中若用空气代替O2进行实验,则测定结果偏高 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列叙述中错误的是
| A.Na投入水中会熔成小球,并四处游动,说明Na与水反应放热并生成气体 |
| B.Na和O2在加热时反应生成Na2O2,在常温下反应生成Na2O |
| C.Na2O与CO2发生化合反应生成Na2CO3,Na2O2与CO2发生置换反应生成O2 |
| D.44gCO2被Na2O2完全吸收,固体增重28g |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】 、HCl的混合气体通入足量的NaOH溶液,充分反应后,溶液中除大量
、HCl的混合气体通入足量的NaOH溶液,充分反应后,溶液中除大量 外,还有
外,还有 、
、 、
、 ,且这三种离子的个数比为9∶2∶1,则原混合气体中
,且这三种离子的个数比为9∶2∶1,则原混合气体中 和HCl的个数之比为
和HCl的个数之比为
 、HCl的混合气体通入足量的NaOH溶液,充分反应后,溶液中除大量
、HCl的混合气体通入足量的NaOH溶液,充分反应后,溶液中除大量 外,还有
外,还有 、
、 、
、 ,且这三种离子的个数比为9∶2∶1,则原混合气体中
,且这三种离子的个数比为9∶2∶1,则原混合气体中 和HCl的个数之比为
和HCl的个数之比为| A.5∶2 | B.2∶5 | C.3∶1 | D.1∶3 |
您最近一年使用:0次
单选题
|
适中
(0.65)
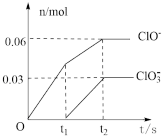
【推荐2】将 通入一定浓度的氢氧化钾溶液中,两者恰好完全反应(已知反应过程放热),生成物中有三种含氯元素的离子,其中
通入一定浓度的氢氧化钾溶液中,两者恰好完全反应(已知反应过程放热),生成物中有三种含氯元素的离子,其中 和
和 两种离子的物质的量(n)与反应时间(t)的变化情况如下图所示。下列说法错误的是
两种离子的物质的量(n)与反应时间(t)的变化情况如下图所示。下列说法错误的是
 通入一定浓度的氢氧化钾溶液中,两者恰好完全反应(已知反应过程放热),生成物中有三种含氯元素的离子,其中
通入一定浓度的氢氧化钾溶液中,两者恰好完全反应(已知反应过程放热),生成物中有三种含氯元素的离子,其中 和
和 两种离子的物质的量(n)与反应时间(t)的变化情况如下图所示。下列说法错误的是
两种离子的物质的量(n)与反应时间(t)的变化情况如下图所示。下列说法错误的是
A. 时生成物中 时生成物中 的物质的量为0.09mol 的物质的量为0.09mol |
| B.反应后转移电子的物质的量为0.21mol |
| C.原氢氧化钾溶液中KOH的物质的量为0.3mol |
D. 和氢氧化钾溶液在不同温度下可能发生不同反应 和氢氧化钾溶液在不同温度下可能发生不同反应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列装置所示的实验中,能达到实验目的的是
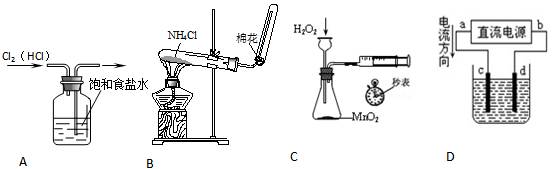

| A.除去Cl2中的HCl杂质 |
| B.实验室制取NH3 |
| C.定量测定H2O2分解化学反应速率 |
| D.c为粗铜,d为纯铜,溶液为硫酸铜溶液,电解精炼铜 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】某同学用下列装置进行有关 性质的实验。下列说法不正确的是
性质的实验。下列说法不正确的是

 性质的实验。下列说法不正确的是
性质的实验。下列说法不正确的是
| A.图1中:实验室制备氯气 |
| B.图2中:产生苍白色火焰 |
| C.图3中:向实验后冷却的固体中加少量水溶解得到蓝色溶液 |
| D.图4中:产生的大量白烟是氯化钠晶体 |
您最近一年使用:0次

 )中的氧原子数均为0.1NA
)中的氧原子数均为0.1NA 是一种广谱型的消毒剂,根据世界环保联盟的要求
是一种广谱型的消毒剂,根据世界环保联盟的要求 和
和 溶液混合并加
溶液混合并加 酸化后反应制得,在以上反应中还原剂和氧化剂的物质的量之比为
酸化后反应制得,在以上反应中还原剂和氧化剂的物质的量之比为 2H++Cl-+ClO-
2H++Cl-+ClO- Mn2++2H2O+2Cl2↑
Mn2++2H2O+2Cl2↑

