氯化钾样品中含有少量碳酸钾、硫酸钾和不溶于水的杂质。为了提纯氯化钾,先将样品溶于适量水中,充分搅拌后过滤,再将滤液按如下图所示步骤进行操作(注意事项:①所加试剂必须过量;②过量试剂必须除去;③不能引入新的杂质)。
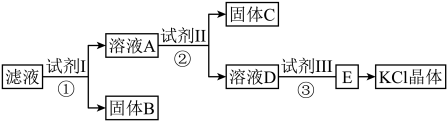
回答下列问题:
(1)试剂Ⅰ的化学式为______ ,①中发生反应的离子方程式为_________ 。
(2)试剂Ⅱ的化学式为_______ ,②中加入试剂Ⅱ的目的是____________ 。
(3)试剂Ⅲ的名称是________ ,③中发生反应的离子方程式为__________ 。

回答下列问题:
(1)试剂Ⅰ的化学式为
(2)试剂Ⅱ的化学式为
(3)试剂Ⅲ的名称是
更新时间:2019-09-07 22:15:51
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】海水是巨大的资源宝库,从海水中提取食盐和溴的过程如下:

(1)除去粗盐中杂质(Mg2+、 、Ca2+),加入的药品顺序正确的是
、Ca2+),加入的药品顺序正确的是__________ 。
A.NaOH溶液→Na2CO3溶液→BaCl2溶液→过滤后加盐酸
B.BaCl2溶液→NaOH溶液→Na2CO3溶液→过滤后加盐酸
C.NaOH溶液→BaCl2溶液→Na2CO3溶液→过滤后加盐酸
D.Na2CO3溶液→NaOH溶液→BaCl2溶液→过滤后加盐酸
(2)步骤I中已获得Br2,步骤II中又将Br2还原为Br-,其目的是富集。发生反应的化学方程式:______________________ 。
(3)某化学小组的同学为了了解从工业溴中提纯溴的方法,查阅了有关资料,Br2的沸点为59℃。微溶于水,有毒性和强腐蚀性。他们参观生产过程后,设计了如下实验装置:

①图中仪器B的名称是______ ,冷却水的出口为_______ (填“甲”或“乙”)。
②D装置的作用是________________ 。
(4)已知某溶液中Cl-、Br-、I-的物质的量之比为2:3:4,现欲使溶液中的Cl一、Br一、I一的物质的量之比变成4:3:2,那么要通入C12的物质的量是原溶液中I一的物质的量的____________ (填选项)。
A. B.
B.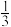 C.
C.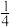 D.
D.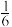

(1)除去粗盐中杂质(Mg2+、
 、Ca2+),加入的药品顺序正确的是
、Ca2+),加入的药品顺序正确的是A.NaOH溶液→Na2CO3溶液→BaCl2溶液→过滤后加盐酸
B.BaCl2溶液→NaOH溶液→Na2CO3溶液→过滤后加盐酸
C.NaOH溶液→BaCl2溶液→Na2CO3溶液→过滤后加盐酸
D.Na2CO3溶液→NaOH溶液→BaCl2溶液→过滤后加盐酸
(2)步骤I中已获得Br2,步骤II中又将Br2还原为Br-,其目的是富集。发生反应的化学方程式:
(3)某化学小组的同学为了了解从工业溴中提纯溴的方法,查阅了有关资料,Br2的沸点为59℃。微溶于水,有毒性和强腐蚀性。他们参观生产过程后,设计了如下实验装置:

①图中仪器B的名称是
②D装置的作用是
(4)已知某溶液中Cl-、Br-、I-的物质的量之比为2:3:4,现欲使溶液中的Cl一、Br一、I一的物质的量之比变成4:3:2,那么要通入C12的物质的量是原溶液中I一的物质的量的
A.
 B.
B.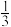 C.
C.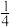 D.
D.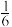
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】完成下列问题。
(1)向CuCl2溶液中滴加NaOH溶液,离子方程式:___________ 。
(2)向Ba(OH)2溶液中加入稀硫酸,离子方程式:___________ 。
(3)某无色透明溶液可能存在大量Ag+、Mg2+、Fe3+、Cu2+、Cl-、NO 、CO
、CO 、K+中的一种或几种,请填写下列空白:
、K+中的一种或几种,请填写下列空白:
①取少量原溶液,加入过量稀盐酸,有白色沉淀生成,再加入过量稀硝酸,沉淀不消失,说明原溶液中肯定存在的离子是___________ 。
②取①的滤液加过量的NaOH溶液,出现白色沉淀,说明原溶液中肯定有___________ ,有关反应的离子方程式为___________ 。
③通过以上叙述可知溶液中肯定不存在的离子是___________ ,可能存在的离子是___________ 。
(1)向CuCl2溶液中滴加NaOH溶液,离子方程式:
(2)向Ba(OH)2溶液中加入稀硫酸,离子方程式:
(3)某无色透明溶液可能存在大量Ag+、Mg2+、Fe3+、Cu2+、Cl-、NO
 、CO
、CO 、K+中的一种或几种,请填写下列空白:
、K+中的一种或几种,请填写下列空白:①取少量原溶液,加入过量稀盐酸,有白色沉淀生成,再加入过量稀硝酸,沉淀不消失,说明原溶液中肯定存在的离子是
②取①的滤液加过量的NaOH溶液,出现白色沉淀,说明原溶液中肯定有
③通过以上叙述可知溶液中肯定不存在的离子是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】海洋资源的利用具有广阔前景。
I.海洋植物如海带、海藻中含有丰富的碘元素,碘元素以碘离子的形式存在。实验室从海带中提取碘的流程如下:

(1)步骤①灼烧海带时,盛放海带的仪器名称是_______ 。
(2)步骤④中反应的离子方程式为_______ 。
(3)步骤⑤的操作为:向含I2的水溶液加入有机试剂,用力震荡后静置分层后分液,则可以选择的有机试剂是_______(填标号)。
II.为除去粗盐中含有的可溶性杂质硫酸钠、氯化钙和氯化镁,某同学利用给定试剂NaOH溶液、BaCl2溶液、 溶液和盐酸,设计了如图实验流程:
溶液和盐酸,设计了如图实验流程:
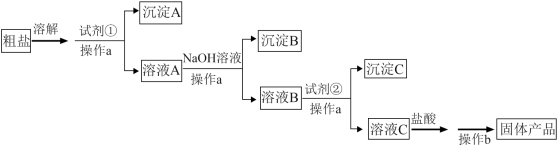
(4)操作a和操作b的名称依次是_______ 、_______ 试剂①是_______ 。
(5)加入试剂②后,发生反应的离子方程式是_______ 。
(6)加入盐酸的作用是_______ 。你设计的流程和该同学的一样吗?简述不同之处_______ (若一样则此空不填)。
I.海洋植物如海带、海藻中含有丰富的碘元素,碘元素以碘离子的形式存在。实验室从海带中提取碘的流程如下:

(1)步骤①灼烧海带时,盛放海带的仪器名称是
(2)步骤④中反应的离子方程式为
(3)步骤⑤的操作为:向含I2的水溶液加入有机试剂,用力震荡后静置分层后分液,则可以选择的有机试剂是_______(填标号)。
| A.四氯化碳 | B.酒精 | C.苯 | D.醋酸 |
II.为除去粗盐中含有的可溶性杂质硫酸钠、氯化钙和氯化镁,某同学利用给定试剂NaOH溶液、BaCl2溶液、
 溶液和盐酸,设计了如图实验流程:
溶液和盐酸,设计了如图实验流程:
(4)操作a和操作b的名称依次是
(5)加入试剂②后,发生反应的离子方程式是
(6)加入盐酸的作用是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】除去括号中杂质,写出所加试剂与反应的离子方程式。
(1) (
( ),所加试剂:
),所加试剂:_________ ,离子方程式:___________________________ 。
(2)Cl-( ),所加试剂:
),所加试剂:_________ ,离子方程式:___________________________ 。
(3)Fe2+(Cu2+),所加试剂:_________ ,离子方程式:___________________________ 。
(4) (Cl-),所加试剂:
(Cl-),所加试剂:_________ ,离子方程式:___________________________ 。
(1)
 (
( ),所加试剂:
),所加试剂:(2)Cl-(
 ),所加试剂:
),所加试剂:(3)Fe2+(Cu2+),所加试剂:
(4)
 (Cl-),所加试剂:
(Cl-),所加试剂:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】用海水“晒盐”的方法得到的粗盐中,除氯化钠外,还含有氯化镁、氯化钙、硫酸钠等杂质。将此粗盐提纯的部分实验方案如图:

(1)加入BaCl2溶液的目的(用离子方程式表示)_______ 。
(2)能否将Na2CO3和BaCl2的顺序对调,请说明原因:_______ 。
(3)生成沉淀a的离子方程式:_______ 。
(4)沉淀b的主要成分的化学式是:_______ 。
(5)用文字描述加入适量稀盐酸的目的:_______ 。

(1)加入BaCl2溶液的目的(用离子方程式表示)
(2)能否将Na2CO3和BaCl2的顺序对调,请说明原因:
(3)生成沉淀a的离子方程式:
(4)沉淀b的主要成分的化学式是:
(5)用文字描述加入适量稀盐酸的目的:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】粗盐中含有难溶性杂质(泥沙等)和多种可溶性杂质(氯化镁、氯化钙等)。某班同学在粗盐提纯实验中,为把少量可溶性杂质 、
、 一并除去,设计了如下方案:
一并除去,设计了如下方案:
(1)为了加快粗盐的溶解,可采取的措施有_______ (填一种即可)。
(2)写出步骤ⅳ中发生反应的化学方程式:_______ 。
(3)沉淀B的主要成分为_______ (填化学式);往沉淀B中加入足量稀盐酸,观察到的现象为_______ 。
(4)在步骤ⅵ中,___ (填“能”或“不能”)用稀硝酸代替稀盐酸进行该实验,理由为____ 。
(5)步骤ⅶ中操作b指的是_______ 。
(6)该方案实际得到的氯化钠比粗盐中含有的氯化钠要多,理由为_______ 。
 、
、 一并除去,设计了如下方案:
一并除去,设计了如下方案: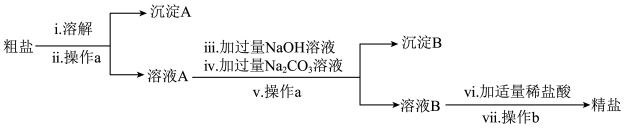
(1)为了加快粗盐的溶解,可采取的措施有
(2)写出步骤ⅳ中发生反应的化学方程式:
(3)沉淀B的主要成分为
(4)在步骤ⅵ中,
(5)步骤ⅶ中操作b指的是
(6)该方案实际得到的氯化钠比粗盐中含有的氯化钠要多,理由为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】工业上的许多反应工艺来源于实验室里的简单操作,比如用铝土矿(成分为氧化铝、氧化铁)制取铝的过程如图:

请回答下列问题:
(1)写出铝土矿中加入NaOH溶液的反应方程式___ 。
(2)沉淀C的化学式___ ,颜色为___ ,写出它的一种用途___ 。
(3)操作I、操作II、操作III的名称为___ ,这个过程用到的玻璃仪器有烧杯、___ 。
(4)整个生产过程中,除可以循环使用的物质有___ (写出3种,填化学式),用此法制取铝的副产品是___ (写出2种,填化学式)。
(5)氧化铝熔点高,氯化铝熔点低,工业上为什么不用熔点较低的氯化铝而用熔点更高的氧化铝为原料电解制铝?___ 。

请回答下列问题:
(1)写出铝土矿中加入NaOH溶液的反应方程式
(2)沉淀C的化学式
(3)操作I、操作II、操作III的名称为
(4)整个生产过程中,除可以循环使用的物质有
(5)氧化铝熔点高,氯化铝熔点低,工业上为什么不用熔点较低的氯化铝而用熔点更高的氧化铝为原料电解制铝?
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】某工厂排放的工业废水中含Fe3+、Al3+、Cu2+,工厂为了防止环境污染,变废为宝,利用废铁屑和其他化学试剂进行如下操作,得到了绿矾(FeSO4·7H2O)、Al2O3和金属Cu,回答下列问题:

(1)固体C是_________ (用化学式表示)。
(2)在过程①中需要通入足量的氯气,该过程中发生反应的离子方程式为__________ 。
(3)溶液E焰色反应呈黄色,溶液a是______________ 。
(4)沉淀F→溶液H中所用试剂:②_________ ,③____________ 。溶液G→溶液H反应的离子方程式是_______________________ 。
(5)实验室中由溶液H得到绿矾的操作是:蒸发、浓缩___________ 、过滤。

(1)固体C是
(2)在过程①中需要通入足量的氯气,该过程中发生反应的离子方程式为
(3)溶液E焰色反应呈黄色,溶液a是
(4)沉淀F→溶液H中所用试剂:②
(5)实验室中由溶液H得到绿矾的操作是:蒸发、浓缩
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】硼氢化钠(NaBH4)在化工等领域具有重要的应用价值,某研究小组采用偏硼酸钠(NaBO2)为主要原料制备NaBH4,其流程如下。已知:NaBH4常温下能与水反应,可溶于异丙酸(沸点:13℃)。

(1)硼氢化钠(NaBH4)的电子式为 ;其中B元素的化合价为
(2)在第①步反应加料之前,需要将反应器加热至100℃以上并通入氩气,该操作的目的是:________________。
(3)请配平第①步反应的化学方程式: NaBO2+ SiO2+ Na+ H2----- NaBH4+ Na2SiO3
(4)第②步操作需要的玻璃仪器有: ;第③步分离(NaBH4)并回收溶剂,采用的方法是____。

(1)硼氢化钠(NaBH4)的电子式为 ;其中B元素的化合价为
(2)在第①步反应加料之前,需要将反应器加热至100℃以上并通入氩气,该操作的目的是:________________。
(3)请配平第①步反应的化学方程式: NaBO2+ SiO2+ Na+ H2----- NaBH4+ Na2SiO3
(4)第②步操作需要的玻璃仪器有: ;第③步分离(NaBH4)并回收溶剂,采用的方法是____。
您最近一年使用:0次



