下图所示甲、乙是电化学实验装置。
(1)若甲、乙两烧杯中均盛有NaCl溶液。
①甲中石墨棒上的电极反应式为__________________________________ 。
②乙中总反应的离子方程式为____________________________________ 。
③将湿润的淀粉KI试纸放在乙烧杯上方,发现试纸先变蓝后褪色,这是因为过量的Cl2氧化了生成的I2。若反应中Cl2和I2的物质的量之比为5∶1,且生成两种酸,该反应的化学方程式为_________ 。
(2)若甲、乙两烧杯中均盛有CuSO4溶液。
①甲中铁棒上的电极反应式为__________________________ 。
②如果起始时乙中盛有200 mL pH=5的CuSO4溶液(25 ℃),一段时间后溶液的pH变为1,若要使溶液恢复到电解前的状态,可向溶液中加入________ (填写物质的化学式)________ g。
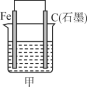
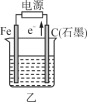
(1)若甲、乙两烧杯中均盛有NaCl溶液。
①甲中石墨棒上的电极反应式为
②乙中总反应的离子方程式为
③将湿润的淀粉KI试纸放在乙烧杯上方,发现试纸先变蓝后褪色,这是因为过量的Cl2氧化了生成的I2。若反应中Cl2和I2的物质的量之比为5∶1,且生成两种酸,该反应的化学方程式为
(2)若甲、乙两烧杯中均盛有CuSO4溶液。
①甲中铁棒上的电极反应式为
②如果起始时乙中盛有200 mL pH=5的CuSO4溶液(25 ℃),一段时间后溶液的pH变为1,若要使溶液恢复到电解前的状态,可向溶液中加入
11-12高三上·河南三门峡·期中 查看更多[14]
江西省南昌市进贤一中2019-2020学年高二上学期期末考试化学试题江西省南城县第二中学2018-2019学年高二上学期第二次月考化学试题(已下线)考点10 电解原理 金属的腐蚀与防护——备战2019年浙江新高考化学考点江西省玉山县第一中学2017届高三化学板块复习测试:基本理论(已下线)2012届山东省潍坊市寿光现代中学高三12月月考化学试卷(已下线)2012届河南省三门峡市高三上学期调研考试化学试卷2017届福建省厦门大学附中高三上学期第二次月考化学试卷2014-2015湖南省娄底市高二上学期期末考试化学(理)试卷(已下线)2013-2014河南省封丘一中高二上学期期末考试化学试卷(已下线)2014年高考化学苏教版总复习 6-3 原电池金属的腐蚀及防护练习卷(已下线)2014年化学高考总复习单元检测 第九章电化学基础练习卷(已下线)2012-2013学年吉林省吉林一中高一4月月考化学试卷(已下线)2011-2012年湖北宜昌金东方学校高二上学期期末考试化学试卷(已下线)2011-2012学年河南省平顶山市高二上学期期末考试化学试卷
更新时间:2011-12-12 16:28:48
|
相似题推荐
填空题
|
适中
(0.65)
名校
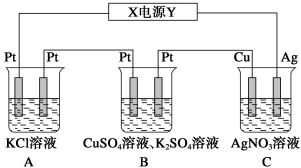
【推荐1】在如图所示的装置中,若通直流电5min时,铜电极质量增加2.16g。请回答下列问题:
(1)电源中Y电极为直流电源的__________ 极。
(2)pH变化:A:________ B:________ C:_________ (填“增大”、“减小”或“不变”)。
(3) 若A中KCl溶液的体积是200 mL,电解后,溶液的pH为__________ (设电解前后溶液体积无变化)。
(1)电源中Y电极为直流电源的
(2)pH变化:A:
(3) 若A中KCl溶液的体积是200 mL,电解后,溶液的pH为
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】某同学设计了一种甲醇燃料电池并探究氯碱工业原理和粗铜的精炼原理,如下图所示,其中乙装置中间 为阳离子交换膜。
为阳离子交换膜。
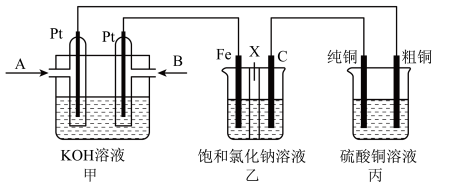
(1)电极 是极
是极_____ (“正”或“负”),电池工作时电极 的电极反应式为
的电极反应式为____________________ 。
(2)已知电解前乙装置溶液的浓度为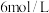 ,总体积为
,总体积为 .当甲装置消耗标准状况下
.当甲装置消耗标准状况下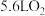 时,乙池中阴极区溶液中
时,乙池中阴极区溶液中 的浓度为
的浓度为__________  ,丙装置中纯铜电极增重
,丙装置中纯铜电极增重__________ g。(电解前后溶液体积变化忽略不计)。
(3)如果丙装置中粗铜中含有锌、银等杂质,丙装置中反应一段时间, 溶液的浓度将
溶液的浓度将________ (填“增大”、“减小”或“不变”).
(4)若将甲装置改为铅蓄电池,当乙装置共产生标况下 气体时,铅蓄电池的负极增重
气体时,铅蓄电池的负极增重_______ g。
 为阳离子交换膜。
为阳离子交换膜。
(1)电极
 是极
是极 的电极反应式为
的电极反应式为(2)已知电解前乙装置溶液的浓度为
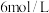 ,总体积为
,总体积为 .当甲装置消耗标准状况下
.当甲装置消耗标准状况下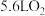 时,乙池中阴极区溶液中
时,乙池中阴极区溶液中 的浓度为
的浓度为 ,丙装置中纯铜电极增重
,丙装置中纯铜电极增重(3)如果丙装置中粗铜中含有锌、银等杂质,丙装置中反应一段时间,
 溶液的浓度将
溶液的浓度将(4)若将甲装置改为铅蓄电池,当乙装置共产生标况下
 气体时,铅蓄电池的负极增重
气体时,铅蓄电池的负极增重
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐3】如图所示,U形管内盛有100mL的溶液,按要求回答下列问题:

(1)打开K2,合并K1,若所盛溶液为CuSO4溶液:则A为___________ 极,A极的电极反应式为___________ 。若所盛溶液为KCl溶液:则B极的电极反应式为___________ 。
(2)打开K1,合并K2,若所盛溶液为滴有酚酞的NaCl溶液,则A电极附近可观察到的现象是___________ ,Na+移向___________ 极(填A、B);B电极上的电极反应式为___________ ,总反应化学方程式是___________ 。
(3)如果要用电解的方法精炼粗铜,打开K1,合并K2,电解液选用CuSO4溶液,则A电极的材料应换成是___________ (填“粗铜”或“纯铜”),电极反应式是___________ ,反应一段时间后电解质溶液中Cu2+的浓度将会___________ (填“增大”、“减小”、“不变”)。

(1)打开K2,合并K1,若所盛溶液为CuSO4溶液:则A为
(2)打开K1,合并K2,若所盛溶液为滴有酚酞的NaCl溶液,则A电极附近可观察到的现象是
(3)如果要用电解的方法精炼粗铜,打开K1,合并K2,电解液选用CuSO4溶液,则A电极的材料应换成是
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】某兴趣小组的同学用如图所示装置研究有关电化学的问题(甲、乙、丙三池中溶质足量),当闭合该装置的电键K时,观察到电流计的指针发生了偏转。请回答下列问题:

(1)丙池中E电极为_______ (填“正极”、“负极”、“阴极”或“阳极”)
(2)当乙池中C极质量减轻5.4g时,甲池中B电极理论上消耗O2的体积为_______ mL(标况)。
(3)一段时间后,断开电键K,下列物质能使丙池恢复到反应前浓度的是_______ 。
(4)爱迪生蓄电池的反应式为:Fe+NiO2+2H2O=Fe(OH)2+Ni(OH)2;高铁酸钠(Na2FeO4)易溶于水,是一种新型净水剂。用如图装置可以制取少量高铁酸钠。
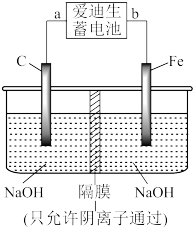
①此装置中爱迪生蓄电池的正极是_______ (填“a”或“b”)
②写出在用电解法制取高铁酸钠时,阳极的电极反应式为_______ 。

(1)丙池中E电极为
(2)当乙池中C极质量减轻5.4g时,甲池中B电极理论上消耗O2的体积为
(3)一段时间后,断开电键K,下列物质能使丙池恢复到反应前浓度的是_______ 。
| A.Cu | B.CuO | C.Cu(OH)2 | D.Cu2(OH)2CO3 |

①此装置中爱迪生蓄电池的正极是
②写出在用电解法制取高铁酸钠时,阳极的电极反应式为
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】如图是一个甲烷燃料电池工作时的示意图,乙池中的两个电极一个是石墨电极,一个是铁电极,工作时N电极的质量减少,请回答下列问题:
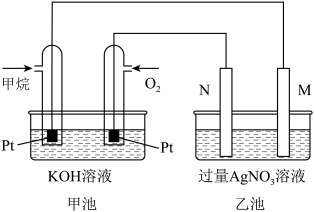
(1)M电极的材料是________ ,其电极反应式为:________ N的电极名称是________ ,电极反应式为:________
(2)通入甲烷的铂电极的电极反应式为________ .
(3)在此过程中,乙池中某一电极析出金属银4.32g时,甲池中理论上消耗氧气为________ L(标准状况下)。

(1)M电极的材料是
(2)通入甲烷的铂电极的电极反应式为
(3)在此过程中,乙池中某一电极析出金属银4.32g时,甲池中理论上消耗氧气为
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐3】试运用电化学知识解决下列问题:
(1)利用自发进行的氧化还原反应: 设计一个原电池,可供选择的材料有:小灯泡、导线、铜棒、锌棒、石墨棒、硫酸铜溶液、硫酸锌溶液。请画出实验装置示意图:
设计一个原电池,可供选择的材料有:小灯泡、导线、铜棒、锌棒、石墨棒、硫酸铜溶液、硫酸锌溶液。请画出实验装置示意图:___________ ,正极反应式为___________ 。
(2)某原电池的工作原理为 ,该电池的两电极分别为铜棒、银棒,若开始时两电极质量相等,当电路中转移
,该电池的两电极分别为铜棒、银棒,若开始时两电极质量相等,当电路中转移 电子时,理论上两电极的质量差为
电子时,理论上两电极的质量差为___________ g。
(3)某研究团队合成的低配位 在碱性条件下催化
在碱性条件下催化 还原生成乙烯的电化学装置如图所示。
还原生成乙烯的电化学装置如图所示。
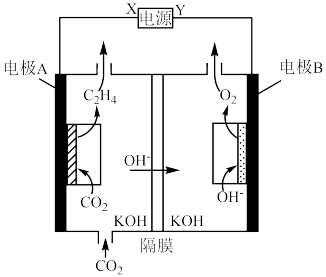
①Y为电源的___________ (填“正极”或“负极”)。
②电极A上的电极反应式为___________ 。
③理论上电极A上消耗的 与电极B上生成的
与电极B上生成的 的物质的量之比为
的物质的量之比为___________ 。
(4)下图为典型的电化学实验装置:

①甲池中C电极为___________ (填“阴极”或“阳极”),甲池的总反应式为___________ 。
②当甲池中 极质量增加
极质量增加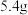 时,理论上乙池中
时,理论上乙池中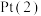 极的质量变化值为
极的质量变化值为___________ g。
(1)利用自发进行的氧化还原反应:
 设计一个原电池,可供选择的材料有:小灯泡、导线、铜棒、锌棒、石墨棒、硫酸铜溶液、硫酸锌溶液。请画出实验装置示意图:
设计一个原电池,可供选择的材料有:小灯泡、导线、铜棒、锌棒、石墨棒、硫酸铜溶液、硫酸锌溶液。请画出实验装置示意图:(2)某原电池的工作原理为
 ,该电池的两电极分别为铜棒、银棒,若开始时两电极质量相等,当电路中转移
,该电池的两电极分别为铜棒、银棒,若开始时两电极质量相等,当电路中转移 电子时,理论上两电极的质量差为
电子时,理论上两电极的质量差为(3)某研究团队合成的低配位
 在碱性条件下催化
在碱性条件下催化 还原生成乙烯的电化学装置如图所示。
还原生成乙烯的电化学装置如图所示。
①Y为电源的
②电极A上的电极反应式为
③理论上电极A上消耗的
 与电极B上生成的
与电极B上生成的 的物质的量之比为
的物质的量之比为(4)下图为典型的电化学实验装置:

①甲池中C电极为
②当甲池中
 极质量增加
极质量增加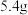 时,理论上乙池中
时,理论上乙池中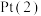 极的质量变化值为
极的质量变化值为
您最近半年使用:0次



