A与B有如下的反应:A+B→C+D。
(1)若C为厨房内常用的调味品;在A溶液中加入铁粉能产生氢气,则A是________ 。若A、B两溶液恰好反应完全,则反应后溶液的pH___ 7(填“<”、“>”或“=”);写出A、B两溶液反应的化学方程式________________ 。
(2)若A的固体俗称火碱,C是蓝色沉淀。则A为___ ,C为___ 。写出A物质的溶液与CO2反应的化学方程式________ 。
(1)若C为厨房内常用的调味品;在A溶液中加入铁粉能产生氢气,则A是
(2)若A的固体俗称火碱,C是蓝色沉淀。则A为
更新时间:2019-09-21 10:22:21
|
相似题推荐
填空题
|
较易
(0.85)
名校
【推荐1】现有中学化学常见的物质A、B、C、D、E、F、G、H,满足如下图所示转化关系。其中A、F为气体单质,A呈黄绿色,C为淡黄色固体化合物。B为生活中常见的液体化合物。回答下列问题:
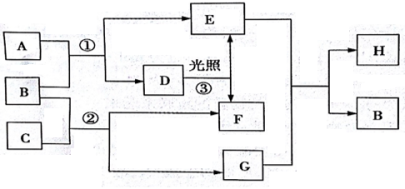
(1)写出下列物质的化学式:C________ ,H______________ 。
(2)出下列化学反应方程式:
①______________________________________ 。
③______________________________________ 。
(3)写出D的一种用途__________________________ 。但由于D易于发生③反应而不易于保存,故生产生活中往往用A与石灰乳反应生成易于保存运输的固体,其在潮湿空气中可以反应生成D,请写出这两个反应方程式_________________ ,_______________ 。

(1)写出下列物质的化学式:C
(2)出下列化学反应方程式:
①
③
(3)写出D的一种用途
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】元素周期律和周期表是我们研究、预测物质性质的重要工具。下表是元素周期表中前四周期的5种元素的相关信息。
回答下列问题:
(1)D在元素周期表中的位置是___________ 。
(2)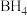 的电子式为
的电子式为___________ 。
(3)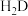 分子中含有
分子中含有___________ (填“极性共价键”或“非极性共价键”)。
(4)少量E的单质加入水中剧烈反应,反应的化学方程式是___________ ;将一块C单质加入上述形成的强碱溶液中反应的离子方程式是___________ ;元素A、E的最高价氧化物对应的水化物中,碱性更强的物质是___________ (填写化学式)。
(5)D的简单离子与的E简单离子半径较大的是___________ (填离子符号)。
(6)任意写出一个化学反应方程式证明氧元素的非金属性强于D元素___________ 。
| 元素 | 元素性质或原子结构 |
| A | 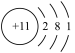 |
| B | B能形成多种单质,其中一种单质是硬度最大的物质 |
| C | 地壳中含量最高的金属元素,其合金可用于制造飞机外壳 |
| D | D的单质是一种黄色晶体 |
| E | 用E的碳酸盐做焰色试验时火焰为紫色(透过蓝色钴玻璃片) |
(1)D在元素周期表中的位置是
(2)
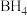 的电子式为
的电子式为(3)
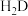 分子中含有
分子中含有(4)少量E的单质加入水中剧烈反应,反应的化学方程式是
(5)D的简单离子与的E简单离子半径较大的是
(6)任意写出一个化学反应方程式证明氧元素的非金属性强于D元素
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】A、B、C为中学常见单质,其中一种为金属;通常情况下A为固体、B为黄绿色气体、C为无色气体。D、E、F、G、H、X均为化合物,其中X常温下是无色气体,其水溶液是一种无氧强酸溶液,E为黑色固体,H在常温下为液体。它们之间的转化关系如图所示(其中某些反应条件和部分反应产物已略去)。

(1)写出下列物质的化学式:D___________ ,X_______________ 。
(2)在反应①~⑦中,不属于氧化还原反应的是_____________ (填编号)。
(3)反应⑥的离子方程式为:______________________________________ 。
(4)往G溶液中加入NaOH溶液观察到的现象是________________________ 。
(5)反应⑦的化学方程式为____________________________________ ;该反应中每消耗0.3mol的A,可转移电子________ mol。
(6)除去D溶液中混有的少量G的化学方程式:_________________ 。

(1)写出下列物质的化学式:D
(2)在反应①~⑦中,不属于氧化还原反应的是
(3)反应⑥的离子方程式为:
(4)往G溶液中加入NaOH溶液观察到的现象是
(5)反应⑦的化学方程式为
(6)除去D溶液中混有的少量G的化学方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】向一定量NaOH溶液的烧杯中通入CO2气体,然后向该溶液中逐滴加入1mol/L盐酸.所加入盐酸溶液的体积与产生二氧化碳气体体积(标准状况)的关系如图所示:

(1)写出OA段所发生反应的离子方程式_____ 。
(2)当加入35mL盐酸时,所产生的二氧化碳的体积(标准状况)是_____ mL。
(3)通入CO2气体后,溶液中所含溶质及溶质的物质的量之比为_____ 。

(1)写出OA段所发生反应的离子方程式
(2)当加入35mL盐酸时,所产生的二氧化碳的体积(标准状况)是
(3)通入CO2气体后,溶液中所含溶质及溶质的物质的量之比为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】I.实验室用固体NaOH配制250mL1.00mol/L的NaOH溶液。请回答下列问题:
(1)配制该溶液需称取NaOH固体___________ g(保留至小数点后一位)。下图中,配制上述溶液不需要的仪器是___________ (填名称)。

(2)配制上述溶液时正确的操作顺序是___________ 。
①继续往容量瓶内小心加水,直到液面接近刻度1~2cm处
③用天平准确称取所需NaOH固体放入烧杯中,加入一定量蒸馏水,并用玻璃棒不断搅拌
③用胶头滴管加水至溶液凹液面与刻度线相切
④将容量瓶盖紧,颠倒摇匀
⑤用适量蒸馏水洗涤烧杯及玻璃棒2~3次,将洗涤液均注入容量瓶,振荡
⑥将已冷却的NaOH溶液沿玻璃棒注入容量瓶中
(3)以下情况会导致所配溶液浓度偏低的是___________(填标号)。
Ⅱ.取上述配得的NaOH溶液150mL,通入一定量的 气体,然后向所得溶液中逐滴加入某浓度的盐酸。产生
气体,然后向所得溶液中逐滴加入某浓度的盐酸。产生 气体的体积(标准状况)与所加入的盐酸的体积之间的关系如图所示。回答下列问题:
气体的体积(标准状况)与所加入的盐酸的体积之间的关系如图所示。回答下列问题:

(4)通入一定量的 气体后溶液溶质为
气体后溶液溶质为___________ (写化学式),其物质的量之比是___________ 。
(5)所加盐酸的浓度为___________ (保留3位有效数字)。
(1)配制该溶液需称取NaOH固体

(2)配制上述溶液时正确的操作顺序是
①继续往容量瓶内小心加水,直到液面接近刻度1~2cm处
③用天平准确称取所需NaOH固体放入烧杯中,加入一定量蒸馏水,并用玻璃棒不断搅拌
③用胶头滴管加水至溶液凹液面与刻度线相切
④将容量瓶盖紧,颠倒摇匀
⑤用适量蒸馏水洗涤烧杯及玻璃棒2~3次,将洗涤液均注入容量瓶,振荡
⑥将已冷却的NaOH溶液沿玻璃棒注入容量瓶中
(3)以下情况会导致所配溶液浓度偏低的是___________(填标号)。
| A.称量时,将NaOH放在纸上称重 | B.配制前,容量瓶中有少量蒸馏水 |
| C.溶解后,未冷却直接转移至容量瓶 | D.定容时,仰视容量瓶的刻度线 |
Ⅱ.取上述配得的NaOH溶液150mL,通入一定量的
 气体,然后向所得溶液中逐滴加入某浓度的盐酸。产生
气体,然后向所得溶液中逐滴加入某浓度的盐酸。产生 气体的体积(标准状况)与所加入的盐酸的体积之间的关系如图所示。回答下列问题:
气体的体积(标准状况)与所加入的盐酸的体积之间的关系如图所示。回答下列问题:
(4)通入一定量的
 气体后溶液溶质为
气体后溶液溶质为(5)所加盐酸的浓度为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】古代的药金外观与金相似,常被误认为是金子,冶炼的方法如下:将碳酸锌、赤铜(Cu2O)、木炭混合加热到800℃,得到金光闪闪的“药金”.
(1)药金的主要成分是______________________________________________________ .
(2)冶炼时发生反应的化学方程式为___________________________________________ .
(1)药金的主要成分是
(2)冶炼时发生反应的化学方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】按要求书写相关化学反应方程式。
(1)生石灰(CaO)吸收水分作干燥剂的反应原理___________ ;
(2)碳60(C60)在空气中充分燃烧生成二氧化碳___________ ;
(3)将铝丝放入硫酸铜的溶液中___________ ;
(4)酒精(C2H5OH)在空气中燃烧___________ 。
(1)生石灰(CaO)吸收水分作干燥剂的反应原理
(2)碳60(C60)在空气中充分燃烧生成二氧化碳
(3)将铝丝放入硫酸铜的溶液中
(4)酒精(C2H5OH)在空气中燃烧
您最近一年使用:0次



