只给出下列甲、乙中对应的量,不能计算出溶液的物质的量浓度的是
| 序号 | ① | ② | ③ | ④ | ⑤ |
| 甲 | 溶质所含微粒数 | 标准状况下气体摩尔体积 | 溶质Na2SO4的质量 | 溶质KCl的质量分数 | 非标准状况下溶质的质量 |
| 乙 | 阿伏加 德罗常数 | 标准状况下气体体积 | 溶液的体积 | 溶液的密度 | 溶质的摩尔质量 |
| A.③ | B.①②④⑤ | C.③④ | D.①②⑤ |
更新时间:2019-09-27 21:47:11
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】已知NA为阿伏加德罗常数的值,下列说法正确的是
| A.16.25gFeCl3完全水解转化为氢氧化铁胶体,生成0.1NA个胶粒 |
| B.6gCH3COOH分子中含有共价键数为0.8NA |
C.1L0.1mol·L-1Na2CO3溶液中含 数为0.1NA 数为0.1NA |
| D.标准状况下的密闭容器中,22.4LNO和11.2LO2混合后,分子总数为NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】NA表示阿伏加德罗常数,如果40 g 某气体中所含有的分子数为2NA,则25 g该气体在标况下的体积是
| A.22.4 L | B.28 L | C.33.6 L | D.40 L |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】在标准状况下,将a L NH3完全溶于水得到V mL氨水,溶液的密度为ρ g·cm-3,溶质的质量分数为w,溶质的物质的量浓度为c mol·L-1.下列叙述中正确的是
① c=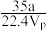 ×100%
×100%
② c=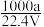
③ 若上述溶液中再加入V mL水后,所得溶液的质量分数小于0.5w
④ 将50 g上述溶液加入一定量的水稀释成0.5c mol·L-1,则加入水的体积应小于50 mL
① c=
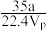 ×100%
×100%② c=
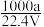
③ 若上述溶液中再加入V mL水后,所得溶液的质量分数小于0.5w
④ 将50 g上述溶液加入一定量的水稀释成0.5c mol·L-1,则加入水的体积应小于50 mL
| A.①④ | B.②③ | C.①③ | D.②④ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】电解质饮料可以补充剧烈运动后流失的水分和电解质。某品牌电解质饮料添加的电解质为NaCl、KCl和MgSO4,其中K+:1.0--27.3 mg/L;Mg2+:0.1--4.8 mg/L,下列说法不正确 的是
| A.NaCl、KCl和MgSO4均为电解质 |
| B.c(K+)最大值为7×10-4 mol/L |
| C.1 L该饮料中含MgSO4的最大质量为12 mg |
| D.若该饮料中c(Cl-)=1×10-3 mol/L,则c(Na⁺)的最小值为3.0×10-4 mol/L |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】现有一混合物的水溶液,可能含有以下离子中的若干种:K+、 、Ba2+、
、Ba2+、 、Cl-、
、Cl-、 。现取两份各100 mL溶液进行如下实验:
。现取两份各100 mL溶液进行如下实验:
①第一份加足量NaOH溶液,加热,收集到气体0.17 g;
②第二份加足量BaCl2溶液后,得干燥沉淀6.63 g,经足量盐酸洗涤、干燥后,剩余沉淀质量为4.66 g。根据上述实验,以下推测正确的是
 、Ba2+、
、Ba2+、 、Cl-、
、Cl-、 。现取两份各100 mL溶液进行如下实验:
。现取两份各100 mL溶液进行如下实验:①第一份加足量NaOH溶液,加热,收集到气体0.17 g;
②第二份加足量BaCl2溶液后,得干燥沉淀6.63 g,经足量盐酸洗涤、干燥后,剩余沉淀质量为4.66 g。根据上述实验,以下推测正确的是
A.一定存在 、 、 、 、 ,一定不存在Ba2+、Cl- ,一定不存在Ba2+、Cl- |
B.一定存在 、 、 、 、 ,可能存在K+ ,可能存在K+ |
| C.溶液中一定存在K+,且c(K+)至少有0.5 mol/L |
D.c( )<c( )<c( )=0.02 mol/L )=0.02 mol/L |
您最近一年使用:0次



