如图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容。据此,下列说法正确的是


| A.该硫酸的物质的量浓度为9.2 mol·L-1 |
| B.该硫酸与等体积的水混合所得溶液的质量分数小于49% |
| C.配制250mL 4.6 mol·L-1的稀硫酸需取该硫酸62.5mL |
| D.该硫酸50.0mL与足量的铜反应可得到标准状况下SO2气体10.304 L |
19-20高三上·黑龙江牡丹江·阶段练习 查看更多[3]
黑龙江省牡丹江市第三高级中学2020届高三上学期第二次月考化学试题(已下线)4.1.2 硫酸的工业制备 浓硫酸的性质练习(2)——《高中新教材同步备课》(苏教版 必修第一册)甘肃省武威市第六中学2020届高三上学期第三次阶段性复习过关考试化学试题
更新时间:2019-10-16 20:01:26
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】下图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容。该硫酸的物质的量浓度为


| A.9.2mol/L | B.12.3mol/L | C.18.4mol/L | D.20.0mol/L |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】将30mL 0.5mol•L的稀硫酸加水稀释到500mL,稀释后稀硫酸的溶质的物质的量浓度为
| A.0.03mol/L | B.0.3mol/L | C.0.05mol/L | D.0.15mol/L |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】设NA为阿伏伽德罗常数的数值。下列说法不正确的是
| A.23gCH3CH2OH与30gCH3COOH反应,生成CH3COOCH2CH3的分子数为0.5NA |
| B.15.6g由Na2S和Na2O2组成的混合物中,含有的阴离子数目为0.2NA |
| C.32.5g锌与一定量浓硫酸恰好完全反应,生成气体的分子数为0.5NA |
| D.过量MnO2与浓盐酸反应产生1molCl2,转移的电子数目为2NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】将6.4 g铜片和10 mL 18 mol·L-1的浓硫酸放在圆底烧瓶中共热,直到无气体生成,小李同学根据所学的化学知识认为还有一定量的硫酸剩余。为了定量或定性地分析剩余硫酸,下列实验方案设计可达到目的的是
| A.铁粉、氯化钡溶液和碳酸氢钠溶液均能够用来证明反应结束后的烧瓶中确有硫酸剩余 |
| B.为定量测定剩余硫酸浓度,可将产生的气体缓缓通过预先称量过的盛有碱石灰的干燥管,结束反应后再次称量,发现干燥管质量增加m1 g。 |
| C.为定量测定剩余硫酸浓度,将气体缓缓通入足量硝酸钡溶液中,然后过滤、洗涤、干燥,称得沉淀的质量为m2 g |
| D.为定量测定剩余硫酸浓度,分离出反应后的溶液(假定反应前后烧瓶中溶液的体积不变)并加蒸馏水稀释至1 000 mL,取20.00 mL于锥形瓶中,滴入2~3滴酚酞指示剂,用标准NaOH溶液进行滴定(已知氢氧化铜开始沉淀的pH约为5),可求出剩余硫酸的浓度 |
您最近一年使用:0次


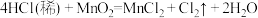
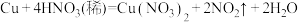
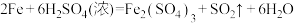
 通入次氯酸钠溶液中:
通入次氯酸钠溶液中:


