自然界中氢有_______ 种同位素,他们的中文名分别为________________ ,若用符号来表示,则分别为______________ ,自然界中氧也有三种同位素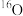 、
、 、
、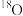 ,从水分子的原子组成来看,自然界中的水分子理论上有
,从水分子的原子组成来看,自然界中的水分子理论上有____________ 种,这些水分子的相对分子质量有__________ 种。
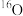 、
、 、
、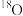 ,从水分子的原子组成来看,自然界中的水分子理论上有
,从水分子的原子组成来看,自然界中的水分子理论上有
更新时间:2019-10-30 03:19:15
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】原子、元素、核素、同位素等都属于重要的化学基本概念。下列八种化学符号: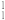 H、
H、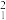 H、
H、 C、
C、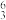 Li、
Li、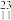 Na、
Na、 N、
N、 Li、
Li、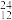 Mg
Mg
(1)涉及的核素共有__ 种;
(2)互为同位素的是__ 、__ ;
(3)质量数相等,但不能互称为同位素的是__ ;
(4)中子数相等,但质子数不相等的是__ 。
(5)氢的三种同位素是__ ,它们与氯的同位素35Cl、37Cl相互结合为氯化氢,可得氯化氢分子的种数为__ 。
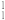 H、
H、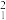 H、
H、 C、
C、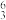 Li、
Li、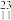 Na、
Na、 N、
N、 Li、
Li、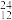 Mg
Mg(1)涉及的核素共有
(2)互为同位素的是
(3)质量数相等,但不能互称为同位素的是
(4)中子数相等,但质子数不相等的是
(5)氢的三种同位素是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】填表:
| 微粒 | 核外电子数 | 中子数 | 质量数 | 最外层电子数 |
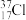 | ||||
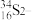 |
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】Na、Fe、Al是中学化学常见的金属元素。回答下列问题:
(1)焰色反应的实验中,Na元素燃烧时的焰色为_______ 色,观察K元素燃烧时的焰色需要透过_______ 。
(2)碘元素的一种核素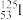 可用于治疗肿瘤。该核素的质子数为
可用于治疗肿瘤。该核素的质子数为_______ ,中子数为_______ ,质量数为_______ ,核外电子数为_______ 。(对应数值125和53)
(1)焰色反应的实验中,Na元素燃烧时的焰色为
(2)碘元素的一种核素
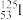 可用于治疗肿瘤。该核素的质子数为
可用于治疗肿瘤。该核素的质子数为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】宏微结合是研究化学的重要方法,从微观的角度了解物质及其变化,有助于更好地认识物质的组成和变化的本质。
I.
(1)下表为部分元素的原子结构示意图:
①表中硫元素的核电荷数x=___________ 。
②R3+离子与氖原子的核外电子排布相同,则R元素为___________ 元素(填元素名称)。
③一个水分子中所含电子总数为___________ 。
④硫元素与氧元素的化学性质相似的原因是___________ 。
(2)甲和乙在一定条件下反应生成丙和丁,反应的微观模型如图所示。

①该反应的生成物中,属于氧化物的是___________ (填化学式)
②每个甲分子是由___________ 构成的。
③参加反应的甲和乙分子个数比为___________ 。
(3)如图是稀硫酸与甲溶液发生复分解反应的微观模型,请写出一种符合图示的a微粒的符号:___________ 。

II.人们在实验研究中总结出常见金属的活动性顺序:

(4)请在表中 内填写对应的元素符号
内填写对应的元素符号___________ 。
(5)Mg、Sn、Pb、Cu、Ag五种金属,能与稀盐酸(或稀硫酸)发生置换反应的金属有___________ 种;写出其中最活泼的金属与稀盐酸反应的化学方程式___________ 。
I.
(1)下表为部分元素的原子结构示意图:
| 元素名称 | 氢 | 氧 | 氟 | 氖 | 钠 | 硫 | 氯 |
| 原子结构示意图 | 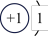 |  | 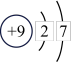 | 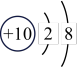 |  | 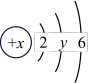 |  |
②R3+离子与氖原子的核外电子排布相同,则R元素为
③一个水分子中所含电子总数为
④硫元素与氧元素的化学性质相似的原因是
(2)甲和乙在一定条件下反应生成丙和丁,反应的微观模型如图所示。

①该反应的生成物中,属于氧化物的是
②每个甲分子是由
③参加反应的甲和乙分子个数比为
(3)如图是稀硫酸与甲溶液发生复分解反应的微观模型,请写出一种符合图示的a微粒的符号:

II.人们在实验研究中总结出常见金属的活动性顺序:

(4)请在表中
 内填写对应的元素符号
内填写对应的元素符号(5)Mg、Sn、Pb、Cu、Ag五种金属,能与稀盐酸(或稀硫酸)发生置换反应的金属有
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】阴离子Xn-含中子N个,X的质量数为A,则m g X元素的气态氢化物所含质子数的物质的量是_______ 。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】用序号按要求回答下列问题:
(1)下列各组微粒: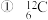 与
与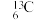
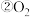 和
和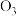
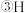 、D、
、D、 金刚石和石墨
金刚石和石墨 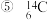 和
和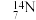 ,互为同位素的是
,互为同位素的是_________ ;互为同素异形体的是________ ;质量数相等,但不能互称为同位素的是 ______ 。
(2)下列各种物质:
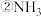
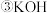 ④Na2O2 ⑤MgCl2
④Na2O2 ⑤MgCl2 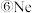 ,不存在化学键的是
,不存在化学键的是______ ;只存在离子键的是______ ;属于共价化合物的是________ ;含非极性键的离子化合物是 _________ 。
(3)下列变化过程: 碘的升华
碘的升华  NaCl固体溶于水
NaCl固体溶于水  O2溶于水
O2溶于水  HCl气体溶于水
HCl气体溶于水 烧碱熔化
烧碱熔化  氯化铵受热分解,化学键没有被破坏的是
氯化铵受热分解,化学键没有被破坏的是__________ ; 仅破坏离子键的是__________ ;仅破坏共价键的是__________ 。
(1)下列各组微粒:
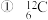 与
与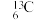
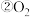 和
和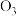
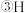 、D、
、D、 金刚石和石墨
金刚石和石墨 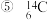 和
和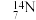 ,互为同位素的是
,互为同位素的是(2)下列各种物质:

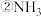
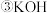 ④Na2O2 ⑤MgCl2
④Na2O2 ⑤MgCl2 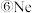 ,不存在化学键的是
,不存在化学键的是(3)下列变化过程:
 碘的升华
碘的升华  NaCl固体溶于水
NaCl固体溶于水  O2溶于水
O2溶于水  HCl气体溶于水
HCl气体溶于水 烧碱熔化
烧碱熔化  氯化铵受热分解,化学键没有被破坏的是
氯化铵受热分解,化学键没有被破坏的是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】化学与生产、生活息息相关,回答下列问题:
(1)丹霞地貌的岩层因含___________ (填化学式)而呈红色。
(2)钠着火了,___________ (填能或不能,下同)用水灭火,实验中没用完的钠块___________ 放回原瓶。
(3)碘元素的一种核素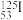 可用于治疗肿瘤。该核素的中子数为
可用于治疗肿瘤。该核素的中子数为___________ ,核外电子数为___________ 。
(4)胃液中含有盐酸,胃酸过多的人常有胃疼烧心的感觉。 和
和 都能治疗胃酸过多,如果病人同时患有胃溃疡,最好用含
都能治疗胃酸过多,如果病人同时患有胃溃疡,最好用含___________ (填化学式)的胃药。 电离方程式为
电离方程式为___________ 。
(5)我国向国际社会承诺,2030年实现“碳达峰”,2060年实现“碳中和”。降低 含量可以用NaOH溶液来“捕捉”,将
含量可以用NaOH溶液来“捕捉”,将 “储存”或“利用”。将一定量的
“储存”或“利用”。将一定量的 通入足量NaOH溶液时发生的离子反应方程式为
通入足量NaOH溶液时发生的离子反应方程式为___________ 。
(6)高铁酸钠( )是一种新型绿色消毒剂,主要用于饮用水处理。一种制备高铁酸钠的方法如下,请配平该离子反应方程式:
)是一种新型绿色消毒剂,主要用于饮用水处理。一种制备高铁酸钠的方法如下,请配平该离子反应方程式:_________

(1)丹霞地貌的岩层因含
(2)钠着火了,
(3)碘元素的一种核素
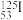 可用于治疗肿瘤。该核素的中子数为
可用于治疗肿瘤。该核素的中子数为(4)胃液中含有盐酸,胃酸过多的人常有胃疼烧心的感觉。
 和
和 都能治疗胃酸过多,如果病人同时患有胃溃疡,最好用含
都能治疗胃酸过多,如果病人同时患有胃溃疡,最好用含 电离方程式为
电离方程式为(5)我国向国际社会承诺,2030年实现“碳达峰”,2060年实现“碳中和”。降低
 含量可以用NaOH溶液来“捕捉”,将
含量可以用NaOH溶液来“捕捉”,将 “储存”或“利用”。将一定量的
“储存”或“利用”。将一定量的 通入足量NaOH溶液时发生的离子反应方程式为
通入足量NaOH溶液时发生的离子反应方程式为(6)高铁酸钠(
 )是一种新型绿色消毒剂,主要用于饮用水处理。一种制备高铁酸钠的方法如下,请配平该离子反应方程式:
)是一种新型绿色消毒剂,主要用于饮用水处理。一种制备高铁酸钠的方法如下,请配平该离子反应方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】有下列各组物质:(A)O2和O3;(B)23592U和23892U;(C) CH3CH2CH2CH3和 ;(D)
;(D)  和
和 ;(E)甲烷和新戊烷。
;(E)甲烷和新戊烷。
(1)__________ 组两物质互为同位素;
(2)__________ 组两物质互为同素异形体;
(3)__________ 组两物质互为同系物;
(4)__________ 组两物质互为同分异构体。
 ;(D)
;(D)  和
和 ;(E)甲烷和新戊烷。
;(E)甲烷和新戊烷。(1)
(2)
(3)
(4)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】(1)下列各组中:
①金刚石 ②12C ③液氯 ④ 14C ⑤CH3CH2CH2CH3 ⑥氯水
⑦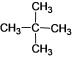 ⑧
⑧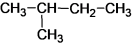 ⑨C60。
⑨C60。
属于同素异形体的是__________ (用序号回答 ,下同),属于同分异构体的是________ ,属于同位素的是______________ 。
(2)有a、MgBr2;b、金刚石;c、NaOH;d、干冰四种物质,按下列要求回答(用字母序号回答 ):
①熔化时不需要破坏化学键的是________ ,熔化时需要破坏共价键的是_________ ,熔点最高的是_____________ 。
②只有离子键的物质是___________ ,既有离子键又有共价键的物质是_________ ,晶体以分子间作用力结合的是______________ 。
(3)已知0.2mol烷烃在足量氧气中完全燃烧,测得生成CO2气体的体积为17.92L(标况下),则该烷烃的分子式为_________________ ,写出比该烃多1个碳的同系物,且其分子结构中含有3个甲基(-CH3)的结构简式______________________________ 。
①金刚石 ②12C ③液氯 ④ 14C ⑤CH3CH2CH2CH3 ⑥氯水
⑦
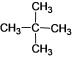 ⑧
⑧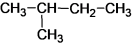 ⑨C60。
⑨C60。属于同素异形体的是
(2)有a、MgBr2;b、金刚石;c、NaOH;d、干冰四种物质,按下列要求回答(
①熔化时不需要破坏化学键的是
②只有离子键的物质是
(3)已知0.2mol烷烃在足量氧气中完全燃烧,测得生成CO2气体的体积为17.92L(标况下),则该烷烃的分子式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】由以下一些微粒: 、
、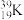 、
、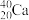 、
、 、
、 、
、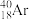 。其中:
。其中:
(1)互为同位素的是________ 和________ ;
(2)质量数相等,但不能互称同位素的是________ 和__________ ;
(3)中子数相等,但质子数不相等的是______ 和______ 、______ 和______ 。
 、
、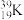 、
、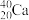 、
、 、
、 、
、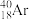 。其中:
。其中:(1)互为同位素的是
(2)质量数相等,但不能互称同位素的是
(3)中子数相等,但质子数不相等的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】某文献资料上记载的相对原子质量数据摘录如表所示:
(1)则65Cu的相对原子质量=____ (保留三位小数)。
常温下,向20mL0.1mol·L-1的硫酸中逐滴加入相同物质的量浓度的Ba(OH)2溶液,生成沉淀的质量与加入Ba(OH)2溶液的体积关系如图所示:

(2)判断溶液处于A、B、C时的酸碱性,A:____ ;B:____ ;C:____ 。
(3)溶液处于____ 点时的导电性最弱,写出该处发生的化学反应的离子方程式:____ 。
向含有I-和Cl-的稀溶液中滴入AgNO3溶液,产生沉淀的质量与加入AgNO3溶液体积的关系如图所示。
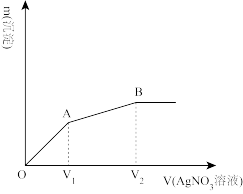
(4)OA段反应生成黄色沉淀,该黄色沉淀的化学式:____ 。
(5)AB段反应生成白色沉淀,写出生成该沉淀的离子方程式:____ 。
(6)原溶液中c(I-):c(Cl-)的比值为:____ (用V1、V2表示)。
| 原子 | 相对原子质量 | 质量数 | 丰度 | 元素的相对原子质量 | 元素的近似相对原子质量 |
| 63Cu | 62.928 | 63 | 69.15% | 63.546 | 63.618 |
| 65Cu | 65 | 30.85% |
常温下,向20mL0.1mol·L-1的硫酸中逐滴加入相同物质的量浓度的Ba(OH)2溶液,生成沉淀的质量与加入Ba(OH)2溶液的体积关系如图所示:

(2)判断溶液处于A、B、C时的酸碱性,A:
(3)溶液处于
向含有I-和Cl-的稀溶液中滴入AgNO3溶液,产生沉淀的质量与加入AgNO3溶液体积的关系如图所示。

(4)OA段反应生成黄色沉淀,该黄色沉淀的化学式:
(5)AB段反应生成白色沉淀,写出生成该沉淀的离子方程式:
(6)原溶液中c(I-):c(Cl-)的比值为:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】按要求填空
(1) 中有
中有_______  质子,
质子,_______  中子,
中子,_______ 个电子。
(2)同温同压下,两种气体A和B的体积比为2∶1,质量比为8∶5,摩尔质量之比为_______ 。
(3)同温同压下,同体积的氨气和硫化氢气体的质量比是_______ ;同质量的氨气和硫化氢气体的体积比是_______ ;若两者所含氢原子个数相同,它们的物质的量之比为_______ 。
(4)某混合气体中,各气体的体积分数为: 、
、 、
、 、
、 ,则此混合气体的平均相对分子质量为
,则此混合气体的平均相对分子质量为_______ ,其对于氢气的密度为_______ 。
(5)在 、
、 下,有
下,有 和
和 混合气体共
混合气体共 ,经点燃后恢复到原状态时,混合气体的体积减少为
,经点燃后恢复到原状态时,混合气体的体积减少为 ,则原混合气体中
,则原混合气体中 的体积为
的体积为_______  。
。
(6)将某文献资料上记载的相对原子质量数据摘录如表所示:
则 的相对原子质量=
的相对原子质量=_______ (保留三位小数)。
(7)在 、
、 、
、 、
、 、
、 等物质中,只存在离子键的是
等物质中,只存在离子键的是_______ ;只存在共价键的是_______ ;既存在离子键又存在共价键的是_______ ;不存在化学键的是_______ 。
(8)下列变化中:①碘的升华;②烧碱熔化;③氯化钠溶于水;④氧气溶于水;⑤氯化氢溶于水;⑥氯化铵受热分解为氯化氢和氨气。(填序号)。化学键没有被破坏的是_______ ;仅发生离子键破坏的是_______ ;仅发生共价键破坏的是_______ ;既发生离子键又发生共价键破坏的是_______ 。
(1)
 中有
中有 质子,
质子, 中子,
中子,(2)同温同压下,两种气体A和B的体积比为2∶1,质量比为8∶5,摩尔质量之比为
(3)同温同压下,同体积的氨气和硫化氢气体的质量比是
(4)某混合气体中,各气体的体积分数为:
 、
、 、
、 、
、 ,则此混合气体的平均相对分子质量为
,则此混合气体的平均相对分子质量为(5)在
 、
、 下,有
下,有 和
和 混合气体共
混合气体共 ,经点燃后恢复到原状态时,混合气体的体积减少为
,经点燃后恢复到原状态时,混合气体的体积减少为 ,则原混合气体中
,则原混合气体中 的体积为
的体积为 。
。(6)将某文献资料上记载的相对原子质量数据摘录如表所示:
| 原子 | 相对原子质量 | 质量数 | 丰度 | 元素的相对原子质量 | 元素的近似相对原子质量 |
 | 62.928 | 63 | 69.15% | 63.546 | 63.618 |
 | _______ | 65 | 30.85% |
则
 的相对原子质量=
的相对原子质量=(7)在
 、
、 、
、 、
、 、
、 等物质中,只存在离子键的是
等物质中,只存在离子键的是(8)下列变化中:①碘的升华;②烧碱熔化;③氯化钠溶于水;④氧气溶于水;⑤氯化氢溶于水;⑥氯化铵受热分解为氯化氢和氨气。(填序号)。化学键没有被破坏的是
您最近一年使用:0次



