化学与生产、生活息息相关,回答下列问题:
(1)丹霞地貌的岩层因含___________ (填化学式)而呈红色。
(2)钠着火了,___________ (填能或不能,下同)用水灭火,实验中没用完的钠块___________ 放回原瓶。
(3)碘元素的一种核素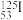 可用于治疗肿瘤。该核素的中子数为
可用于治疗肿瘤。该核素的中子数为___________ ,核外电子数为___________ 。
(4)胃液中含有盐酸,胃酸过多的人常有胃疼烧心的感觉。 和
和 都能治疗胃酸过多,如果病人同时患有胃溃疡,最好用含
都能治疗胃酸过多,如果病人同时患有胃溃疡,最好用含___________ (填化学式)的胃药。 电离方程式为
电离方程式为___________ 。
(5)我国向国际社会承诺,2030年实现“碳达峰”,2060年实现“碳中和”。降低 含量可以用NaOH溶液来“捕捉”,将
含量可以用NaOH溶液来“捕捉”,将 “储存”或“利用”。将一定量的
“储存”或“利用”。将一定量的 通入足量NaOH溶液时发生的离子反应方程式为
通入足量NaOH溶液时发生的离子反应方程式为___________ 。
(6)高铁酸钠( )是一种新型绿色消毒剂,主要用于饮用水处理。一种制备高铁酸钠的方法如下,请配平该离子反应方程式:
)是一种新型绿色消毒剂,主要用于饮用水处理。一种制备高铁酸钠的方法如下,请配平该离子反应方程式:_________

(1)丹霞地貌的岩层因含
(2)钠着火了,
(3)碘元素的一种核素
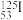 可用于治疗肿瘤。该核素的中子数为
可用于治疗肿瘤。该核素的中子数为(4)胃液中含有盐酸,胃酸过多的人常有胃疼烧心的感觉。
 和
和 都能治疗胃酸过多,如果病人同时患有胃溃疡,最好用含
都能治疗胃酸过多,如果病人同时患有胃溃疡,最好用含 电离方程式为
电离方程式为(5)我国向国际社会承诺,2030年实现“碳达峰”,2060年实现“碳中和”。降低
 含量可以用NaOH溶液来“捕捉”,将
含量可以用NaOH溶液来“捕捉”,将 “储存”或“利用”。将一定量的
“储存”或“利用”。将一定量的 通入足量NaOH溶液时发生的离子反应方程式为
通入足量NaOH溶液时发生的离子反应方程式为(6)高铁酸钠(
 )是一种新型绿色消毒剂,主要用于饮用水处理。一种制备高铁酸钠的方法如下,请配平该离子反应方程式:
)是一种新型绿色消毒剂,主要用于饮用水处理。一种制备高铁酸钠的方法如下,请配平该离子反应方程式:
更新时间:2022-01-27 19:32:36
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】完成下列问题:
(1)现有下列十种物质:①铜;②小苏打;③固体纯碱;④二氧化碳;⑤葡萄糖;⑥氢氧化钾;⑦氢氧化铁胶体;⑧盐酸;⑨乙醇;⑩硫酸铁。上述十种物质中,属于混合物的是_______ (填序号),⑩的电离方程式为_______ 。
(2)下列物质属于如图所示化学概念交叉部分(阴影部分)的是_______ 。 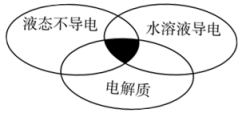
A. B.HCl C.
B.HCl C. (乙醇) D .NaCl E.Hg
(乙醇) D .NaCl E.Hg
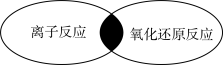
(3)下列各反应属于如图中阴影部分所示关系的有_______。
(4)高铁酸钠( )是一种新型绿色消毒剂
)是一种新型绿色消毒剂
①其中一种制备 的离子方程式可表示为:
的离子方程式可表示为:  ____
____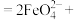 _______
_______ _______
_______
请补全以上反应,并用双线桥法表示电子转移的方向和数目_____ 。
②已知: 在处理饮用水的过程中铁元素会被转化为
在处理饮用水的过程中铁元素会被转化为 ,进而
,进而 在水中产生
在水中产生 胶体,
胶体, 胶体具有吸附性。
胶体具有吸附性。 在处理饮用水的过程中发生了
在处理饮用水的过程中发生了_______ (填“氧化”、“还原”或“非氧化还原”)反应。 胶体为
胶体为_______ 色,写出区分胶体与溶液的实验方法名称:_______ 。
(1)现有下列十种物质:①铜;②小苏打;③固体纯碱;④二氧化碳;⑤葡萄糖;⑥氢氧化钾;⑦氢氧化铁胶体;⑧盐酸;⑨乙醇;⑩硫酸铁。上述十种物质中,属于混合物的是
(2)下列物质属于如图所示化学概念交叉部分(阴影部分)的是

A.
 B.HCl C.
B.HCl C. (乙醇) D .NaCl E.Hg
(乙醇) D .NaCl E.Hg(3)下列各反应属于如图中阴影部分所示关系的有_______。

| A.氨气与盐酸 | B.氢气与氧气 | C.过氧化钠与水 | D.氯气与氢氧化钠溶液 |
 )是一种新型绿色消毒剂
)是一种新型绿色消毒剂①其中一种制备
 的离子方程式可表示为:
的离子方程式可表示为:  ____
____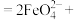 _______
_______ _______
_______
请补全以上反应,并用双线桥法表示电子转移的方向和数目
②已知:
 在处理饮用水的过程中铁元素会被转化为
在处理饮用水的过程中铁元素会被转化为 ,进而
,进而 在水中产生
在水中产生 胶体,
胶体, 胶体具有吸附性。
胶体具有吸附性。 在处理饮用水的过程中发生了
在处理饮用水的过程中发生了 胶体为
胶体为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】化学与人类生活息息相关,请根据所学知识回答下列问题
现有以下物质:①Ba(OH)2•8H2O,②漂白粉,③食醋,④石墨,⑤四氯化碳,⑥NaHSO4水溶液,请回答下列问题(填序号):
Ⅰ.以上物质中属于电解质的是___ 。
Ⅱ.以上物质中属于非电解质的是___ 。
Ⅲ.请写出NaHSO4在水中的电离方程式__ 。
现有以下物质:①Ba(OH)2•8H2O,②漂白粉,③食醋,④石墨,⑤四氯化碳,⑥NaHSO4水溶液,请回答下列问题(填序号):
Ⅰ.以上物质中属于电解质的是
Ⅱ.以上物质中属于非电解质的是
Ⅲ.请写出NaHSO4在水中的电离方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】阅读下列科普短文并填空:
海洋约占地球表面积的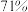 ,其中水资源和其他化学资源具有巨大的开发潜力。海水中含有多种盐类,如
,其中水资源和其他化学资源具有巨大的开发潜力。海水中含有多种盐类,如 、
、 等。目前,通过海水晒盐可制得食盐晶体和苦卤,食盐精制后可制成饱和
等。目前,通过海水晒盐可制得食盐晶体和苦卤,食盐精制后可制成饱和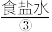 用以生产
用以生产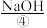 、
、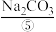 、
、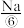 、
、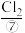 、
、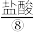 等,苦卤经过氯气氧化,热空气吹出、
等,苦卤经过氯气氧化,热空气吹出、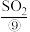 吸收等一系列操作可获得
吸收等一系列操作可获得 。海水淡化与化工生产、能源开发等相结合已经成为海水综合利用的重要方向。
。海水淡化与化工生产、能源开发等相结合已经成为海水综合利用的重要方向。
(1)上述标有序号的物质中属于电解质的是___________ (填序号,下同);属于非电解质的是___________ ;能导电的物质是___________ 。
(2)写出⑤溶于水的电离方程式:___________ 。将少量的⑤溶于装有 蒸馏水的烧杯中后,逐滴加入⑧观察到刚开始并没有出现气泡,一段时间后出现气泡,则出现该现象的原因是
蒸馏水的烧杯中后,逐滴加入⑧观察到刚开始并没有出现气泡,一段时间后出现气泡,则出现该现象的原因是___________ ,写出对应反应的离子方程式:______ ,______ 。
(3)海水提溴的过程中涉及的反应有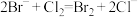 ,
, ,根据上述反应可判断
,根据上述反应可判断 、
、 、
、 的还原性由强到弱的顺序为
的还原性由强到弱的顺序为___________ 。
海洋约占地球表面积的
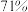 ,其中水资源和其他化学资源具有巨大的开发潜力。海水中含有多种盐类,如
,其中水资源和其他化学资源具有巨大的开发潜力。海水中含有多种盐类,如 、
、 等。目前,通过海水晒盐可制得食盐晶体和苦卤,食盐精制后可制成饱和
等。目前,通过海水晒盐可制得食盐晶体和苦卤,食盐精制后可制成饱和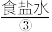 用以生产
用以生产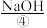 、
、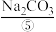 、
、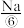 、
、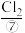 、
、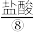 等,苦卤经过氯气氧化,热空气吹出、
等,苦卤经过氯气氧化,热空气吹出、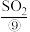 吸收等一系列操作可获得
吸收等一系列操作可获得 。海水淡化与化工生产、能源开发等相结合已经成为海水综合利用的重要方向。
。海水淡化与化工生产、能源开发等相结合已经成为海水综合利用的重要方向。(1)上述标有序号的物质中属于电解质的是
(2)写出⑤溶于水的电离方程式:
 蒸馏水的烧杯中后,逐滴加入⑧观察到刚开始并没有出现气泡,一段时间后出现气泡,则出现该现象的原因是
蒸馏水的烧杯中后,逐滴加入⑧观察到刚开始并没有出现气泡,一段时间后出现气泡,则出现该现象的原因是(3)海水提溴的过程中涉及的反应有
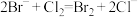 ,
, ,根据上述反应可判断
,根据上述反应可判断 、
、 、
、 的还原性由强到弱的顺序为
的还原性由强到弱的顺序为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】回答下列问题:
(1)化学与生活、生产息息相关。
① 可用于制备纯碱; ②
可用于制备纯碱; ② 可用于葡萄酒保存;
可用于葡萄酒保存;
③ 可用于制供氧剂; ④
可用于制供氧剂; ④ 可用于制耐火材料;
可用于制耐火材料;
⑤CO可用于冶炼金属; ⑥ 可用于制硫酸;
可用于制硫酸;
⑦ 可用于制硝酸
可用于制硝酸
上述物质中,属于酸性氧化物的是______________________ (填序号)。
(2)硝酸是用途广泛的重要化工原科。氨的催化氧化是工业合成硝酸的重要步骤,其中氧化剂与还原剂物质的量之比为___________ 。
(3)央视《每周质量报告》曝光了河北省一些明胶企业将皮革废料熬制成工业明胶,出售给浙江绍兴某些制药企业,最终变成药用胶囊。明胶是水溶性蛋白质混合物,溶于水形成胶体。明胶的水溶液与NaCl溶液的共同点是___________ (填序号)。
A.都可以产生丁达尔效应 B.都属于混合物 C.都能透过滤纸
(4)氮、磷都是生命元素,它们的氢化物结构相似。 的沸点
的沸点___________  的沸点(填“>”或“<”)。
的沸点(填“>”或“<”)。
(5)经研究,发现可能存在第119号元素,有人称“类纺”,其位于元素周期表第八周期ⅠA族。有关“类钫”的预测正确的是 。
(6)实验室中 溶液久置后出现浑浊,请写出发生的化学反应方程式
溶液久置后出现浑浊,请写出发生的化学反应方程式_________________________ 。
(7)氰气[ ]称为拟卤素,与
]称为拟卤素,与 结构相似、性质相近。在
结构相似、性质相近。在 中元素
中元素___________ (写元素符号)显负价。
(1)化学与生活、生产息息相关。
①
 可用于制备纯碱; ②
可用于制备纯碱; ② 可用于葡萄酒保存;
可用于葡萄酒保存;③
 可用于制供氧剂; ④
可用于制供氧剂; ④ 可用于制耐火材料;
可用于制耐火材料;⑤CO可用于冶炼金属; ⑥
 可用于制硫酸;
可用于制硫酸;⑦
 可用于制硝酸
可用于制硝酸上述物质中,属于酸性氧化物的是
(2)硝酸是用途广泛的重要化工原科。氨的催化氧化是工业合成硝酸的重要步骤,其中氧化剂与还原剂物质的量之比为
(3)央视《每周质量报告》曝光了河北省一些明胶企业将皮革废料熬制成工业明胶,出售给浙江绍兴某些制药企业,最终变成药用胶囊。明胶是水溶性蛋白质混合物,溶于水形成胶体。明胶的水溶液与NaCl溶液的共同点是
A.都可以产生丁达尔效应 B.都属于混合物 C.都能透过滤纸
(4)氮、磷都是生命元素,它们的氢化物结构相似。
 的沸点
的沸点 的沸点(填“>”或“<”)。
的沸点(填“>”或“<”)。(5)经研究,发现可能存在第119号元素,有人称“类纺”,其位于元素周期表第八周期ⅠA族。有关“类钫”的预测正确的是 。
| A.“类钫”单质具有强氧化性 | B.“类钫”单质能与冷水剧烈反应 |
| C.“类钫”最高价氧化物对应的水化物为弱碱 | D.“类钫”在化合物中显+1价 |
 溶液久置后出现浑浊,请写出发生的化学反应方程式
溶液久置后出现浑浊,请写出发生的化学反应方程式(7)氰气[
 ]称为拟卤素,与
]称为拟卤素,与 结构相似、性质相近。在
结构相似、性质相近。在 中元素
中元素
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】纯过氧化氢(H2O2,俗称双氧水)是淡蓝色的粘稠液体,可任意比例与水混溶。双氧水在医疗以及生产、生活中有广泛的应用。请分析在下列反应中,H2O2的作用(填写“氧化剂”或“还原剂”),并用单线桥标出反应过程中电子转移方向和数目。
(1)双氧水在氧化剂的作用下,可定量地产生O2,这在分析化学中,具有重要的意义。
___________ 。反应中,H2O2在反应中的作用是___________ 。
(2)双氧水曾在文艺复兴时期的油画修复中发挥很大的作用。其中发生的反应是:
___________ 。反应中,H2O2在反应中的作用是___________ 。
(3)稀释以后的双氧水常用于医疗中的杀菌消毒,使用过程中可见有气体产生,涉及到的反应有:
___________ 。H2O2在反应中的作用是___________ 。
(4)将双氧水滴加到FeCl3溶液中,也会产生有趣的现象。
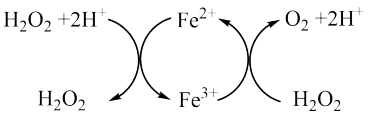
虽说H2O2可以将Fe2+氧化为Fe3+,可是反应中依然有气体生成。研究表明,在此主要涉及到Fe2+、Fe3+和H2O2发生的循环反应(如图)。请根据图示,写出两个相应反应的离子方程式。___________ 、___________
(1)双氧水在氧化剂的作用下,可定量地产生O2,这在分析化学中,具有重要的意义。

(2)双氧水曾在文艺复兴时期的油画修复中发挥很大的作用。其中发生的反应是:

(3)稀释以后的双氧水常用于医疗中的杀菌消毒,使用过程中可见有气体产生,涉及到的反应有:

(4)将双氧水滴加到FeCl3溶液中,也会产生有趣的现象。
虽说H2O2可以将Fe2+氧化为Fe3+,可是反应中依然有气体生成。研究表明,在此主要涉及到Fe2+、Fe3+和H2O2发生的循环反应(如图)。请根据图示,写出两个相应反应的离子方程式。

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】2.2010年第41届世博会将在上海举办,世博会的主题是“城市,让生活更美好”。回答下列问题:
①世博园地区的改造提升了上海的环境质量,位于规划区的一座大型钢铁厂搬迁后,附近居民将不再受到该厂产生的棕红色烟尘的困扰.你认为棕红色烟尘是______________
A.CaCO3粉尘 B.P2O5粉尘 C.Fe2O3粉尘 D.SiO2粉尘
②上海白龙港污水处理厂升级改造,处理废水时加入明矾可作为混凝剂以吸附水中的杂质,明矾的化学式为_________________ ;利用漂白粉可用来杀菌消毒,工业上利用氯气和石灰水制取漂白粉的化学反应方程式是___________________________________ 。
③低碳经济是以低能耗、低污染、低排放为基础的经济模式,上海世博会的亮点之一是实现“二氧化碳零排放”。现在人们使用乙醇汽油作为汽车燃料充分体现了低碳经济,物质的量相同的乙醇与汽油(设为C8H18)均完全燃烧产生的CO2的物质的量之比为______________ ;
④世博会期间将用可降解的“玉米塑料”替代一次性饭盒、并可被用来制作世博会证件及胸卡,目的是为了防止产生___________ 污染。
①世博园地区的改造提升了上海的环境质量,位于规划区的一座大型钢铁厂搬迁后,附近居民将不再受到该厂产生的棕红色烟尘的困扰.你认为棕红色烟尘是
A.CaCO3粉尘 B.P2O5粉尘 C.Fe2O3粉尘 D.SiO2粉尘
②上海白龙港污水处理厂升级改造,处理废水时加入明矾可作为混凝剂以吸附水中的杂质,明矾的化学式为
③低碳经济是以低能耗、低污染、低排放为基础的经济模式,上海世博会的亮点之一是实现“二氧化碳零排放”。现在人们使用乙醇汽油作为汽车燃料充分体现了低碳经济,物质的量相同的乙醇与汽油(设为C8H18)均完全燃烧产生的CO2的物质的量之比为
④世博会期间将用可降解的“玉米塑料”替代一次性饭盒、并可被用来制作世博会证件及胸卡,目的是为了防止产生
您最近一年使用:0次
【推荐2】铁(Fe)钴(Co)镍(Ni)合金是一种典型的软磁材料,具有优异的磁导率和饱和磁感应强度,可用于电感器、传感器和电磁设备等领域。
(1)中国古代就对磁性材料有研究,四大发明之一的司南是由天然磁石制成的,其主要成分是___________ (选填编号)。
a.Fe b.FeO c. d.
d.
(2)铁的原子结构示意图为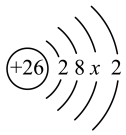 。由此可知,铁是第
。由此可知,铁是第___________ 周期元素,铁原子核外3d轨道上共填充了___________ 个电子。
(3)钴(Co)元素基态原子的电子排布式为___________ ,处于元素周期表的___________ 区。
(4)基态镍(Ni)原子的价电子轨道表示式为___________ 。
(5)磁性材料原子中的未配对电子对其磁性起主要作用,含 磁性材料的磁性比含
磁性材料的磁性比含 的更强,试从结构角度分析原因
的更强,试从结构角度分析原因___________ 。
(6)与Fe、Co、Ni同周期的铜、锌两种元素的第一电离能( ),第二电离能(
),第二电离能( )数据如下表所示:
)数据如下表所示:
请解释铜的 小于锌,
小于锌, 却大于锌的主要原因是
却大于锌的主要原因是___________ 。
(1)中国古代就对磁性材料有研究,四大发明之一的司南是由天然磁石制成的,其主要成分是
a.Fe b.FeO c.
 d.
d.
(2)铁的原子结构示意图为
 。由此可知,铁是第
。由此可知,铁是第(3)钴(Co)元素基态原子的电子排布式为
(4)基态镍(Ni)原子的价电子轨道表示式为
(5)磁性材料原子中的未配对电子对其磁性起主要作用,含
 磁性材料的磁性比含
磁性材料的磁性比含 的更强,试从结构角度分析原因
的更强,试从结构角度分析原因(6)与Fe、Co、Ni同周期的铜、锌两种元素的第一电离能(
 ),第二电离能(
),第二电离能( )数据如下表所示:
)数据如下表所示:电离能/(kJ·mol ) ) |  |  |
| 铜 | 746 | 1958 |
| 锌 | 906 | 1733 |
 小于锌,
小于锌, 却大于锌的主要原因是
却大于锌的主要原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】回答下列问题:
(1)有下列各组物质:A. 和
和 B.
B.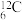 和
和 C.
C. 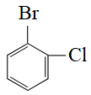 和
和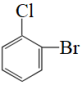 D.甲烷和新戊烷 E.
D.甲烷和新戊烷 E. 和
和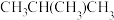 F.
F.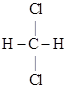 和
和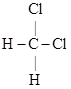 (填字母)
(填字母)
①_______ 组两物质间互为同位素。
②_______ 组两物质间互为同素异形体。
③_______ 组两物质属于同系物。
④_______ 组两物质互为同分异构体。
⑤_______ 组是同一物质。
(2)在下列变化中:①水的汽化、②NaCl熔化、③NaOH溶于水、④ 溶于水、⑤
溶于水、⑤ 溶于水、⑥
溶于水、⑥ 溶于水、⑦
溶于水、⑦ 溶于水。仅破坏离子键的是
溶于水。仅破坏离子键的是_______ (填序号,下同);仅破坏共价键的是_______ ;既破坏离子键又破坏共价键的是_______ 。
(3)写出下列物质的电子式:
_______ ,
_______ 。
(1)有下列各组物质:A.
 和
和 B.
B.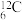 和
和 C.
C.  和
和 D.甲烷和新戊烷 E.
D.甲烷和新戊烷 E. 和
和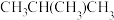 F.
F.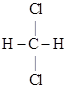 和
和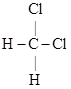 (填字母)
(填字母)①
②
③
④
⑤
(2)在下列变化中:①水的汽化、②NaCl熔化、③NaOH溶于水、④
 溶于水、⑤
溶于水、⑤ 溶于水、⑥
溶于水、⑥ 溶于水、⑦
溶于水、⑦ 溶于水。仅破坏离子键的是
溶于水。仅破坏离子键的是(3)写出下列物质的电子式:


您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】碳、硅、锗等碳族元素的单质及化合物广泛应用于我们生活的各个领域。回答下列问题。
(1)锗(Ge)曾被作为半导体材料,其的原子序数为32,则周期表的位置为__________ 。
(2)和田玉成分是Ca2Mg5H2Si8O24,将其用氧化物的形式表示__________ 。
(3)光导纤维在强碱性条件下容易发生“断路”,用离子方程式解释其原因________ 。
(4)水玻璃的主要成分是____ (化学式),是制备硅胶和木材防火剂的原料。
(5)铅为碳族元素中的一种元素,低价铅相对高价铅更稳定,铅的氧化物Pb3O4的氧化性比MnO2更强,请写出Pb3O4与浓盐酸反应的化学方程式____________ 。
(6)在12C、13C、14C、16O、17O、18O微粒中,共有_____ 种原子,属于________ 种元素;组成CO2分子种类有_______ 种。
(1)锗(Ge)曾被作为半导体材料,其的原子序数为32,则周期表的位置为
(2)和田玉成分是Ca2Mg5H2Si8O24,将其用氧化物的形式表示
(3)光导纤维在强碱性条件下容易发生“断路”,用离子方程式解释其原因
(4)水玻璃的主要成分是
(5)铅为碳族元素中的一种元素,低价铅相对高价铅更稳定,铅的氧化物Pb3O4的氧化性比MnO2更强,请写出Pb3O4与浓盐酸反应的化学方程式
(6)在12C、13C、14C、16O、17O、18O微粒中,共有
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】(1)符号 、
、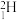 、
、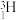 、
、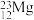 、
、 和
和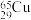 表示的共有
表示的共有______ 种元素,_______ 种原子,中子数最多的粒子是___________ 。
(2)电子表所用的某种钮扣电池的电极材料为Zn和Ag2O,电解质溶液为KOH,其电极反应式为:Zn + 2OH--2e-= ZnO + H2O、Ag2O + H2O + 2e-= 2Ag + 2OH-;电池的负极是______________ (填电极材料),正极发生的是_______________ 反应(填反应类型),总反应式为______________ 。
 、
、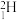 、
、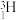 、
、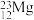 、
、 和
和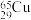 表示的共有
表示的共有(2)电子表所用的某种钮扣电池的电极材料为Zn和Ag2O,电解质溶液为KOH,其电极反应式为:Zn + 2OH--2e-= ZnO + H2O、Ag2O + H2O + 2e-= 2Ag + 2OH-;电池的负极是
您最近一年使用:0次

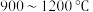 下,在回转炉中重晶石
下,在回转炉中重晶石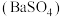 被过量焦炭还原为可溶性硫化钡,该过程的化学方程式为
被过量焦炭还原为可溶性硫化钡,该过程的化学方程式为

