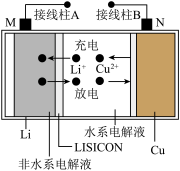
锂海水电池的反应原理为:2Li+2H2O=2LiOH+H2↑,其示意图如图所示。有关该电池工作时说法错误的是
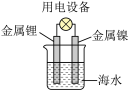

| A.金属锂作正极 |
| B.镍电极上发生还原反应 |
| C.海水作为电解质溶液 |
| D.可将化学能转化为电能 |
更新时间:2019-10-31 10:43:43
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】铝-海水-空气电池在航海中得到广泛的应用,其以海水做为电解液,电池的电极反应式分别为:Al-3eˉ=Al3+,O2 + 2H2O + 4eˉ=4OHˉ,下列说法正确的是( )
| A.该电池的正极是铝,发生氧化反应 |
| B.电池工作时,电子通过外电路从负极流向正极,再从电解质溶液流回负极。 |
| C.该电池的正极反应物是氧气 |
| D.该电池实现了将电能转化为化学能 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】按图甲装置进行实验,若图乙中横坐标X表示通过电极的电子的物质的量。下列叙述不正确的是
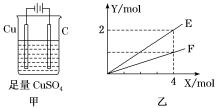

| A.E表示反应消耗H2O的物质的量 |
| B.E表示反应生成H2SO4的物质的量 |
| C.F表示反应生成Cu的物质的量 |
| D.F表示反应生成O2的物质的量 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】近年来一些近海的煤电厂利用海水微碱性(8.0≤pH≤8.3)开发海水脱硫新工艺。主要原理是:工业烟气中的SO2与海水生成H2SO3,H2SO3被进一步氧化成SO 。脱硫后海水酸性增强,与新鲜海水中的CO
。脱硫后海水酸性增强,与新鲜海水中的CO 和HCO
和HCO 反应,最终烟气中的SO2大部分以硫酸盐的形式排入大海。SO2可用于原电池法生产硫酸,其工作原理如图所示。电池工作时,下列说法正确的是
反应,最终烟气中的SO2大部分以硫酸盐的形式排入大海。SO2可用于原电池法生产硫酸,其工作原理如图所示。电池工作时,下列说法正确的是

 。脱硫后海水酸性增强,与新鲜海水中的CO
。脱硫后海水酸性增强,与新鲜海水中的CO 和HCO
和HCO 反应,最终烟气中的SO2大部分以硫酸盐的形式排入大海。SO2可用于原电池法生产硫酸,其工作原理如图所示。电池工作时,下列说法正确的是
反应,最终烟气中的SO2大部分以硫酸盐的形式排入大海。SO2可用于原电池法生产硫酸,其工作原理如图所示。电池工作时,下列说法正确的是
| A.电极b周围溶液pH变小 |
| B.溶液中H+由a极区→b极区 |
C.a极为正极,反应式:SO2-2e-+2H2O=4H++SO |
| D.一段时间后,a极消耗的SO2与b极消耗的O2物质的量相等 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】关于各实验将出现的现象,下列描述错误的是
| A.把铜片和铁片紧靠在一起浸入稀硫酸中,铜片表面将会出现气泡 |
B.用导线连接锌片和铜片,插入 溶液中,铜片质量将增加 溶液中,铜片质量将增加 |
| C.把铜片插入三氯化铁溶液中,在铜片表面将出现一层铁 |
D.Ag和Cu分别作为两电极,用导线连接插入 溶液中,铜将溶解,溶液变成蓝色 溶液中,铜将溶解,溶液变成蓝色 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】某化学兴趣小组为了探究铝电极在电池中的作用,设计并进行了以下一系列实验,实验结果记录如下:
下列回答错误的是
| 编号 | 电极材料 | 电解质溶液 | 电流表指针 |
| 1 | Mg、Al | 稀盐酸 | 偏转 |
| 2 | Al、Cu | 稀盐酸 | 偏转 |
| 3 | Al、C(石墨) | 稀盐酸 | 偏转 |
| 4 | Mg、Al | 氢氧化钠溶液 | 偏转 |
| 5 | Al、Zn | 浓硝酸 | 偏转 |
下列回答错误的是
| A.实验1、2中铝所作的电极(正极或负极)不相同 |
| B.实验2、3,铝电极的电极反应式均为Al-3e-=Al3+ |
| C.实验4中铝电极的电极反应式为Al-3e-+4OH-=[Al(OH)4]- |
| D.实验5中铝始终作原电池的负极 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】下图装置是一种微生物脱盐电池的装置,它可以通过处理有机废水(以含CH3COO-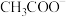 的溶液为例)获得电能,同时还可实现海水淡化。已知a、b电极为惰性电极,X、Y均为离子交换膜,下列说法
的溶液为例)获得电能,同时还可实现海水淡化。已知a、b电极为惰性电极,X、Y均为离子交换膜,下列说法错误 的是
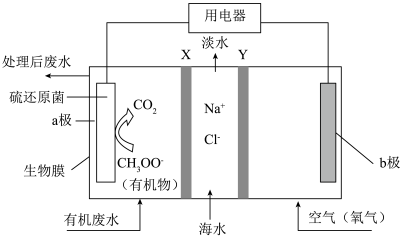
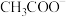 的溶液为例)获得电能,同时还可实现海水淡化。已知a、b电极为惰性电极,X、Y均为离子交换膜,下列说法
的溶液为例)获得电能,同时还可实现海水淡化。已知a、b电极为惰性电极,X、Y均为离子交换膜,下列说法
| A.X、Y依次为阴离子、阳离子选择性交换膜 |
B.a极反应为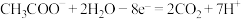 ,产生的H+向b极移动 ,产生的H+向b极移动 |
| C.b极为正极 |
| D.当电路中转移1 mol电子时,在b极室可以生成40 g NaOH |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】热电厂尾气经处理得到较纯的 ,可用于原电池法生产硫酸,其工作原理如图所示。电池工作时,下列说法不正确的是
,可用于原电池法生产硫酸,其工作原理如图所示。电池工作时,下列说法不正确的是

 ,可用于原电池法生产硫酸,其工作原理如图所示。电池工作时,下列说法不正确的是
,可用于原电池法生产硫酸,其工作原理如图所示。电池工作时,下列说法不正确的是
| A.电极b为正极 | B.该装置把电能转化为化学能 |
C.溶液中 由a极区向b极区迁移 由a极区向b极区迁移 | D.电极a的电极反应式: |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】高铁电池的总反应为: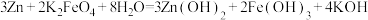 。如图是高铁电池的模拟实验装置,下列说法不正确的是
。如图是高铁电池的模拟实验装置,下列说法不正确的是

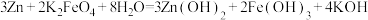 。如图是高铁电池的模拟实验装置,下列说法不正确的是
。如图是高铁电池的模拟实验装置,下列说法不正确的是
A.该电池放电时正极的电极反应式为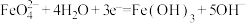 |
B. 被氧化,转移3mol电子 被氧化,转移3mol电子 |
| C.放电过程中负极附近溶液的pH减小 |
| D.盐桥中盛有饱和KCl溶液,此盐桥中氯离子向右移动 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
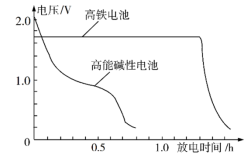
【推荐2】高铁电池是以高铁酸盐(K2FeO4、BaFeO4等)为材料的新型可充电电池,这种电池能量密度大、体积小、重量轻、污染低。这种电池的总反应为:3Zn+2 +8H2O
+8H2O 3Zn(OH)2+2Fe(OH)3+4OH−。下图是高铁电池与普通的高能碱性电池的使用电压对比。下列有关高铁电池的判断不正确的是
3Zn(OH)2+2Fe(OH)3+4OH−。下图是高铁电池与普通的高能碱性电池的使用电压对比。下列有关高铁电池的判断不正确的是
 +8H2O
+8H2O 3Zn(OH)2+2Fe(OH)3+4OH−。下图是高铁电池与普通的高能碱性电池的使用电压对比。下列有关高铁电池的判断不正确的是
3Zn(OH)2+2Fe(OH)3+4OH−。下图是高铁电池与普通的高能碱性电池的使用电压对比。下列有关高铁电池的判断不正确的是
| A.放电过程中正极区域电解液pH升高 |
| B.放电时负极反应式为:Zn+2H2O−2e−=Zn(OH)2+2H+ |
| C.充电时,每转移3 mol电子,则有1 mol Fe(OH)3被氧化 |
| D.高铁电池比高能碱性电池电压稳定,放电时间长 |
您最近一年使用:0次

 作电解质,电极反应:
作电解质,电极反应: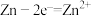 ,
,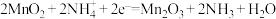 。下列说法
。下列说法 为正极材料
为正极材料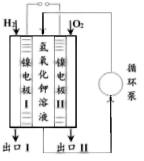
 向镍电极Ⅰ的方向迁移
向镍电极Ⅰ的方向迁移