将8gSO3溶于92g水中,所得溶液中溶质的质量分数为__________ ,每100个水分子中约含H+离子______________ 个。
更新时间:2019-11-03 09:37:55
|
相似题推荐
填空题
|
容易
(0.94)
【推荐1】判断正误
1.物质的量是衡量物质数量的基本物理量。________
2.摩尔是用来描述微观粒子的物理量。________
3.摩尔质量实际上就是相对原子质量。________
4.两种不同粒子的摩尔质量一定不同。________
5.1 mol氧中含有6.02×1023个氧原子。________
6.1 mol任何物质都含有6.02×1023个分子。________
1.物质的量是衡量物质数量的基本物理量。
2.摩尔是用来描述微观粒子的物理量。
3.摩尔质量实际上就是相对原子质量。
4.两种不同粒子的摩尔质量一定不同。
5.1 mol氧中含有6.02×1023个氧原子。
6.1 mol任何物质都含有6.02×1023个分子。
您最近一年使用:0次
填空题
|
容易
(0.94)
【推荐2】(1)含6.02×1022个分子的CO中,n(CO)=_______ 。
(2)2molH2SO4的m(H2SO4)=_______ 。
(3)7gN2在标准状况下的V(N2)=_______ 。
(4)5L2mol·L-1NaOH溶液中所含NaOH的m(NaOH)=_______ 。
(5)将钠用铝箔包好并刺些小孔,再放入水中,请写出有关反应的离子方程式:
①_____ ;
②_____________ 。
(2)2molH2SO4的m(H2SO4)=
(3)7gN2在标准状况下的V(N2)=
(4)5L2mol·L-1NaOH溶液中所含NaOH的m(NaOH)=
(5)将钠用铝箔包好并刺些小孔,再放入水中,请写出有关反应的离子方程式:
①
②
您最近一年使用:0次
填空题
|
容易
(0.94)
【推荐1】(1)含6.02×1022个分子的CO中,n(CO)=_______ 。
(2)2molH2SO4的m(H2SO4)=_______ 。
(3)7gN2在标准状况下的V(N2)=_______ 。
(4)5L2mol·L-1NaOH溶液中所含NaOH的m(NaOH)=_______ 。
(5)将钠用铝箔包好并刺些小孔,再放入水中,请写出有关反应的离子方程式:
①_____ ;
②_____________ 。
(2)2molH2SO4的m(H2SO4)=
(3)7gN2在标准状况下的V(N2)=
(4)5L2mol·L-1NaOH溶液中所含NaOH的m(NaOH)=
(5)将钠用铝箔包好并刺些小孔,再放入水中,请写出有关反应的离子方程式:
①
②
您最近一年使用:0次
填空题
|
容易
(0.94)
【推荐2】判断正误
1.物质的量是衡量物质数量的基本物理量。________
2.摩尔是用来描述微观粒子的物理量。________
3.摩尔质量实际上就是相对原子质量。________
4.两种不同粒子的摩尔质量一定不同。________
5.1 mol氧中含有6.02×1023个氧原子。________
6.1 mol任何物质都含有6.02×1023个分子。________
1.物质的量是衡量物质数量的基本物理量。
2.摩尔是用来描述微观粒子的物理量。
3.摩尔质量实际上就是相对原子质量。
4.两种不同粒子的摩尔质量一定不同。
5.1 mol氧中含有6.02×1023个氧原子。
6.1 mol任何物质都含有6.02×1023个分子。
您最近一年使用:0次
填空题
|
容易
(0.94)
解题方法
【推荐3】某同学为了探究硫与氧气的反应情况,装配好如图所示的装置,待内外空气压强不变时标注出水银液面的刻度(用红漆)。取下橡胶塞,在玻璃燃烧匙中加入硫粉,用酒精灯点燃迅速移入锥形瓶中并塞紧橡胶塞。硫粉安静地燃烧,水银柱推向左管。当火焰熄灭后,静置,水银柱又慢慢地回到原先标定的刻度。简要回答下列问题:
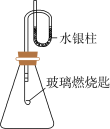
(1)水银柱推向左管是否一定说明生成气体的量一定大于反应气体的量,说明原因:_______ 。
(2)硫粉未燃尽时火焰就熄灭了,说明_______ 。
(3)根据水银柱最后又回到原先标定的刻度,可得到什么结论?_______ 。
(4)根据反应方程式S+O2 SO2和上述结论又可推导(证明)出什么?
SO2和上述结论又可推导(证明)出什么?_______ 。

(1)水银柱推向左管是否一定说明生成气体的量一定大于反应气体的量,说明原因:
(2)硫粉未燃尽时火焰就熄灭了,说明
(3)根据水银柱最后又回到原先标定的刻度,可得到什么结论?
(4)根据反应方程式S+O2
 SO2和上述结论又可推导(证明)出什么?
SO2和上述结论又可推导(证明)出什么?
您最近一年使用:0次
填空题
|
容易
(0.94)
【推荐1】(1)0.5 mol H2O的质量为________ g,其中含有_______ 个水分子,共有____ 个原子。
(2)质量都是50 g的 HCl、NH3、CO2、O2四种气体中,含有分子数目最少的是______ ,在相同温度和相同压强条件下,体积最大的是____ ,体积最小的是______ 。
(3)配制50 mL 0.2 mol/L CuSO4溶液,需要CuSO4____ g;需要CuSO4·5H2O____ g。
(4)中和相同体积、相同物质的量浓度的NaOH溶液,并使其生成正盐,需要相同物质的量浓度的HCl、H2SO4、H3PO4溶液的体积比为_________ 。
(2)质量都是50 g的 HCl、NH3、CO2、O2四种气体中,含有分子数目最少的是
(3)配制50 mL 0.2 mol/L CuSO4溶液,需要CuSO4
(4)中和相同体积、相同物质的量浓度的NaOH溶液,并使其生成正盐,需要相同物质的量浓度的HCl、H2SO4、H3PO4溶液的体积比为
您最近一年使用:0次
填空题
|
容易
(0.94)
解题方法
【推荐2】为确定未知物质的量浓度溶液的浓度,将已知物质的量浓度的溶液与___________ 未知物质的量浓度的溶液反应,根据反应时消耗的___________ ,通过计算确定未知浓度溶液的物质的量浓度。
您最近一年使用:0次
填空题
|
容易
(0.94)
解题方法
【推荐1】现有m g某气体,它由双原子分子构成,它的摩尔质量为M g·mol-1。若阿伏加 德罗常数用NA表示,则:
(1)该气体的物质的量为________ mol
(2)该气体在标准状况下的体积为____________ L。
(3)该气体溶于水后形成VL溶液,其溶质的物质的量浓度为____ mol·L-1。
(1)该气体的物质的量为
(2)该气体在标准状况下的体积为
(3)该气体溶于水后形成VL溶液,其溶质的物质的量浓度为
您最近一年使用:0次
填空题
|
容易
(0.94)
名校
解题方法
【推荐2】在标准状况下,1.5molCO2的体积为________ L;2.5molO2质量为_________ g;将2gNaOH的物质的量为___________ mol,将其溶于水配成100mL溶液,该溶液的浓度为___________ mol/L。
您最近一年使用:0次

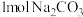 溶于水稀释成1L的溶液相比,
溶于水稀释成1L的溶液相比, 的物质的量浓度是否相等
的物质的量浓度是否相等 气体中:
气体中:  的
的 溶液100mL,取出10mL,
溶液100mL,取出10mL, 的物质的量浓度为
的物质的量浓度为

