在25℃时向VmL pH=m的HNO3中,滴加pH=n的KOH溶液10 V mL时,溶液中NO3-物质的量恰好等于加入的K+的物质的量,则m+n的值为
| A.13 | B.14 | C.15 | D.不能确定 |
更新时间:2016-12-09 02:35:26
|
【知识点】 溶液pH的计算
相似题推荐
单选题
|
较易
(0.85)
【推荐1】25℃时,0.005mol•L﹣1Ba(
OH)
2溶液的pH值为( )
OH)
2溶液的pH值为( )
| A.10 | B.11 | C.12 | D.13 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】常温下,pH=10的X、Y两种碱溶液各1mL,分别加水稀释到100mL,其pH与溶液体积(V)的关系如图所示,下列说法正确的是
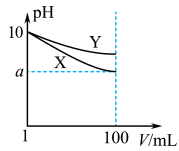

| A.稀释前,两种碱溶液中溶质的物质的量浓度一定相等 |
| B.稀释后,X溶液的碱性比Y溶液的碱性强 |
| C.完全中和X、Y溶液时,消耗同浓度盐酸的体积:VX>VY |
| D.若8<a<10,则X、Y都是弱碱 |
您最近一年使用:0次



