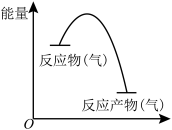
可逆反应NO2(g)+CO(g) CO2(g)+NO(g),反应过程中的能量变化如图所示,下列说法正确的是
CO2(g)+NO(g),反应过程中的能量变化如图所示,下列说法正确的是

 CO2(g)+NO(g),反应过程中的能量变化如图所示,下列说法正确的是
CO2(g)+NO(g),反应过程中的能量变化如图所示,下列说法正确的是
| A.1molNO2与1molCO混合经充分反应放热234kJ |
| B.若反应开始时加入催化剂,则E1、E2都变大 |
| C.加入催化剂,不影响ΔH的大小 |
| D.该反应的反应热ΔH=E2-E1 |
18-19高二·浙江·阶段练习 查看更多[1]
(已下线)【新东方】高中化学5015
更新时间:2019-11-09 20:23:55
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列有关反应热的描述正确的是
①化学反应过程中一定有能量变化
②反应热是1mol物质参加反应时的能量变化
③ΔH的大小与热化学方程式中的化学计量数成正比
④放热反应在常温下就一定能进行⑤化学反应中放出的热才是反应热
①化学反应过程中一定有能量变化
②反应热是1mol物质参加反应时的能量变化
③ΔH的大小与热化学方程式中的化学计量数成正比
④放热反应在常温下就一定能进行⑤化学反应中放出的热才是反应热
| A.①③ | B.②④ | C.①②③ | D.④⑤ |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】化学反应H2+Cl2→2HCl的能量变化如图所示。关于该过程能量变化的叙述不正确的是
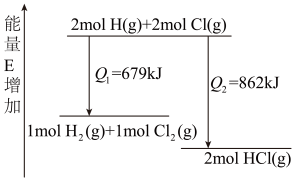

| A.氢气与氯气反应的热化学方程式:H2(g)+Cl2(g)→2HCl(g)+183kJ |
| B.该反应在光照和点燃条件下的反应热效应是相同的 |
| C.2molHCl分子中的化学键形成时要释放862kJ能量 |
| D.2mol气态氢原子的能量低于1mol氢气的能量 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】如图是CH4与Cl2生成CH3Cl的部分反应过程中各物质物质的能量变化关系图(Ea表示活化能),下列说法错误的是


| A.增大Cl2的浓度,可提高反应速率,但不影响ΔH的大小 |
| B.第一步反应的速率小于第二步反应 |
| C.总反应为放热反应 |
| D.升高温度,Ea1、Ea2均增大,反应速率加快 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】 在超临界水中进行碳碳加成反应时存在两条不同的路径,其反应机理如图所示。下列有关说法错误的是
在超临界水中进行碳碳加成反应时存在两条不同的路径,其反应机理如图所示。下列有关说法错误的是
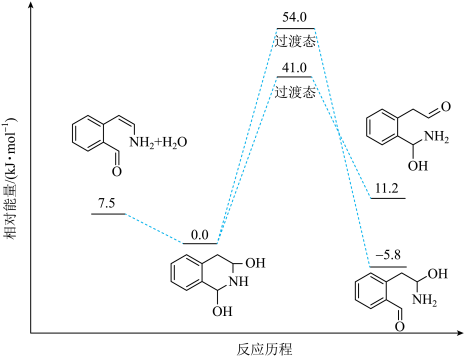
 在超临界水中进行碳碳加成反应时存在两条不同的路径,其反应机理如图所示。下列有关说法错误的是
在超临界水中进行碳碳加成反应时存在两条不同的路径,其反应机理如图所示。下列有关说法错误的是
A. 比 比 稳定 稳定 |
B.反应生成 的活化能为54.0kJ•mol-1 的活化能为54.0kJ•mol-1 |
C.生成 的反应为吸热反应 的反应为吸热反应 |
| D.选择适当的催化剂,有可能改变不同路径产物的产量 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】某密闭容器中发生反应X2(g)+3Y(g) Z(g)+W(g) ΔH,其反应进程和能量的变化如图所示:
Z(g)+W(g) ΔH,其反应进程和能量的变化如图所示:
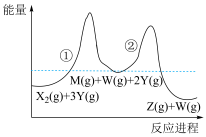
下列有关说法正确的是
 Z(g)+W(g) ΔH,其反应进程和能量的变化如图所示:
Z(g)+W(g) ΔH,其反应进程和能量的变化如图所示:
下列有关说法正确的是
| A.总反应快慢主要由反应②决定 |
| B.总反应的ΔH<0 |
| C.平衡后缩小容器容积,正反应速率增大,逆反应速率减小 |
| D.其他条件不变,加入X2(g),平衡向右移动,X2的平衡转化率增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列有关反应热的描述正确的是
A.稀 与NaOH固体反应生成 与NaOH固体反应生成 放出的热量为中和热 放出的热量为中和热 |
| B.反应条件与反应所需活化能有关,与反应热无关 |
C.若一个反应的反应物总键能大于生成物总键能,则反应 |
D.已知 的燃烧热为 的燃烧热为 ,则完全燃烧 ,则完全燃烧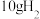 生成水蒸气放出的热量大于 生成水蒸气放出的热量大于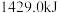 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】某同学设计如图所示实验,探究反应中的能量变化。下列判断正确的是( )




| A.将实验(a)中的铝片更换为等质量的铝粉后释放出的热量有所增加 |
| B.实验(b)反应物的总能量高于生成物的总能量 |
| C.实验(c)铝热反应的反应物总键能小于生成物总键能 |
| D.三个实验中反应的焓变与反应热均相等 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】2SO2(g)+O2(g) 2SO3(g) △H=-198kJ•mol-1。在V2O5存在时该反应机理为:①V2O5+SO2→2VO2+SO3(快);②4VO2+O2→2V2O5(慢)。下列说法不正确的是
2SO3(g) △H=-198kJ•mol-1。在V2O5存在时该反应机理为:①V2O5+SO2→2VO2+SO3(快);②4VO2+O2→2V2O5(慢)。下列说法不正确的是
 2SO3(g) △H=-198kJ•mol-1。在V2O5存在时该反应机理为:①V2O5+SO2→2VO2+SO3(快);②4VO2+O2→2V2O5(慢)。下列说法不正确的是
2SO3(g) △H=-198kJ•mol-1。在V2O5存在时该反应机理为:①V2O5+SO2→2VO2+SO3(快);②4VO2+O2→2V2O5(慢)。下列说法不正确的是| A.基元反应发生的先决条件是反应物分子发生有效碰撞 |
| B.增大SO2的浓度可以显著提高总反应的速率 |
| C.V2O5的存在提高了该反应活化分子百分数,使有效碰撞次数增加,反应速率加快 |
| D.逆反应的活化能比正反应的活化能大198kJ•mol-1 |
您最近一年使用:0次


 在光照和点燃条件下的
在光照和点燃条件下的 不同
不同 ,则正反应活化能大于
,则正反应活化能大于

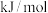 ,则碳的燃烧热为
,则碳的燃烧热为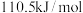
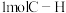 键需要吸收
键需要吸收 能量。无催化剂作用下甲烷在温度达到1200℃以上才可裂解。在催化剂及一定条件下,
能量。无催化剂作用下甲烷在温度达到1200℃以上才可裂解。在催化剂及一定条件下, 可在较低温度下发生裂解反应,甲烷在镍基催化剂上转化过程中的能量变化如图所示。下列说法正确的是
可在较低温度下发生裂解反应,甲烷在镍基催化剂上转化过程中的能量变化如图所示。下列说法正确的是
 甲烷催化裂解成C和
甲烷催化裂解成C和