在铜、锌、稀硫酸构成的原电池中(如图所示)
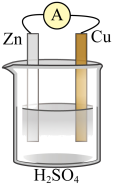
(1)负极是__________ (填“铜”或“锌”),_________ 电子(填“失去”或“得到”),发__________ (填“氧化”或 “还原”),电极反应方程式______________ ;
(2)电流由__________ 流向__________ (填“铜”或“锌),铜片上观察到的现象是________________ 。

(1)负极是
(2)电流由
更新时间:2019-11-28 22:35:20
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】依据氧化还原反应:2Ag+(aq)+Cu(s)=Cu2+(aq)+2Ag(s)设计的原电池如图所示。请回答下列问题:
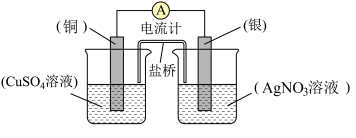
(1)电极铜是原电池的____________ 极(填正或负)。
(2)铜电极上发生的电极反应为___________ ;银电极上发生的电极反应为___________ ;
(3)外电路中的电子是从___________ 电极流向____________ 电极。

(1)电极铜是原电池的
(2)铜电极上发生的电极反应为
(3)外电路中的电子是从
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
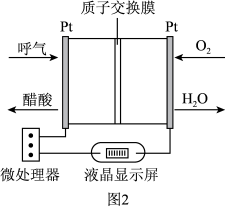
【推荐2】利用反应6NO2+8NH3=7N2+12H2O构成电池的方法,即能实现有效消除氮氧化物的排放,减轻环境污染,又能充分利用化学能,装置如图1所示,回答问题:

(1)电流从_______ (填“左”或“右”)侧电极经过负载后流向另一电极;电极A发生_______ 反应(填“氧化”或“还原”)。
(2)为使电池持续放电,离子交换膜需选用_______ (填“阴”或“阳”)离子交换膜。
(3)A电极上的电极反应式为:_______ 。
(4)当有4.48 L NO2(标准状况)被处理时,转移电子的物质的量为_______ 。
(5)负载可以测定电流大小,从而确定气体含量,酒驾测定工作原理与其相似。仔细阅读图2,写出酒驾测定中电池的总反应式:_______ 。

(1)电流从
(2)为使电池持续放电,离子交换膜需选用
(3)A电极上的电极反应式为:
(4)当有4.48 L NO2(标准状况)被处理时,转移电子的物质的量为
(5)负载可以测定电流大小,从而确定气体含量,酒驾测定工作原理与其相似。仔细阅读图2,写出酒驾测定中电池的总反应式:

您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】某学生利用下面实验装置探究盐桥式原电池的工作原理(Cu:相对原子质量为64)。
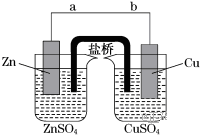
按照实验步骤依次回答下列问题:
(1)导线中电流方向为__________________ (用a、b表示)。
(2)原电池的正极为___________
(3)写出装置中铜电极上的电极反应式:____________________________________ ;
(4)若装置中铜电极的质量增加32 g,则导线中转移的电子数目为________ ;
(5)装置的盐桥中除添加琼脂外,还要添加KCl的饱和溶液,电池工作时,盐桥中的K+向______ (填“左侧”或“右侧”)烧杯移动

按照实验步骤依次回答下列问题:
(1)导线中电流方向为
(2)原电池的正极为
(3)写出装置中铜电极上的电极反应式:
(4)若装置中铜电极的质量增加32 g,则导线中转移的电子数目为
(5)装置的盐桥中除添加琼脂外,还要添加KCl的饱和溶液,电池工作时,盐桥中的K+向
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】Mg-AgCl电池是一种能被海水激活的一次性贮备电池,电池反应方程式为2AgCl+Mg=Mg2++2Ag+2Cl-,试书写该电池的正、负极电极反应式。正极:__________ ;负极:_________ 。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】如图是银锌原电池装置的示意图,以硫酸铜为电解质溶液。回答下列问题:
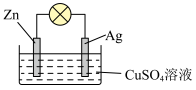
银电极上发生_______ 反应(“氧化”或“还原”),电极反应式为_______ ,该原电池的总反应离子方程式为_______ 。

银电极上发生
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】根据下列要求回答问题。
(1)我国科研人员研制出的可充电“Na-CO2”电池,以钠箔和多壁碳纳米管(MWCNT)为电极材料,总反应方程式为4Na+3CO2 2Na2CO3+C.放电时该电池“吸入”CO2,其工作原理如图所示。
2Na2CO3+C.放电时该电池“吸入”CO2,其工作原理如图所示。
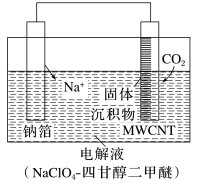
①放电时,正极的电极反应式为___________ 。
②若生成的Na2CO3和C全部沉积在正极表面,当正极增加的质量为28 g时,转移电子的物质的量为___________ 。
③可选用高氯酸钠-四甘醇二甲醚作电解液的理由是___________ 。
(2)用电化学法模拟工业处理SO2。将硫酸工业尾气中的SO2通入如图装置(电极均为惰性材料)进行实验,可用于制备硫酸,同时获得电能。
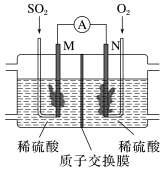
①M极发生的电极反应式为___________ 。
②质子交换膜右侧的溶液在反应后pH___________ (填“增大”“减小”或“不变”)。
③当外电路通过0.2 mol e-时,质子交换膜左侧的溶液质量___________ (填“增大”或“减小”)___________ g。
(1)我国科研人员研制出的可充电“Na-CO2”电池,以钠箔和多壁碳纳米管(MWCNT)为电极材料,总反应方程式为4Na+3CO2
 2Na2CO3+C.放电时该电池“吸入”CO2,其工作原理如图所示。
2Na2CO3+C.放电时该电池“吸入”CO2,其工作原理如图所示。
①放电时,正极的电极反应式为
②若生成的Na2CO3和C全部沉积在正极表面,当正极增加的质量为28 g时,转移电子的物质的量为
③可选用高氯酸钠-四甘醇二甲醚作电解液的理由是
(2)用电化学法模拟工业处理SO2。将硫酸工业尾气中的SO2通入如图装置(电极均为惰性材料)进行实验,可用于制备硫酸,同时获得电能。

①M极发生的电极反应式为
②质子交换膜右侧的溶液在反应后pH
③当外电路通过0.2 mol e-时,质子交换膜左侧的溶液质量
您最近一年使用:0次



