根据下列要求回答问题。
(1)我国科研人员研制出的可充电“Na-CO2”电池,以钠箔和多壁碳纳米管(MWCNT)为电极材料,总反应方程式为4Na+3CO2 2Na2CO3+C.放电时该电池“吸入”CO2,其工作原理如图所示。
2Na2CO3+C.放电时该电池“吸入”CO2,其工作原理如图所示。
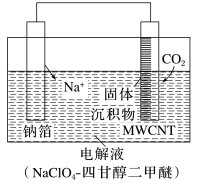
①放电时,正极的电极反应式为___________ 。
②若生成的Na2CO3和C全部沉积在正极表面,当正极增加的质量为28 g时,转移电子的物质的量为___________ 。
③可选用高氯酸钠-四甘醇二甲醚作电解液的理由是___________ 。
(2)用电化学法模拟工业处理SO2。将硫酸工业尾气中的SO2通入如图装置(电极均为惰性材料)进行实验,可用于制备硫酸,同时获得电能。
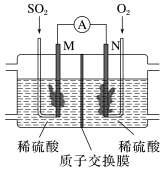
①M极发生的电极反应式为___________ 。
②质子交换膜右侧的溶液在反应后pH___________ (填“增大”“减小”或“不变”)。
③当外电路通过0.2 mol e-时,质子交换膜左侧的溶液质量___________ (填“增大”或“减小”)___________ g。
(1)我国科研人员研制出的可充电“Na-CO2”电池,以钠箔和多壁碳纳米管(MWCNT)为电极材料,总反应方程式为4Na+3CO2
 2Na2CO3+C.放电时该电池“吸入”CO2,其工作原理如图所示。
2Na2CO3+C.放电时该电池“吸入”CO2,其工作原理如图所示。
①放电时,正极的电极反应式为
②若生成的Na2CO3和C全部沉积在正极表面,当正极增加的质量为28 g时,转移电子的物质的量为
③可选用高氯酸钠-四甘醇二甲醚作电解液的理由是
(2)用电化学法模拟工业处理SO2。将硫酸工业尾气中的SO2通入如图装置(电极均为惰性材料)进行实验,可用于制备硫酸,同时获得电能。

①M极发生的电极反应式为
②质子交换膜右侧的溶液在反应后pH
③当外电路通过0.2 mol e-时,质子交换膜左侧的溶液质量
更新时间:2024-01-08 20:26:39
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】如图所示的原电池装置中
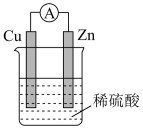
(1)正极的电极反应方程式是_______ 。
(2)该原电池的中反应离子方程式_______ 。

(1)正极的电极反应方程式是
(2)该原电池的中反应离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
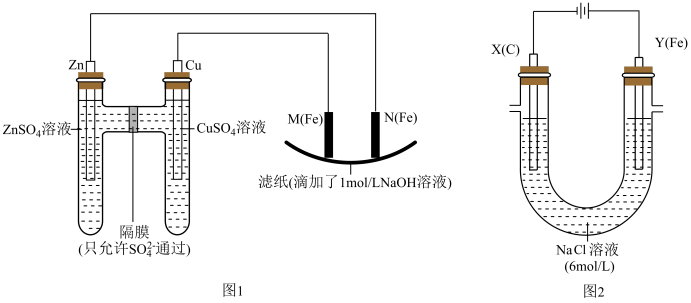
【推荐2】某课外小组分别用下图所示装置对原电池和电解原理进行实验探究。
请回答:
Ⅰ.用图1所示装置进行第一组实验。
(1)在保证电极反应不变的情况下,不能替代Cu做电极的是_________ (填字母序号)。
(2)N极发生反应的电极反应式为____________________ 。
(3)实验过程中,SO42-_________ (填“从左向右”、“从右向左”或“不”)移动;
滤纸上能观察到的现象有___________________ 。
Ⅱ.用图2所示装置进行第二组实验。实验过程中,两极均有气体产生,Y极区溶液逐渐变成紫红色;停止实验,铁电极明显变细,电解液仍然澄清。查阅资料发现,高铁酸根(FeO42-)在溶液中呈紫红色。
(4)电解过程中,X极区溶液的pH___________ (填“增大” 、“减小”或“不变”)。电解过程中,Y极发生的电极反应为Fe-6e-+8OH-=FeO42-+4H2O 和_______________ 。
(5)若在X极收集到672 mL气体,在Y极收集到168 mL气体(均已折算为标准状况时气体体积),则Y电极(铁电极)质量减少________ g。

请回答:
Ⅰ.用图1所示装置进行第一组实验。
(1)在保证电极反应不变的情况下,不能替代Cu做电极的是
| A.铝 | B.石墨 | C.银 | D.铂 |
(2)N极发生反应的电极反应式为
(3)实验过程中,SO42-
滤纸上能观察到的现象有
Ⅱ.用图2所示装置进行第二组实验。实验过程中,两极均有气体产生,Y极区溶液逐渐变成紫红色;停止实验,铁电极明显变细,电解液仍然澄清。查阅资料发现,高铁酸根(FeO42-)在溶液中呈紫红色。
(4)电解过程中,X极区溶液的pH
(5)若在X极收集到672 mL气体,在Y极收集到168 mL气体(均已折算为标准状况时气体体积),则Y电极(铁电极)质量减少
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】回答下列问题:
(1)我国是世界上最早使用湿法炼铜的国家。湿法炼铜的原理是Fe+CuSO4=FeSO4+Cu,其中CuSO4被_______ (填“氧化”或“还原”),铁作_______ (填“氧化剂”或“还原剂”)。在该反应中,若生成了32 g Cu,消耗Fe的物质的量是_______ 。
(2)某学习小组设计下图所示装置观察氧化还原反应中电子的转移。
①实验Ⅰ中,Fe与CuSO4溶液反应的离子方程式是_______ 。
②根据实验Ⅰ的原理,推测实验Ⅱ中:锌片上发生_______ (填“氧化反应”或“还原反应”);铜片上的实验现象是_______ 。
(1)我国是世界上最早使用湿法炼铜的国家。湿法炼铜的原理是Fe+CuSO4=FeSO4+Cu,其中CuSO4被
(2)某学习小组设计下图所示装置观察氧化还原反应中电子的转移。
| 实验I | 实验II | |
| 装置 | 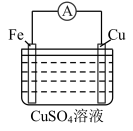 | 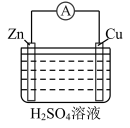 |
| 现象 | 电流计指针向右偏转;铁片溶解;铜片上有红色物质(铜)析出,铜片质量增加 | 电流计指针向右偏转;…… |
②根据实验Ⅰ的原理,推测实验Ⅱ中:锌片上发生
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】以氨气代替氢气研发氨燃料电池是当前科研的一个热点.
(1)氨燃料电池使用的电解质溶液是2mol•L﹣1的KOH溶液,电池反应为:4NH3+3O2=2N2+6H2O.该电池负极的电极反应式为______ ;每消耗1.7g NH3转移的电子数目为______ .
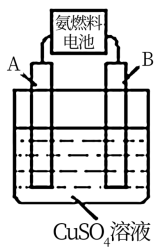
(2)用氨燃料电池电解CuSO4溶液,如图所示,A、B均为铂电极,通电一段时间后,在A电极上有红色固体析出,则B电极上发生的电极反应式为______ ;此时向所得溶液中加入8gCuO固体后恰好可使溶液恢复到电解前的浓度,则电解过程中收集到的气体在标准状况下体积为_______ L.
(3)纳米级氧化亚铜(Cu2O)是一种重要光电材料.现用铜棒和石墨做电极,饱和食盐水做电解质制备纳米级氧化亚铜(Cu2O),电解反应为2Cu+H2O Cu2O+H2↑铜棒上发生的电极反应式为
Cu2O+H2↑铜棒上发生的电极反应式为__ .
(1)氨燃料电池使用的电解质溶液是2mol•L﹣1的KOH溶液,电池反应为:4NH3+3O2=2N2+6H2O.该电池负极的电极反应式为
(2)用氨燃料电池电解CuSO4溶液,如图所示,A、B均为铂电极,通电一段时间后,在A电极上有红色固体析出,则B电极上发生的电极反应式为

(3)纳米级氧化亚铜(Cu2O)是一种重要光电材料.现用铜棒和石墨做电极,饱和食盐水做电解质制备纳米级氧化亚铜(Cu2O),电解反应为2Cu+H2O
 Cu2O+H2↑铜棒上发生的电极反应式为
Cu2O+H2↑铜棒上发生的电极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】某学习小组用利用反应2Fe3++Cu=2Fe2++Cu2+设计原电池,装置如图所示。请回答下列问题。
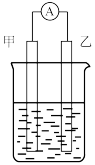
(1)实验过程中观察到电流表指针向右偏转(电流方向),则电极乙所用材料是____ ,电解质溶液是____ ,甲电极上发生的电极反应式是____ ,乙电极上发生的电极反应式是____ 。
(2)电池工作过程中,电解质溶液中的阳离子向____ 极移动(填“甲”或“乙”)。若电池反应过程共转移0.6mole-,则电解质溶液质量变化为____ 。
(3)电流表指针为0时,将乙电极换为铁电极,此时,乙电极为电池的____ 极(填“正”或“负”),电池总反应为____ 。

(1)实验过程中观察到电流表指针向右偏转(电流方向),则电极乙所用材料是
(2)电池工作过程中,电解质溶液中的阳离子向
(3)电流表指针为0时,将乙电极换为铁电极,此时,乙电极为电池的
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】如图是某化学兴趣小组探究不同条件下化学能转变为电能的装置。请回答下列问题:
(1)当电极a为Al,电极b为Cu,电解质溶液为稀硫酸时,正极的电极反应式为:___________ 。
(2)当电极a为Al,电极b为Mg,电解质溶液为氢氧化钠溶液时,该装置______ (填“能”或“不能”)
形成原电池,若不能,请说明理由;若能,请指出正、负极材料:__________ 。当反应中收集到标准状况下224mL气体时,消耗的电极质量为________ g。
(3)燃料电池工作原理是将燃料和氧化剂(如O2)反应产生的化学能直接转化为电能。现设计一燃料电池,以电极a为正极,电极b为负极,甲烷为燃料,采用氢氧化钠溶液为电解液;则甲烷应通入____ 极(填a或b,下同),电子从____ 极流出,电解质溶液中OH-向____ 极移动。
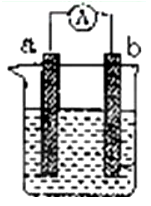
(1)当电极a为Al,电极b为Cu,电解质溶液为稀硫酸时,正极的电极反应式为:
(2)当电极a为Al,电极b为Mg,电解质溶液为氢氧化钠溶液时,该装置
形成原电池,若不能,请说明理由;若能,请指出正、负极材料:
(3)燃料电池工作原理是将燃料和氧化剂(如O2)反应产生的化学能直接转化为电能。现设计一燃料电池,以电极a为正极,电极b为负极,甲烷为燃料,采用氢氧化钠溶液为电解液;则甲烷应通入
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】下表是元素周期表中的一部分。
根据A—J在周期表中的位置,用元素符号、化学式或反应式 回答下列问题:
(1)氧化性最强的单质是___ ,用一个化学反应证明H单质的氧化性强于G单质__________ 。
(2)A分别与F、G、H形成的简单化合物中,稳定性由强到弱的顺序为_________ 。
(3)B、C、G、H离子半径由大到小的顺序是_________ 。
(4)D单质可用来制造D—空气燃料电池,该电池通常以氯化钠或氢氧化钾溶液为电解质溶液,通入空气的电极为正极。若以氯化钠为电解质溶液时,正极的反应式为______ 。若以氢氧化钾溶液为电解质溶液时,电池的总反应式为____ 。
族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 1 | A | |||||||
| 2 | E | F | G | H | J | |||
| 3 | B | C | D | I |
(1)氧化性最强的单质是
(2)A分别与F、G、H形成的简单化合物中,稳定性由强到弱的顺序为
(3)B、C、G、H离子半径由大到小的顺序是
(4)D单质可用来制造D—空气燃料电池,该电池通常以氯化钠或氢氧化钾溶液为电解质溶液,通入空气的电极为正极。若以氯化钠为电解质溶液时,正极的反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】如图所示将锌、铜通过导线相连,置于硫酸溶液中。___________ 能转化为___________ 能。
(2) 电极为
电极为___________ 极,发生___________ (填“氧化”或“还原”)反应,电极方程式为___________ 。
(3)外电路电流由___________ (填“锌”或“铜”,下同)电极经导线流向___________ 电极。
(4)标准状况下,若反应过程中溶解了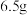 锌,则生成的氢气的体积为
锌,则生成的氢气的体积为___________  。
。

(2)
 电极为
电极为(3)外电路电流由
(4)标准状况下,若反应过程中溶解了
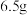 锌,则生成的氢气的体积为
锌,则生成的氢气的体积为 。
。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】(1)将两铂片插入KOH溶液中作为电极,在两极区分别通入甲烷(或氢气、一氧化碳等可燃性气体)和氧气构成燃料电池,则通入甲烷气体的一极是原电池的____ 极,该极的电极反应式是____ ,电池工作时的总反应的离子方程式是_____ 。
(2)熔融盐燃料电池具有高的发电效率,因而受到重视,可用Li2CO3和Na2CO3的熔融盐混合物作电解质,CO为负极气体,空气与CO2的混合气体为正极气体,制得650 ℃下工作的燃料电池,完成下列反应式:
正极:_______ ,
负极:2CO+2CO32--4e-=4CO2。
总反应:______ 。
(3)铅蓄电池放电时,总反应为PbO2+Pb+2H2SO4=2PbSO4+2H2O,由此可以判断:
①原电池的电极材料:负极:__ 。
②电极反应式:正极:PbO2+4H++SO42-+2e-=PbSO4+2H2O,负极反应式为_______ 。
③工作后,铅蓄电池里电解质溶液的pH____ (填“变大”“变小”或“不变”),理由是_____ 。
(2)熔融盐燃料电池具有高的发电效率,因而受到重视,可用Li2CO3和Na2CO3的熔融盐混合物作电解质,CO为负极气体,空气与CO2的混合气体为正极气体,制得650 ℃下工作的燃料电池,完成下列反应式:
正极:
负极:2CO+2CO32--4e-=4CO2。
总反应:
(3)铅蓄电池放电时,总反应为PbO2+Pb+2H2SO4=2PbSO4+2H2O,由此可以判断:
①原电池的电极材料:负极:
②电极反应式:正极:PbO2+4H++SO42-+2e-=PbSO4+2H2O,负极反应式为
③工作后,铅蓄电池里电解质溶液的pH
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】某原电池装置如图所示,装置中盐桥的作用是使整个装置形成一个闭合回路,电解质溶液足量,闭合开关,观察到电流计指针发生偏转,回答下列问题。
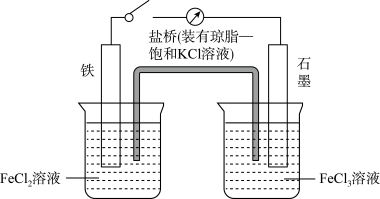
(1)该原电池工作过程中,电池的负极上的电极反应式为___________ ,石墨电极上发生了___________ (填“氧化”或“还原”)反应。
(2)该原电池工作时,下列说法正确的是___________ (填标号)。
a.电子移动的方向: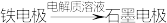
b.盐桥中的 会向右侧烧杯移动
会向右侧烧杯移动
c. 溶液的颜色会逐渐变浅
溶液的颜色会逐渐变浅
d.将 盐桥换成
盐桥换成 盐桥,该装置不能长时间正常工作
盐桥,该装置不能长时间正常工作
(3)当铁电极减少28g时,外电路中转移的电子数目为___________  ;取走盐桥,电流计指针
;取走盐桥,电流计指针___________ (填“会”或“不会”)偏转,原因是___________ 。
(4)原电池工作时能量转化形式为___________,根据原电池形成条件,下列反应理论上可以设计成原电池的是___________(填标号)。

(1)该原电池工作过程中,电池的负极上的电极反应式为
(2)该原电池工作时,下列说法正确的是
a.电子移动的方向:
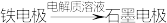
b.盐桥中的
 会向右侧烧杯移动
会向右侧烧杯移动c.
 溶液的颜色会逐渐变浅
溶液的颜色会逐渐变浅d.将
 盐桥换成
盐桥换成 盐桥,该装置不能长时间正常工作
盐桥,该装置不能长时间正常工作(3)当铁电极减少28g时,外电路中转移的电子数目为
 ;取走盐桥,电流计指针
;取走盐桥,电流计指针(4)原电池工作时能量转化形式为___________,根据原电池形成条件,下列反应理论上可以设计成原电池的是___________(填标号)。
A. 与 与 的反应 的反应 | B. 和 和 的反应 的反应 |
C. 和 和 的反应 的反应 | D. 和 和 的反应 的反应 |
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】Li-SOCl2电池采用LiAlCl4的SOCl2溶液为电解质溶液,是目前比能量最高的化学电源,具有电压高.储存寿命长.工作温度范围宽.成本低等优点。
(1)该电池的工作原理为:4Li+2SOCl2=4LiCl↓+SO2↑+S↓,该反应的还原产物为__________ ,若生成标准状况下气体11.2L,则转移电子的数目为_____________ ;
(2)SOCl2可用于AlCl3·6H2O制备无水AlCl3,请结合离子方程式解释不采用直接加热晶体的方法除去结晶水的原因_____________________________________________________________ ;
(3)解释Li-SOCl2电池组装必须在无水条件下的原因_______________________________ ;
(4)工业制硫酸中,SO2的催化氧化采用常压而不是高压的原因______________________ ;
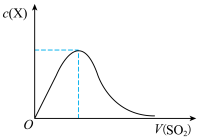
(5)向NaOH溶液中缓慢通入SO2至过量,反应过程中某微粒X的物质的量浓度随着通入SO2体积的变化如图所示,该微粒X为_____________ ,SO2过量时溶液仍然存在微粒X的原因____________________________ 。
(1)该电池的工作原理为:4Li+2SOCl2=4LiCl↓+SO2↑+S↓,该反应的还原产物为
(2)SOCl2可用于AlCl3·6H2O制备无水AlCl3,请结合离子方程式解释不采用直接加热晶体的方法除去结晶水的原因
(3)解释Li-SOCl2电池组装必须在无水条件下的原因
(4)工业制硫酸中,SO2的催化氧化采用常压而不是高压的原因
(5)向NaOH溶液中缓慢通入SO2至过量,反应过程中某微粒X的物质的量浓度随着通入SO2体积的变化如图所示,该微粒X为

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】空军通信卫星电源是以硼氢化合物NaBH4(B元素的化合价为+3价)和H2O2为原料的燃料电池,电极材料均采用Pt,其工作原理如图所示。回答下列问题:

(1)该燃料电池能量转化的主要形式是__ ,外电路中电子的流动方向为___ (填标号)。
①电极a→用电器→电极b;②电极b→用电器→电极a;③电极a→离子交换膜→电极b;④电极b→离子交换膜→电极a。
(2)电极a上的电极反应式为___ 。
(3)图中离子交换膜为___ (填“阴”或“阳”)离子交换膜,电池工作时,Na+往___ (填“电极a”或“电极b”)方向迁移。
(4)每生成0.01molOH-,转移的电子数为__ NA,需要H2O2溶液(质量分数2%)的质量为___ g。
(5)若用LiAlH4代替NaBH4进行上述反应,则该电池的总反应为___ 。

(1)该燃料电池能量转化的主要形式是
①电极a→用电器→电极b;②电极b→用电器→电极a;③电极a→离子交换膜→电极b;④电极b→离子交换膜→电极a。
(2)电极a上的电极反应式为
(3)图中离子交换膜为
(4)每生成0.01molOH-,转移的电子数为
(5)若用LiAlH4代替NaBH4进行上述反应,则该电池的总反应为
您最近一年使用:0次



