按要求准确表达下列变化过程中的化学用语,其中(1)(2)写化学方程式,(3)(4)写离子方程式:
(1)工业制取漂白粉___________________________ 。
(2)呼吸面具(过氧化钠为制氧剂)发生的主要反应_________________ 。
(3)硝酸银溶液中滴入氯化钠溶液_______________________ 。
(4)醋酸和澄清石灰水的反应_____________________ 。
(1)工业制取漂白粉
(2)呼吸面具(过氧化钠为制氧剂)发生的主要反应
(3)硝酸银溶液中滴入氯化钠溶液
(4)醋酸和澄清石灰水的反应
更新时间:2019-12-02 16:41:43
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】写出下列化学方程式的离子方程式
(1)Na2CO3+2HNO3=CO2↑+H2O+2NaNO3_______
(2)Mg(OH)2+2HNO3= Mg(NO3)2+2H2O_______
(3)Cu(NO3)2+2NaOH=Cu(OH)2↓+2NaNO3_______
(4)SO2+2NaOH=Na2SO3+H2O_______
(1)Na2CO3+2HNO3=CO2↑+H2O+2NaNO3
(2)Mg(OH)2+2HNO3= Mg(NO3)2+2H2O
(3)Cu(NO3)2+2NaOH=Cu(OH)2↓+2NaNO3
(4)SO2+2NaOH=Na2SO3+H2O
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】阅读下列科普短文并填空:
海洋的水资源和其他化学资源具有巨大的开发潜力。海水中含有多种盐类,如 、
、 等。目前,通过海水晒盐可制得食盐晶体和苦卤,食盐精制后可制成饱和
等。目前,通过海水晒盐可制得食盐晶体和苦卤,食盐精制后可制成饱和 用以生产
用以生产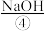 、
、 、
、 、
、 、
、 等。苦卤经过氯气氧化、热空气吹出、
等。苦卤经过氯气氧化、热空气吹出、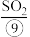 吸收等一操作可获得
吸收等一操作可获得 。电解熔融氯化钠可冶炼
。电解熔融氯化钠可冶炼 。海底埋藏大量可燃冰资源,
。海底埋藏大量可燃冰资源, 是一种清洁能源。
是一种清洁能源。
(1)上述标有序号的物质中属于非电解质的是__________ (填序号)
(2)写出⑤溶于水的电离方程式:___________________ 。将⑧与④混合,写出离子反应方程式_________________ 。将⑤与④的溶液混合,写出离子反应方程式_______________________________ 。
(3)元素G的一种含氧酸化学式为 ,属于二元酸,则
,属于二元酸,则 与过量氢氧化钠溶液反应,生成的正盐的化学式
与过量氢氧化钠溶液反应,生成的正盐的化学式_________________ 。
海洋的水资源和其他化学资源具有巨大的开发潜力。海水中含有多种盐类,如
 、
、 等。目前,通过海水晒盐可制得食盐晶体和苦卤,食盐精制后可制成饱和
等。目前,通过海水晒盐可制得食盐晶体和苦卤,食盐精制后可制成饱和 用以生产
用以生产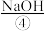 、
、 、
、 、
、 、
、 等。苦卤经过氯气氧化、热空气吹出、
等。苦卤经过氯气氧化、热空气吹出、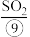 吸收等一操作可获得
吸收等一操作可获得 。电解熔融氯化钠可冶炼
。电解熔融氯化钠可冶炼 。海底埋藏大量可燃冰资源,
。海底埋藏大量可燃冰资源, 是一种清洁能源。
是一种清洁能源。(1)上述标有序号的物质中属于非电解质的是
(2)写出⑤溶于水的电离方程式:
(3)元素G的一种含氧酸化学式为
 ,属于二元酸,则
,属于二元酸,则 与过量氢氧化钠溶液反应,生成的正盐的化学式
与过量氢氧化钠溶液反应,生成的正盐的化学式
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】写出下列反应的方程式
(1)实验室制备氯气的离子方程式___________ 。
(2)工业上制备漂白粉的化学方程式___________ 。
(1)实验室制备氯气的离子方程式
(2)工业上制备漂白粉的化学方程式
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】请填写下列空白。
(1)在常温下,将 通入
通入 溶液中,可以得到一种漂白液。上述反应的离子方程式为
溶液中,可以得到一种漂白液。上述反应的离子方程式为___________ ,该漂白液的有效成分是___________ (填名称)。
(2)检验某溶液中是否含有 的方法是
的方法是________ ,有关反应的离子方程式为_________ 。
(1)在常温下,将
 通入
通入 溶液中,可以得到一种漂白液。上述反应的离子方程式为
溶液中,可以得到一种漂白液。上述反应的离子方程式为(2)检验某溶液中是否含有
 的方法是
的方法是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】现有下列4种物质:①SO2 、②FeCl3溶液、③NaHCO3 、④Na2O2 请回答:
(1)能用于呼吸面具的是_______ (填序号)。
(2)受热分解放出气体的是______ (填序号)。
(3)能用做葡萄酒等食品防腐剂的是______ (填序号)。
(4)用于腐蚀印刷电路板的是______ (填序号)。
(1)能用于呼吸面具的是
(2)受热分解放出气体的是
(3)能用做葡萄酒等食品防腐剂的是
(4)用于腐蚀印刷电路板的是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】“化学——我们的生活,我们的未来”,学习化学应该明白“从生活中来,到生活中去”的道理。请填空:
(1)在呼吸面具和潜水艇中可用过氧化钠作为供氧剂,请写出其中一个反应的化学方程式___________ 。
(2)小苏打的化学式为___________ ,可用于治疗胃酸过多,其反应的离子方程式为___________ 。
(3)氯水和漂白粉都有漂白作用,也可用于水体的杀菌消毒。
①漂白粉有效成分的化学式为___________ ;其能消毒杀菌是因有强___________ 性。
②某同学设计了下图实验装置进一步研究氯气的漂白性,已知通入的氯气中还含有空气和水蒸气。回答下列问题:

浓H2SO4的作用是___________ 。与研究目的直接相关的实验现象是________ 。该实验设计存在事故隐患,应在D处增加一装置,该装置中应加入___________ 溶液以除去多余的氯气。
(1)在呼吸面具和潜水艇中可用过氧化钠作为供氧剂,请写出其中一个反应的化学方程式
(2)小苏打的化学式为
(3)氯水和漂白粉都有漂白作用,也可用于水体的杀菌消毒。
①漂白粉有效成分的化学式为
②某同学设计了下图实验装置进一步研究氯气的漂白性,已知通入的氯气中还含有空气和水蒸气。回答下列问题:

浓H2SO4的作用是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】在鲜活水产品的长途运输中,必须考虑以下几点:①水中需要保持适量的氧气;②及时去除鱼排出的二氧化碳;③防止细菌的大量繁殖。
(1)过氧化物具有杀菌消毒的性质,金属的过氧化物能与水反应产生氧气,现有两种在水中能起供氧灭菌作用的物质:过氧化钠和过氧化钙(CaO2),已知过氧化钙能缓慢与水反应。根据以上介绍,运输鲜活水产品时应选择_______ (填“CaO2”或“Na2O2”)放入水中,理由是_______ 。
(2)写出过氧化钙与水反应的化学方程式_______ 。
(3)一养鱼爱好者欲测定过氧化钙样品中过氧化钙的质量分数,做如下实验:称取样品2.0g,加入到足量的水中,生成0.32g氧气(杂质不产生氧气)。试计算所用样品中过氧化钙的质量分数为____ 。
(1)过氧化物具有杀菌消毒的性质,金属的过氧化物能与水反应产生氧气,现有两种在水中能起供氧灭菌作用的物质:过氧化钠和过氧化钙(CaO2),已知过氧化钙能缓慢与水反应。根据以上介绍,运输鲜活水产品时应选择
(2)写出过氧化钙与水反应的化学方程式
(3)一养鱼爱好者欲测定过氧化钙样品中过氧化钙的质量分数,做如下实验:称取样品2.0g,加入到足量的水中,生成0.32g氧气(杂质不产生氧气)。试计算所用样品中过氧化钙的质量分数为
您最近一年使用:0次



