实验室配制250mL 0.1mol/L的Na2CO3溶液,填空并请回答下列问题:
(1)配制250mL 0.1mol/L的Na2CO3溶液,所需仪器除托盘天平、药匙、烧杯外,还需要____________ 、_______________ 、_________________ 。
(2)配制时,其正确的操作顺序是(用字母表示)______________________ 。
A.每次用30mL水洗涤烧杯2-3次,洗涤液均注入容量瓶,振荡;
B.将冷切的Na2CO3溶液沿玻璃棒注入250mL的容量瓶中
C.称取______ g的Na2CO3固体,置于烧杯中,再加入少量水(约80mL),用玻璃棒慢慢搅动,使其溶解;
D.继续往容量瓶内小心加水,使溶液凹面恰好与刻度相切;
E.将容量瓶盖紧,振荡,摇匀;
(3)若出现如下情况,对所配溶液浓度将有何影响(填“偏高”、“偏低”、或“无影响”)若没有进行A操作___________ ;若容量瓶洗净后没有干燥 ____________ 。
(4)若定容时不小心水加多了,应如何处理?_________________________ 。
(1)配制250mL 0.1mol/L的Na2CO3溶液,所需仪器除托盘天平、药匙、烧杯外,还需要
(2)配制时,其正确的操作顺序是(用字母表示)
A.每次用30mL水洗涤烧杯2-3次,洗涤液均注入容量瓶,振荡;
B.将冷切的Na2CO3溶液沿玻璃棒注入250mL的容量瓶中
C.称取
D.继续往容量瓶内小心加水,使溶液凹面恰好与刻度相切;
E.将容量瓶盖紧,振荡,摇匀;
(3)若出现如下情况,对所配溶液浓度将有何影响(填“偏高”、“偏低”、或“无影响”)若没有进行A操作
(4)若定容时不小心水加多了,应如何处理?
更新时间:2019-11-29 13:22:05
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
【推荐1】Ⅰ.如图所示为常见玻璃仪器的部分结构:
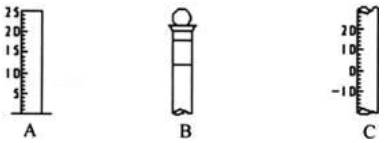
(1)请写出所列仪器的名称: A______ ,B_______ ,C_______ ;
(2)仪器 B 上标记有________ (填序号);
①质量 ②温度 ③刻度线 ④浓度 ⑤容积
(3)仪器 B 使用前必须__________________ 。
II.已知某“84 消毒液”瓶体部分标签如图所示,该“84 消毒液”通常稀释 100 倍(体积之比)后使用。请回答下列问题:
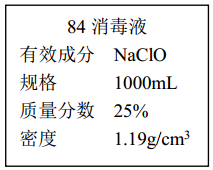
(1)该“84 消毒液”的物质的量浓度约为________ mol·L-1。(保留两位有效数字)
(2)某同学取 100 mL 该“84 消毒液”,稀释后用于消毒,稀释后的溶液中 c(Na+)=________ mol·L-1。
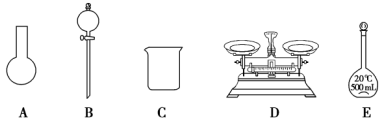
(3)该同学参阅该“84 消毒液”的配方,欲用 NaClO 固体配制 250 mL含 NaClO 质量分数为 25%的消毒液。下列说法不正确的是________ (填序号)。
a.如图所示的仪器中,有三种是不需要的,还需要其它玻璃仪器
b.容量瓶用蒸馏水洗净后,应烘干后才能用于溶液配制
c.配制过程中,未用蒸馏水洗涤烧杯和玻璃棒可能导致结果偏低
(4)“84 消毒液”与稀硫酸混合使用可增强消毒能力,某消毒小组人员用 98%(密度为1.84g·cm-3)的浓硫酸配制2 000 mL 2.3 mol·L-1 的稀硫酸用于增强“84 消毒液”的消毒能力。需用浓硫酸的体积为________ mL。

(1)请写出所列仪器的名称: A
(2)仪器 B 上标记有
①质量 ②温度 ③刻度线 ④浓度 ⑤容积
(3)仪器 B 使用前必须
II.已知某“84 消毒液”瓶体部分标签如图所示,该“84 消毒液”通常稀释 100 倍(体积之比)后使用。请回答下列问题:

(1)该“84 消毒液”的物质的量浓度约为
(2)某同学取 100 mL 该“84 消毒液”,稀释后用于消毒,稀释后的溶液中 c(Na+)=
(3)该同学参阅该“84 消毒液”的配方,欲用 NaClO 固体配制 250 mL含 NaClO 质量分数为 25%的消毒液。下列说法不正确的是
a.如图所示的仪器中,有三种是不需要的,还需要其它玻璃仪器
b.容量瓶用蒸馏水洗净后,应烘干后才能用于溶液配制
c.配制过程中,未用蒸馏水洗涤烧杯和玻璃棒可能导致结果偏低

(4)“84 消毒液”与稀硫酸混合使用可增强消毒能力,某消毒小组人员用 98%(密度为1.84g·cm-3)的浓硫酸配制2 000 mL 2.3 mol·L-1 的稀硫酸用于增强“84 消毒液”的消毒能力。需用浓硫酸的体积为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】T、U、V、W、X、Y、Z是元素周期表中前四周期元素,它们在元素周期表中的位置关系如图所示。
请回答下列问题:
(1)地壳中含量最多的元素在元素周期表中的位置为_______ 。
(2)W2V2与T2V反应的化学方程式为_______ 。
(3)位于Y下一周期的同主族元素的原子序数为_______ 。
(4)Z的原子结构示意图为_______ 。
(5)常温下X的单质能溶于氢氧化钠溶液,写出反应的化学方程式:_______ 。
(6)W与V、Y形成的某种盐常用作杀菌消毒剂,实验室需用480mL0.2mol·L-l该盐溶液配制消毒液。
①该盐为_______ (填化学式)。
②需要用托盘天平称量该盐固体的质量为_______ g;在配制过程中,除托盘天平、烧杯、玻璃棒、胶头滴管外还必需的仪器有_______ 。
③下列情况会导致所配制溶液浓度偏高的是_______ (填标号)。
a.称量时所用的砝码生锈
b.移液时,有少量液体溅出
c.定容时,俯视刻度线
| T | ||||||||
| U | V | |||||||
| W | X | Y | ||||||
| Z | …… |
(1)地壳中含量最多的元素在元素周期表中的位置为
(2)W2V2与T2V反应的化学方程式为
(3)位于Y下一周期的同主族元素的原子序数为
(4)Z的原子结构示意图为
(5)常温下X的单质能溶于氢氧化钠溶液,写出反应的化学方程式:
(6)W与V、Y形成的某种盐常用作杀菌消毒剂,实验室需用480mL0.2mol·L-l该盐溶液配制消毒液。
①该盐为
②需要用托盘天平称量该盐固体的质量为
③下列情况会导致所配制溶液浓度偏高的是
a.称量时所用的砝码生锈
b.移液时,有少量液体溅出
c.定容时,俯视刻度线
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】醋酸和氨水是常用的化学试剂,某研究小组对两种试剂进行了如下实验。
实验一、配制并标定醋酸溶液的浓度
取冰醋酸配制250mL0.2mol·L-1的醋酸溶液,用0.2mol·L-1的醋酸溶液稀释成所需浓度的溶液,再用NaOH标准溶液对所配醋酸溶液的浓度进行标定。回答下列问题:
(1)配制250mL0.2mol·L-1醋酸溶液时需要用到的玻璃仪器有量筒、烧杯、玻璃棒、______ 和______ 。
(2)为标定某醋酸溶液的准确浓度,用0.2000mol·L-1的NaOH溶液对20.00mL醋酸溶液进行滴定,几次滴定消耗NaOH溶液的体积如下:
则该醋酸溶液的准确浓度为______ (保留小数点后四位)。
实验二、探究温度对醋酸电离程度的影响
(3)请你设计一个实验完成该探究,请简述你的实验方案______ 。
(4)氨水中存在电离平衡,用电离常数Kb和电离度α(电离部分占总量的比值)来定量表示其电离程度,它们均可通过各浓度氨水对应的c(OH-)进行换算。下面是该小组在25℃时测定一系列浓度氨水的pH所对应的c(OH-):
【仪器与试剂】酸度计、50mL碱式滴定管、100mL烧杯、0.10mol·L-1氨水
【实验数据】(不必填表格)
根据以上信息回答以下问题:
①表格中x=______ 。
②25℃时,氨水的电离常数Kb≈______ ,通过计算所得所得的数据和简洁文字说明电离度与弱电解质的初始浓度的关系是______ 。
③用0.10mol/L的盐酸分别滴定20.00mL0.10mol·L-1NaOH溶液和20.00mL0.10mol·L-1氨水所得的滴定曲线如图:

请指出盐酸滴定氨水的曲线为______ (填A或B),请写出曲线上a点所对应的溶液中各离子浓度 由大到小的排列顺序______ 。
实验一、配制并标定醋酸溶液的浓度
取冰醋酸配制250mL0.2mol·L-1的醋酸溶液,用0.2mol·L-1的醋酸溶液稀释成所需浓度的溶液,再用NaOH标准溶液对所配醋酸溶液的浓度进行标定。回答下列问题:
(1)配制250mL0.2mol·L-1醋酸溶液时需要用到的玻璃仪器有量筒、烧杯、玻璃棒、
(2)为标定某醋酸溶液的准确浓度,用0.2000mol·L-1的NaOH溶液对20.00mL醋酸溶液进行滴定,几次滴定消耗NaOH溶液的体积如下:
| 实验序号 | 1 | 2 | 3 | 4 |
| 消耗NaOH溶液的体积(mL) | 19.05 | 19.00 | 18.10 | 18.95 |
实验二、探究温度对醋酸电离程度的影响
(3)请你设计一个实验完成该探究,请简述你的实验方案
(4)氨水中存在电离平衡,用电离常数Kb和电离度α(电离部分占总量的比值)来定量表示其电离程度,它们均可通过各浓度氨水对应的c(OH-)进行换算。下面是该小组在25℃时测定一系列浓度氨水的pH所对应的c(OH-):
【仪器与试剂】酸度计、50mL碱式滴定管、100mL烧杯、0.10mol·L-1氨水
【实验数据】(不必填表格)
| 烧杯号 | V氨水(mL) | V水(mL) | c(NH3·H2O)(mol·L-1) | c(OH-) | Kb | α |
| 1 | 50.00 | 0.00 | 1.34×10-3 | |||
| 2 | 25.00 | 25.00 | 9.48×10-4 | |||
| 3 | 5.00 | x | 4.24×10-4 |
①表格中x=
②25℃时,氨水的电离常数Kb≈
③用0.10mol/L的盐酸分别滴定20.00mL0.10mol·L-1NaOH溶液和20.00mL0.10mol·L-1氨水所得的滴定曲线如图:

请指出盐酸滴定氨水的曲线为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】实验室用KMnO4固体配制1000mL0.1 mol·L-1KMnO4溶液。
(1)计算并称量KMnO4固体的质量为_______ g。
(2)下图为甲同学的部分实验操作,其中规范的是_______。
(3)该实验中可做为反应容器的仪器名称是_______ 。
(4)下列情况对所配制的KMnO4溶液度没有影响的是_______。
(5)乙同学用所配制的KMnO4溶液测定人体血液中Ca2+的浓度,步骤如下
a.取1.0mL上述配制的KMnO4溶液稀释为10.0mL;
b.抽取血样10.0mL,使其中的Ca2+ 完全转变为草酸钙(CaC2O4)沉淀,过滤、洗涤后用稀硫酸溶解沉淀得到草酸(H2C2O4)溶液;
c.将稀释后的KMnO4溶液滴加到草酸溶液中,反应恰好消耗2.0mLKMnO4溶液。
已知,KMnO4溶液与草酸的反应为:2KMnO4+5H2C2O4+3H2SO4=2MnSO3+K2SO4+10CO2↑+8H2O
①KMnO4与H2C2O4反应中的氧化剂是_______ 。
②该血样中的Ca2+ 浓度为_______ mol·L-1。
(1)计算并称量KMnO4固体的质量为
(2)下图为甲同学的部分实验操作,其中规范的是_______。
A.称量 | B.转移溶液 | C.溶解 | D.定容 |
(4)下列情况对所配制的KMnO4溶液度没有影响的是_______。
| A.将溶解后的溶液转移至容量瓶之前,容量瓶未干燥 |
| B.将溶解后的溶液转移至容量瓶之后,未洗涤烧杯和玻璃棒 |
| C.定容时,俯视刻度线 |
| D.定容时,发现液面超过刻度线,用吸管将多余的溶液吸出 |
a.取1.0mL上述配制的KMnO4溶液稀释为10.0mL;
b.抽取血样10.0mL,使其中的Ca2+ 完全转变为草酸钙(CaC2O4)沉淀,过滤、洗涤后用稀硫酸溶解沉淀得到草酸(H2C2O4)溶液;
c.将稀释后的KMnO4溶液滴加到草酸溶液中,反应恰好消耗2.0mLKMnO4溶液。
已知,KMnO4溶液与草酸的反应为:2KMnO4+5H2C2O4+3H2SO4=2MnSO3+K2SO4+10CO2↑+8H2O
①KMnO4与H2C2O4反应中的氧化剂是
②该血样中的Ca2+ 浓度为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】某同学欲配制480 mL物质的量浓度为0.1mol·L-1的CuSO4溶液。
(1)完成该实验用到的仪器主要有:托盘天平、胶头滴管、烧杯、玻璃棒、药匙和____________ 。
(2)写出整个实验简单的操作过程:计算→称量→溶解→转移→____________ →定容→摇匀。
(3)如果用CuSO4固体来配制,应该称量固体的质量为_________________ ;如果用CuSO4·5H2O来配制,应该称量固体的质量为____________________ 。
(4)下列操作使配制的溶液浓度偏低的是__________________ 。
A.配制的过程中有少量的液体溅出烧杯。
B.使用前容量瓶用蒸馏水洗涤,且没有干燥。
C.定容时俯视液面。
D.定容摇匀后,液面下降,又加水至刻度线。
(5)取配制好的溶液50 mL用水稀释到100 mL所得溶液中Cu2+的物质的量浓度为_________ 。
(1)完成该实验用到的仪器主要有:托盘天平、胶头滴管、烧杯、玻璃棒、药匙和
(2)写出整个实验简单的操作过程:计算→称量→溶解→转移→
(3)如果用CuSO4固体来配制,应该称量固体的质量为
(4)下列操作使配制的溶液浓度偏低的是
A.配制的过程中有少量的液体溅出烧杯。
B.使用前容量瓶用蒸馏水洗涤,且没有干燥。
C.定容时俯视液面。
D.定容摇匀后,液面下降,又加水至刻度线。
(5)取配制好的溶液50 mL用水稀释到100 mL所得溶液中Cu2+的物质的量浓度为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】某同学通过以下装置测定M样品(只含 、
、 、
、 )中各成分的质量分数。取两份质量均为
)中各成分的质量分数。取两份质量均为 的M样品,按实验1(如图1)和实验2(如图2)进行实验,该同学顺利完成了实验并测得气体体积分别为
的M样品,按实验1(如图1)和实验2(如图2)进行实验,该同学顺利完成了实验并测得气体体积分别为 和
和 (已折算到标准状况下)。
(已折算到标准状况下)。

(1)该实验中所用稀硫酸是用98%的浓硫酸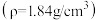 配制的,则该浓硫酸的物质的量浓度是
配制的,则该浓硫酸的物质的量浓度是______  。
。
(2)写出实验1中可能发生反应的离子方程式:____________ 。
(3)对于实验2,平视读数前应依次进行的两种操作是:①______ ,②________ 。
(4)M样品中铜的质量分数的数学表达式为(用 和
和 表示):
表示):___________ 。
(5)该实验需要 的
的 溶液
溶液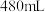 ,请回答下列问题:
,请回答下列问题:
①配制时应称量______ 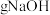 ;
;
②配制 溶液时,
溶液时, 固体中含有
固体中含有 杂质会导致所配溶液浓度
杂质会导致所配溶液浓度______ 。(填“偏大”、“偏小”或“无影响”,下同)。
(6)若拆去实验2中导管a,使测得气体体积______ ;实验1进行实验前,B瓶中水没有装满,使测得气体体积______ 。
 、
、 、
、 )中各成分的质量分数。取两份质量均为
)中各成分的质量分数。取两份质量均为 的M样品,按实验1(如图1)和实验2(如图2)进行实验,该同学顺利完成了实验并测得气体体积分别为
的M样品,按实验1(如图1)和实验2(如图2)进行实验,该同学顺利完成了实验并测得气体体积分别为 和
和 (已折算到标准状况下)。
(已折算到标准状况下)。
(1)该实验中所用稀硫酸是用98%的浓硫酸
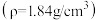 配制的,则该浓硫酸的物质的量浓度是
配制的,则该浓硫酸的物质的量浓度是 。
。(2)写出实验1中可能发生反应的离子方程式:
(3)对于实验2,平视读数前应依次进行的两种操作是:①
(4)M样品中铜的质量分数的数学表达式为(用
 和
和 表示):
表示):(5)该实验需要
 的
的 溶液
溶液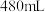 ,请回答下列问题:
,请回答下列问题:①配制时应称量
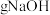 ;
;②配制
 溶液时,
溶液时, 固体中含有
固体中含有 杂质会导致所配溶液浓度
杂质会导致所配溶液浓度(6)若拆去实验2中导管a,使测得气体体积
您最近一年使用:0次



