某2.0L硫酸溶液中含有1.0molH2SO4。试计算:
(1)溶液中H2SO4的物质的量浓度。___________
(2)向上述溶液中加入足量的铁粉,产生气体的体积(标准状况下)。____________
(3)假设反应前后溶液体积不变,则所得溶液中FeSO4的物质的量浓度。____________
(1)溶液中H2SO4的物质的量浓度。
(2)向上述溶液中加入足量的铁粉,产生气体的体积(标准状况下)。
(3)假设反应前后溶液体积不变,则所得溶液中FeSO4的物质的量浓度。
更新时间:2019-12-03 18:38:40
|
【知识点】 化学方程式计算中物质的量的运用解读
相似题推荐
【推荐1】硫能溶解于 形成多硫化钠,
形成多硫化钠,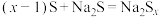 (其中
(其中 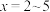 )。
)。
(1)

 溶液中加入0.64g硫粉恰好反应生成多硫化钠(
溶液中加入0.64g硫粉恰好反应生成多硫化钠( ),则
),则
___________ ;
(2)在一定体积和浓度的 溶液中加入1.6g硫粉,控制条件使硫粉完全反应,反应后溶液中阴离子有
溶液中加入1.6g硫粉,控制条件使硫粉完全反应,反应后溶液中阴离子有 、
、 、
、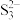 (忽略其它阴离子),且物质的量之比为
(忽略其它阴离子),且物质的量之比为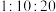 。则反应后溶液中
。则反应后溶液中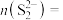
___________  。
。
 形成多硫化钠,
形成多硫化钠,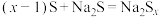 (其中
(其中 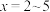 )。
)。(1)


 溶液中加入0.64g硫粉恰好反应生成多硫化钠(
溶液中加入0.64g硫粉恰好反应生成多硫化钠( ),则
),则
(2)在一定体积和浓度的
 溶液中加入1.6g硫粉,控制条件使硫粉完全反应,反应后溶液中阴离子有
溶液中加入1.6g硫粉,控制条件使硫粉完全反应,反应后溶液中阴离子有 、
、 、
、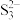 (忽略其它阴离子),且物质的量之比为
(忽略其它阴离子),且物质的量之比为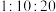 。则反应后溶液中
。则反应后溶液中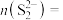
 。
。
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】回答下列问题:
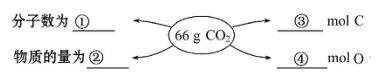
(1)在①②③④处的横线上填写适当的内容。_____________ 、____________ 、____________ 、_________
(2)在质量分数为28%的KOH水溶液中,K+与H2O的数目之比是___________
(3)2 mol O3和3 mol O2的质量之比为_______________
(4)在标准状况下,体积为8.96 L的CO和CO2的混合气体共14.4 g。
①CO的质量为___________ g。
②CO的体积为______________ L。
③在标准状况下,该混合气体中,碳与氧两种原子的数目之比为_____________
(1)在①②③④处的横线上填写适当的内容。

(2)在质量分数为28%的KOH水溶液中,K+与H2O的数目之比是
(3)2 mol O3和3 mol O2的质量之比为
(4)在标准状况下,体积为8.96 L的CO和CO2的混合气体共14.4 g。
①CO的质量为
②CO的体积为
③在标准状况下,该混合气体中,碳与氧两种原子的数目之比为
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐3】“孤蓬自振”学习小组向一定质量的Fe、FeO、Fe2O3的混合物中,加入100mL1.0mol/L的盐酸,恰好使混合物完全溶解并放出约224mL(标准状况)气体,溶液体积仍为100mL,所得溶液中滴加几滴KSCN溶液,溶液未显红色。请回答:
(1)加盐酸后所得溶液的溶质是______ (填化学式),物质的量浓度是______ mol/L。
(2)若用足量的CO在高温下还原相同质量的该混合物,最多能得到单质铁的质量是______ g。
(3)该混合物中铁、氧两种元素的粒子个数比N(Fe):N(O)=______ 。
(1)加盐酸后所得溶液的溶质是
(2)若用足量的CO在高温下还原相同质量的该混合物,最多能得到单质铁的质量是
(3)该混合物中铁、氧两种元素的粒子个数比N(Fe):N(O)=
您最近一年使用:0次



