1g氢气在氧气中燃烧生成液态水,放出142.9kJ的热量,表示该反应的热化学方程式是( )
A.H2(g)+1/2O2(g) H2O(l) ΔH=-285.8kJ·mol-1 H2O(l) ΔH=-285.8kJ·mol-1 |
B.H2(g)+1/2O2(g) H2O(g) ΔH=-285.8kJ·mol-1 H2O(g) ΔH=-285.8kJ·mol-1 |
C.2H2(g)+O2(g) 2H2O(l) ΔH=-285.8kJ·mol-1 2H2O(l) ΔH=-285.8kJ·mol-1 |
D.H2+1/2O2 H2O ΔH=-285.8kJ·mol-1 H2O ΔH=-285.8kJ·mol-1 |
更新时间:2019-12-02 15:54:50
|
相似题推荐
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】强酸与强碱的稀溶液发生中和反应的热效应为:H+(aq)+OH﹣(aq)═H2O(l)△H=﹣57.3kJ•mol﹣1.分别向1L 0.5mol•L﹣1的NaOH溶液中加入①浓硫酸、②稀醋酸、③稀硝酸,恰好完全反应的焓变分别为△H1、△H2、△H3,下列关系正确的是( )
| A.△H2>△H3>△H1 | B.△H1<△H2<△H3 |
| C.△H1>△H2=△H3 | D.△H1=△H2<△H3 |
您最近半年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】已知:25°C,101 kPa时,反应①Mn(s)+ O2(g)=MnO2(s) ΔH1 =-520 kJ·mol-1;反应②Mn(s)+ SO2(g)+ O2(g)=MnSO4(s) ΔH2 =-768 kJ·mol-1,则反应MnO2 (s)+SO2(g)=MnSO4(s)的 ΔH为
| A.-248 kJ·mol-1 | B.+248 kJ·mol-1 |
| C.-1288 kJ·mol-1 | D.+1288 kJ·mol-1 |
您最近半年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】下列说法正确的是
A.已知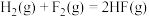 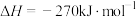 ,则 ,则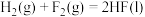  |
B.反应 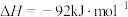 ,当反应放出9.2kJ热量时,转移电子数为 ,当反应放出9.2kJ热量时,转移电子数为 |
C.已知  ,则 ,则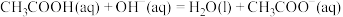  |
D.在101kPa时,氢气的摩尔燃烧焓为 ,则 ,则  |
您最近半年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】当1 g氨气完全分解为氮气、氢气时,吸收2.72 kJ的热量,则下列热化学方程式正确的是( )
①N2(g)+3H2(g)=2NH3(g) ΔH=-92.48 kJ/mol
②N2(g)+3H2(g)=2NH3(g) ΔH=-46.24kJ/mol
③NH3(g)=1/2N2(g)+3/2H2(g) ΔH=+46.24 kJ/mol
④2NH3(g)=N2(g)+3H2(g) ΔH=-92.48 kJ/mol
①N2(g)+3H2(g)=2NH3(g) ΔH=-92.48 kJ/mol
②N2(g)+3H2(g)=2NH3(g) ΔH=-46.24kJ/mol
③NH3(g)=1/2N2(g)+3/2H2(g) ΔH=+46.24 kJ/mol
④2NH3(g)=N2(g)+3H2(g) ΔH=-92.48 kJ/mol
| A.① ③ | B.② ④ | C.② ③ | D.① ④ |
您最近半年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐3】下列热化学方程式书写正确的是( )
| A.在101kPa时,2gH2完全燃烧生成液态水,放出285.8kJ热量,氢气燃烧的热化学方程式表示为:2H2(g)+O2(g)=2H2O(l) ΔH=+285.8kJ·mol-1 |
| B.甲烷的燃烧热为△H=-890kJ·mol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)=CO2(g)+2H2O(l) △H=-890kJ∙mol-1 |
C.500℃、30MPa下,将0.5molN2和1.5molH2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热方程式为:N2(g)+3H2(g)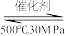 2NH3(g) △H=-38.6kJ∙mol-1 2NH3(g) △H=-38.6kJ∙mol-1 |
D.25℃、101kPa时,强酸与强碱的稀溶液发生中和反应的中和热为57.3kJ·mol-1,则2H+(aq)+SO (aq)+Ba2+(aq)+2OH-(aq)=BaSO4(s)+2H2O(l) ΔH=-114.6kJ·mol-1 (aq)+Ba2+(aq)+2OH-(aq)=BaSO4(s)+2H2O(l) ΔH=-114.6kJ·mol-1 |
您最近半年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】下列热化学方程式正确的是
| A.甲烷的燃烧热为890.3 kJ·mol-1,则甲烷燃烧的热化学方程式可表示为CH4(g)+2O2(g)=CO2(g)+2H2O(g) ΔH=-890.3 kJ·mol-1 |
B.500 ℃、30 MPa下,将0.5 mol N2和1.5 mol H2置于密闭容器中充分反应生成NH3(g),放热19.3 kJ,其热化学方程式为N2(g)+3H2(g)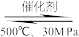 2NH3(g) ΔH=-38.6 kJ·mol-1 2NH3(g) ΔH=-38.6 kJ·mol-1 |
C.已知在25℃、101 kPa下,1 g H2燃烧生成水蒸气放出121 kJ热量,其热化学方程式为H2(g)+ O2(g)=H2O(g) ΔH=-242 kJ·mol-1 O2(g)=H2O(g) ΔH=-242 kJ·mol-1 |
| D.25 ℃,101 kPa时,强酸与强碱的稀溶液发生中和反应的中和热为57.3 kJ·mol-1,表示硫酸溶液与氢氧化钾溶液反应的中和热的热化学方程式为H2SO4(aq)+2KOH(aq)=K2SO4(aq)+2H2O(l) ΔH=-114.6 kJ·mol-1 |
您最近半年使用:0次
单选题
|
较易
(0.85)
【推荐2】下列说法或表示方法中正确的是
| A.等质量的硫蒸气和硫固体分别完全燃烧后都恢复至常温,后者放热量多 |
| B.在101 kPa 时,2 g H2完全燃烧生成液态水,放出285.8kJ热量,氢气燃烧的热化学方程式为:2H2 (g) + O2 (g) = 2H2O (l) ;△H =" +285.8" kJ / mol |
| C.已知中和热为57.3 kJ·mol-1,若将含0.5mol H2SO4的浓溶液与含1molNaOH的溶液混合,放出的热量大于57.3kJ |
| D.Ba(OH)2·8H2O (s) + 2NH4Cl (S) = BaCl2 (s) + 2NH3(g) + 10H2O(l);△H<0 |
您最近半年使用:0次