已知反应2FeCl2+Cl2=2FeCl3。现有铁粉、氯气、氧化铁和盐酸四种物质,试用三种方法制取FeCl3(用化学方程式表示)。
(1)___________________ 。
(2)__________________ 。
(3)_______________ 。
(1)
(2)
(3)
更新时间:2019-12-13 10:42:28
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】与铁三角的转化
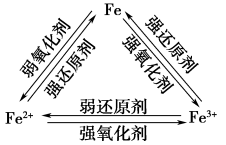

①与I2反应:_______ 。
②与S反应:_______ 。
③与过量稀硝酸反应:_______ 。


①与I2反应:
②与S反应:
③与过量稀硝酸反应:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】从古至今,铁及其化合物在人类的生产生活中都起了巨大的作用。
(1)中国四大发明之一的指南针由天然磁石制成的,其主要成分是___________(填字母)。
(2)将烧至红热的铁丝伸入盛有氯气的集气瓶中,可观察到有棕黄色的烟生成,该反应中被还原的物质是___________ (填化学式)。
(3)实验室用绿矾(FeSO4·7H2O)配制FeSO4溶液时,为防止FeSO4被空气氧化为Fe2(SO4)3,常向其中加入铁粉,写出加入铁粉的离子方程式___________ 。
(4)利用部分变质的FeSO4溶液制备Fe2O3:部分变质的FeSO4溶液 溶液Ⅰ
溶液Ⅰ 沉淀Ⅱ
沉淀Ⅱ Fe2O3;H2O2的作用是把FeSO4氧化为Fe2(SO4)3。
Fe2O3;H2O2的作用是把FeSO4氧化为Fe2(SO4)3。
①写出由“溶液Ⅰ”到“沉淀Ⅱ”反应的离子方程式___________ 。
②“操作Ⅲ”的名称是___________ 。
(1)中国四大发明之一的指南针由天然磁石制成的,其主要成分是___________(填字母)。
| A.Fe | B.FeO | C.Fe3O4 | D.Fe2O3 |
(3)实验室用绿矾(FeSO4·7H2O)配制FeSO4溶液时,为防止FeSO4被空气氧化为Fe2(SO4)3,常向其中加入铁粉,写出加入铁粉的离子方程式
(4)利用部分变质的FeSO4溶液制备Fe2O3:部分变质的FeSO4溶液
 溶液Ⅰ
溶液Ⅰ 沉淀Ⅱ
沉淀Ⅱ Fe2O3;H2O2的作用是把FeSO4氧化为Fe2(SO4)3。
Fe2O3;H2O2的作用是把FeSO4氧化为Fe2(SO4)3。①写出由“溶液Ⅰ”到“沉淀Ⅱ”反应的离子方程式
②“操作Ⅲ”的名称是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】钠、镁、铝、铁是四种重要的金属。请回答:
(1)钠的金属活动性比铝的______ (填“强”或“弱”)。
(2)钠与水反应,观察不到的实验现象是______ (填编号)。
a.钠沉到水底 b.钠熔成小球 c.小球四处游动
(3) 跟S在加热条件下反应,生成物的化学式为
跟S在加热条件下反应,生成物的化学式为______ 。
(4)铁在高温时与水蒸气反应的化学方程式为______ 。
(5)将镁铝合金与过量NaOH溶液反应,所得溶液中不存在的离子是______ 。
A.Na+ B.Mg2+ C.OH- D.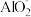
(1)钠的金属活动性比铝的
(2)钠与水反应,观察不到的实验现象是
a.钠沉到水底 b.钠熔成小球 c.小球四处游动
(3)
 跟S在加热条件下反应,生成物的化学式为
跟S在加热条件下反应,生成物的化学式为(4)铁在高温时与水蒸气反应的化学方程式为
(5)将镁铝合金与过量NaOH溶液反应,所得溶液中不存在的离子是
A.Na+ B.Mg2+ C.OH- D.
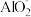
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】工厂烟气(主要污染物NO)直接排放会造成空气污染,需处理后才能排放。“纳米零价铁— ”体系可将烟气中难溶的NO氧化为可溶的
”体系可将烟气中难溶的NO氧化为可溶的 。
。
(1)制备纳米零价铁将 溶液与碱性
溶液与碱性 溶液混合可生成纳米零价铁、
溶液混合可生成纳米零价铁、 和
和 等。
等。
 中
中 电子排布式为
电子排布式为___________ 。
(2)NO的氧化:在一定温度下,将 溶液和HCl溶液雾化后与烟气按一定比例混合,以一定流速通过装有纳米零价铁的反应装置,可将烟气中的NO氧化。
溶液和HCl溶液雾化后与烟气按一定比例混合,以一定流速通过装有纳米零价铁的反应装置,可将烟气中的NO氧化。
①X催化 分解产生HO·,HO·将NO氧化为
分解产生HO·,HO·将NO氧化为 的机理如图所示,则Y的化学式为
的机理如图所示,则Y的化学式为___________ ,纳米零价铁的作用是___________ 。___________ 。
③ 与Y反应可实现X再生,同时产生
与Y反应可实现X再生,同时产生 ,写出
,写出 的电子式
的电子式___________ ,此时 作为
作为___________ 剂。
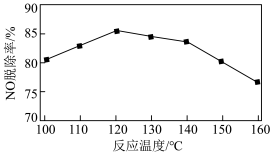
④NO脱除率随温度的变化如下图所示。温度高于120℃时,NO脱除率随温度升高呈现下降趋势的主要原因是___________ 。 表示),可大致分为2个过程,反应原理如下图所示。
表示),可大致分为2个过程,反应原理如下图所示。___________ 。
 ”体系可将烟气中难溶的NO氧化为可溶的
”体系可将烟气中难溶的NO氧化为可溶的 。
。(1)制备纳米零价铁将
 溶液与碱性
溶液与碱性 溶液混合可生成纳米零价铁、
溶液混合可生成纳米零价铁、 和
和 等。
等。 中
中 电子排布式为
电子排布式为(2)NO的氧化:在一定温度下,将
 溶液和HCl溶液雾化后与烟气按一定比例混合,以一定流速通过装有纳米零价铁的反应装置,可将烟气中的NO氧化。
溶液和HCl溶液雾化后与烟气按一定比例混合,以一定流速通过装有纳米零价铁的反应装置,可将烟气中的NO氧化。①X催化
 分解产生HO·,HO·将NO氧化为
分解产生HO·,HO·将NO氧化为 的机理如图所示,则Y的化学式为
的机理如图所示,则Y的化学式为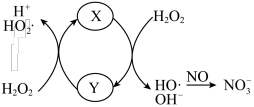
③
 与Y反应可实现X再生,同时产生
与Y反应可实现X再生,同时产生 ,写出
,写出 的电子式
的电子式 作为
作为④NO脱除率随温度的变化如下图所示。温度高于120℃时,NO脱除率随温度升高呈现下降趋势的主要原因是
 表示),可大致分为2个过程,反应原理如下图所示。
表示),可大致分为2个过程,反应原理如下图所示。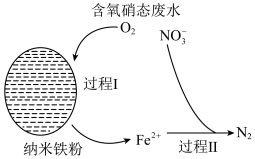
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】铁是人类较早使用的金属之一,铁及其化合物之间的相互转化作用可用下式表示:
Ⅰ.回答下列有关问题:
(1)向沸水中逐滴滴加1mol/LFeCl3溶液,至液体呈透明的红褐色,形成该分散系的微粒大小范围是______ nm。
(2)电子工业需用30%的FeCl3溶液腐蚀敷在绝缘板上的铜,生成FeCl2和CuCl2,制造印刷电路板。写出FeCl3溶液腐蚀铜的化学反应方程式:___________ 。检验反应后溶液中还存在Fe3+的试剂是__________ 。
(3)在下列化学方程式中:2Fe(OH)3+3NaClO+4NaOH=2Na2FeO4+3NaCl+5H2O还原剂是______ 。
Ⅱ.现有五种溶液,分别含下列离子:①Ag+,②Mg2+,③Fe2+,④Al3+,⑤Fe3+。
(4)写出符合下列条件的离子符号:既能被氧化又能被还原的离子是______ ,加铁粉后溶液增重的是 _____________ (填写离子符号)
(5)向Fe2+的溶液中滴加NaOH溶液,现象是___________________ 。
(6)欲除去FeCl2中FeCl3选用的试剂是________ ,并写出相应离子方程式:__________ 。
Ⅰ.回答下列有关问题:
(1)向沸水中逐滴滴加1mol/LFeCl3溶液,至液体呈透明的红褐色,形成该分散系的微粒大小范围是
(2)电子工业需用30%的FeCl3溶液腐蚀敷在绝缘板上的铜,生成FeCl2和CuCl2,制造印刷电路板。写出FeCl3溶液腐蚀铜的化学反应方程式:
(3)在下列化学方程式中:2Fe(OH)3+3NaClO+4NaOH=2Na2FeO4+3NaCl+5H2O还原剂是
Ⅱ.现有五种溶液,分别含下列离子:①Ag+,②Mg2+,③Fe2+,④Al3+,⑤Fe3+。
(4)写出符合下列条件的离子符号:既能被氧化又能被还原的离子是
(5)向Fe2+的溶液中滴加NaOH溶液,现象是
(6)欲除去FeCl2中FeCl3选用的试剂是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】“价类”二维图是学习元素及其化合物的重要工具,如图所示是铁及其化合物的“价类”二维图。
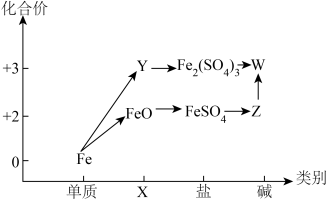
(1)X、Y分别代表_______ 、_______ ;Z在空气中转化为W的化学方程式为_______ 。
(2)某小组研究 性质,预测
性质,预测 能与
能与_______ 发生氧化还原反应(填序号)。
①NaOH溶液②氯水③稀盐酸④酸性 溶液⑤镁⑥碳酸钠
溶液⑤镁⑥碳酸钠
(3)往FeBr2溶液中通入一定量氯气,已知n(FeBr2)∶n(Cl2)=1,写出该反应的离子方程式_______ 。
(4)为检验食品中的铁元素,可将菠菜剪碎、研磨、溶解、_______ ,然后将少许滤液加入试管中,加入少量稀硝酸(稀硝酸具有氧化性),再滴加几滴KSCN溶液,振荡,若观察到_______ 现象,说明试验样品中含有铁元素。
(5)高铁酸钠是一种能杀菌、脱色、除臭的新型高效水处理剂。工业上可用 氧化
氧化 的方法制备
的方法制备 ,其原理为
,其原理为 ,用双线桥法表示该反应的电子转移方向和数目
,用双线桥法表示该反应的电子转移方向和数目_______ 。

(1)X、Y分别代表
(2)某小组研究
 性质,预测
性质,预测 能与
能与①NaOH溶液②氯水③稀盐酸④酸性
 溶液⑤镁⑥碳酸钠
溶液⑤镁⑥碳酸钠(3)往FeBr2溶液中通入一定量氯气,已知n(FeBr2)∶n(Cl2)=1,写出该反应的离子方程式
(4)为检验食品中的铁元素,可将菠菜剪碎、研磨、溶解、
(5)高铁酸钠是一种能杀菌、脱色、除臭的新型高效水处理剂。工业上可用
 氧化
氧化 的方法制备
的方法制备 ,其原理为
,其原理为 ,用双线桥法表示该反应的电子转移方向和数目
,用双线桥法表示该反应的电子转移方向和数目
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】铁及其化合物在生产、生活中存在广泛用途。
(1)基态铁原子电子排布式为___ ,自然界中存在的54Fe和56Fe,它们互称为__ 。
(2)将铁片放入冷浓硫酸中,片刻后将铁片移入硫酸铜溶液中,发现铁片表面无明显变化,原因是___ 。通常证明某溶液中含Fe3+的实验步骤是__ 。
(3)SO2有强还原性,写出其与FeCl3溶液反应的离子方程式___ 。若有0.4molFeCl3发生反应,则需要标准状况下的SO2__ 升。
(4)发黄的深井水通常含Fe3+,若向水中加入Na2CO3溶液,则产生红褐色沉淀和无色无味的气体。写出相应的离子方程式___ 。
(1)基态铁原子电子排布式为
(2)将铁片放入冷浓硫酸中,片刻后将铁片移入硫酸铜溶液中,发现铁片表面无明显变化,原因是
(3)SO2有强还原性,写出其与FeCl3溶液反应的离子方程式
(4)发黄的深井水通常含Fe3+,若向水中加入Na2CO3溶液,则产生红褐色沉淀和无色无味的气体。写出相应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
真题
名校
【推荐2】离子液体是一种室温熔融盐,为非水体系.由有机阳离子、Al2Cl7﹣和AlCl4﹣组成的离子液体做电解液时,可在钢制品上电镀铝.
(1)钢制品应接电源的_______ 极,已知电镀过程中不产生其他离子且有机阳离子不参与电极反应,阴极电极反应式为________________ ,若改用AlCl3水溶液作电解液,则阴极产物为_____________ .
(2)为测定镀层厚度,用NaOH溶液溶解钢制品表面的铝镀层,当反应转移6mol电子时,所得还原产物的物质的量为________ mol.
(3)用铝粉和Fe2O3做铝热反应实验,需要的试剂还有__________
a、KCl b、KClO3 c、MnO2 d、Mg
取少量铝热反应所得的固体混合物,将其溶于足量稀H2SO4,滴加KSCN溶液无明显现象,_______ (填“能”或“不能”)说明固体混合物中无Fe2O3,理由是__________________ (用离子方程式说明).
(1)钢制品应接电源的
(2)为测定镀层厚度,用NaOH溶液溶解钢制品表面的铝镀层,当反应转移6mol电子时,所得还原产物的物质的量为
(3)用铝粉和Fe2O3做铝热反应实验,需要的试剂还有
a、KCl b、KClO3 c、MnO2 d、Mg
取少量铝热反应所得的固体混合物,将其溶于足量稀H2SO4,滴加KSCN溶液无明显现象,
您最近一年使用:0次

 在一定条件下恰好完全反应,将所得产物溶于水配成溶液,分装在二支试管中。请回答:
在一定条件下恰好完全反应,将所得产物溶于水配成溶液,分装在二支试管中。请回答:

