如图所示,某同学设计一个甲醚(CH3OCH3)燃料电池并探究氯碱工业原理和粗铜的精炼原理,其中乙装置中X为阳离子交换膜。
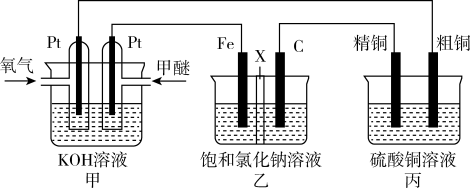
(1)写出负极的电极反应式________________________ 。
(2)石墨电极(C)的电极反应式为___________________ 。
(3)反应一段时间后,乙装置中生成NaOH主要在__________ (填“铁极”或“石墨极”)区。
(4)如果粗铜中含有锌、银等杂质,丙装置中锌先于金属铜放电进入溶液,反应一段时间,硫酸铜溶液浓度将_________ (填“增大”、“减小”或“不变”)
(5)若在标准状况下,有2.24L氧气参加反应,则在乙装置中铁电极上生成的气体在标准状况下的体积为__________________

(1)写出负极的电极反应式
(2)石墨电极(C)的电极反应式为
(3)反应一段时间后,乙装置中生成NaOH主要在
(4)如果粗铜中含有锌、银等杂质,丙装置中锌先于金属铜放电进入溶液,反应一段时间,硫酸铜溶液浓度将
(5)若在标准状况下,有2.24L氧气参加反应,则在乙装置中铁电极上生成的气体在标准状况下的体积为
更新时间:2019-12-13 19:05:46
|
相似题推荐
填空题
|
较难
(0.4)
【推荐1】 是一种高效、安全消毒剂。目前已开发出多种电解法制取
是一种高效、安全消毒剂。目前已开发出多种电解法制取 气体的新工艺,方法一:如图乙,电解精制饱和食盐水制取
气体的新工艺,方法一:如图乙,电解精制饱和食盐水制取 ;方法二:如图丙,电极上通入
;方法二:如图丙,电极上通入 
 酸性溶液中电解
酸性溶液中电解 制取
制取 。某浓差电池的示意图如图丁,该电池既能提供电能,又能产生产生多种化学品。
。某浓差电池的示意图如图丁,该电池既能提供电能,又能产生产生多种化学品。
(1)图甲中,操作Ⅰ、Ⅱ为_______ ,试剂 Ⅱ为_______ (填化学式)
(2)图乙中,电解精制饱和食盐水产生 的电极反应式为
的电极反应式为________ ;电解一段时间,若有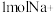 通过离子交换膜,在电极A上产生的气体体积(标准状况)为
通过离子交换膜,在电极A上产生的气体体积(标准状况)为______ L。
(3)图丙中,阴极电极反应式为_______ ;电解一段时间后,阴极区(溶液体积变化忽略不计 溶液的 pH
溶液的 pH______ (填“变大”、“变小”、“不变”)
(4)若以图丁所示电池作图乙的电源,则 a端与______ 相连(填 “e”或 “f”),图乙中阳极的另一产物可不断补充到图丁的正极区,该物质是_______ (填化学式)
(5)工业生产中,还可以用酸性 溶液还原
溶液还原 制得
制得 ,则每生成0.2mol
,则每生成0.2mol ,转移电子的数目为
,转移电子的数目为___________ 。
 是一种高效、安全消毒剂。目前已开发出多种电解法制取
是一种高效、安全消毒剂。目前已开发出多种电解法制取 气体的新工艺,方法一:如图乙,电解精制饱和食盐水制取
气体的新工艺,方法一:如图乙,电解精制饱和食盐水制取 ;方法二:如图丙,电极上通入
;方法二:如图丙,电极上通入 
 酸性溶液中电解
酸性溶液中电解 制取
制取 。某浓差电池的示意图如图丁,该电池既能提供电能,又能产生产生多种化学品。
。某浓差电池的示意图如图丁,该电池既能提供电能,又能产生产生多种化学品。
(1)图甲中,操作Ⅰ、Ⅱ为
(2)图乙中,电解精制饱和食盐水产生
 的电极反应式为
的电极反应式为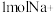 通过离子交换膜,在电极A上产生的气体体积(标准状况)为
通过离子交换膜,在电极A上产生的气体体积(标准状况)为(3)图丙中,阴极电极反应式为
 溶液的 pH
溶液的 pH(4)若以图丁所示电池作图乙的电源,则 a端与
(5)工业生产中,还可以用酸性
 溶液还原
溶液还原 制得
制得 ,则每生成0.2mol
,则每生成0.2mol ,转移电子的数目为
,转移电子的数目为
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐2】回答下列问题
(1)二氧化氯具有杀菌、漂白、除臭、消毒、保鲜的功能。电解法制取 的新工艺如图所示。
的新工艺如图所示。
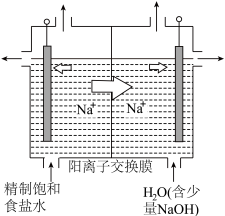
①用石墨作电极,在一定条件下电解饱和食盐水制取 (如图所示),阳极产生
(如图所示),阳极产生 的电极反应式为
的电极反应式为________ 。
②电解一段时间,当阴极产生的气体体积为 (标准状况)时,停止电解,则通过阳离子交换膜的阳离子的物质的量为
(标准状况)时,停止电解,则通过阳离子交换膜的阳离子的物质的量为________  。
。
(2)粗银精炼装置如图所示,电解液为稀硫酸。
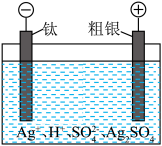
①阳极的电极反应式为________ 。
②下列说法正确的是________ (填字母)。
a.一段时间后,阳极质量减小
b.阴极区可获得银单质的原理:
c.体系中存在沉淀溶解平衡: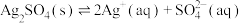
(3)一种用于心脏起搏器的微型电池具有容量大、寿命长和电压稳定等特点。该电池的电极材料是石墨和锂,电解质溶液为等物质的量的 、
、 溶解在
溶解在 中形成的溶液。这种电池的总反应为
中形成的溶液。这种电池的总反应为 。
。
①锂电极的电势比石墨电极的________ (填“低”或“高”)。
②放电时,石墨电极发生________ (填“氧化”或“还原”)反应。
③电池的正极反应为________ 。
(1)二氧化氯具有杀菌、漂白、除臭、消毒、保鲜的功能。电解法制取
 的新工艺如图所示。
的新工艺如图所示。
①用石墨作电极,在一定条件下电解饱和食盐水制取
 (如图所示),阳极产生
(如图所示),阳极产生 的电极反应式为
的电极反应式为②电解一段时间,当阴极产生的气体体积为
 (标准状况)时,停止电解,则通过阳离子交换膜的阳离子的物质的量为
(标准状况)时,停止电解,则通过阳离子交换膜的阳离子的物质的量为 。
。(2)粗银精炼装置如图所示,电解液为稀硫酸。

①阳极的电极反应式为
②下列说法正确的是
a.一段时间后,阳极质量减小
b.阴极区可获得银单质的原理:

c.体系中存在沉淀溶解平衡:
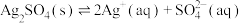
(3)一种用于心脏起搏器的微型电池具有容量大、寿命长和电压稳定等特点。该电池的电极材料是石墨和锂,电解质溶液为等物质的量的
 、
、 溶解在
溶解在 中形成的溶液。这种电池的总反应为
中形成的溶液。这种电池的总反应为 。
。①锂电极的电势比石墨电极的
②放电时,石墨电极发生
③电池的正极反应为
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐3】如图,某同学设计了一个燃料电池并探究氯碱工业的原理和粗铜的精炼原理,其中乙装置中的X为阳离子交换膜。请按要求回答相关问题:

(1)甲烷燃料电池的负极反应为__________________________ 。
(2)石墨(C)极的电极反应为______________________________ 。
(3)若在标准状况下,有2.24 L氧气参加反应,则乙装置中铁电极上生成的气体的体积为________ L。
(4)某同学利用甲烷燃料电池设计电解法制取漂白液的实验装置(如图)。若用于制漂白液,a为电池的______ 极,电解质溶液最好用______________ 。


(1)甲烷燃料电池的负极反应为
(2)石墨(C)极的电极反应为
(3)若在标准状况下,有2.24 L氧气参加反应,则乙装置中铁电极上生成的气体的体积为
(4)某同学利用甲烷燃料电池设计电解法制取漂白液的实验装置(如图)。若用于制漂白液,a为电池的

您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐1】如图1所示,某同学设计了一个燃料电池并探究氯碱工业原理和粗铜的精炼原理,其中乙烧杯中X为阳离子交换膜。请按要求回答相关问题:
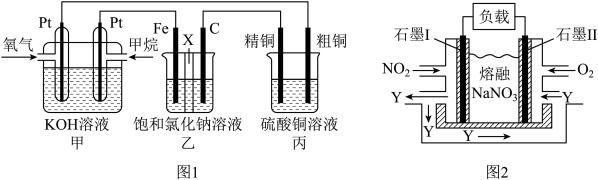
(1)甲烷燃料电池负极电极反应式是___________ ;正极电极反应式是___________________
(2)石墨(C)为__________ 极,其电极反应式为____________________________ ;乙中总反应的离子方程式为__________________________________________________
(3)若在标准状况下,有2.24 L氧气参加反应,则丙装置中阴极析出铜的质量为_________ g ;
(4)若将甲装置中的甲烷换成甲醇(CH3OH),KOH溶液换成稀硫酸,则负极电极反应式为___________ ,消耗等量氧气时,需要甲烷与甲醇的物质的量之比为_________ 。
(5)NO2、O2和熔融NaNO3可制作燃料电池,其原理见图2,该电池在使用过程中石墨I电极上生成氧化物Y,其电极反应式为________________________________

(1)甲烷燃料电池负极电极反应式是
(2)石墨(C)为
(3)若在标准状况下,有2.24 L氧气参加反应,则丙装置中阴极析出铜的质量为
(4)若将甲装置中的甲烷换成甲醇(CH3OH),KOH溶液换成稀硫酸,则负极电极反应式为
(5)NO2、O2和熔融NaNO3可制作燃料电池,其原理见图2,该电池在使用过程中石墨I电极上生成氧化物Y,其电极反应式为
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐2】利用电化学原理,将NO2、O2和熔融KNO3制成燃料电池,模拟工业电解法来处理含 废水,如下图所示;电解过程中溶液发生反应:
废水,如下图所示;电解过程中溶液发生反应: +6Fe2++14H+=2Cr3++6Fe3++7H2O,工作一段时间后,乙池中
+6Fe2++14H+=2Cr3++6Fe3++7H2O,工作一段时间后,乙池中 减少0.1mol。
减少0.1mol。

(1)工作时,甲池内的NO3-向石墨_______ 极移动(填“I”或“II”);在相同条件下,消耗的O2和NO2的体积比为_______ 。
(2)甲池工作时,NO2转变成绿色硝化剂Y,Y是N2O5,可循环使用。则石墨I是电池的_______ 极;石墨I附近发生的电极反应式为_______ 。
(3)丙池中阳极的电极反应式为_______ ,阳极产生气体的体积为_______ L(标况下),若阴极生成气体为6.72L(标况下),则可以加入_______ 复原(填字母序号)。
A.0.3molCu(OH)2 B.0.15molCu2(OH)2CO3 C.0.3molCuO D.0.3molCuCO3
 废水,如下图所示;电解过程中溶液发生反应:
废水,如下图所示;电解过程中溶液发生反应: +6Fe2++14H+=2Cr3++6Fe3++7H2O,工作一段时间后,乙池中
+6Fe2++14H+=2Cr3++6Fe3++7H2O,工作一段时间后,乙池中 减少0.1mol。
减少0.1mol。
(1)工作时,甲池内的NO3-向石墨
(2)甲池工作时,NO2转变成绿色硝化剂Y,Y是N2O5,可循环使用。则石墨I是电池的
(3)丙池中阳极的电极反应式为
A.0.3molCu(OH)2 B.0.15molCu2(OH)2CO3 C.0.3molCuO D.0.3molCuCO3
您最近一年使用:0次
【推荐3】一氧化氮-空气质子交换膜燃料电池将化学能转化为电能,实现了制硝酸、发电环保三位一体的结合。如图所示,某同学设计用该电池探究将雾霾中的SO2、NO转化为(NH4)2SO4的原理和粗铜的精炼原理。
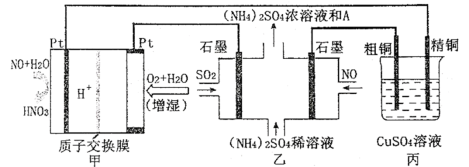
(1)燃料电池放电过程中负极的电极反应式____ 。
(2)乙装置中物质A是____ (填化学式),理由是___ ;电解过程中阳极附近pH___ (填“增大”“减小”或“不变”),阴极的电极反应式是____ 。
(3)如果粗铜中含有锌、银等杂质,丙装置中反应一段时间,CuSO4溶液的浓度将__ (填“增大”、“减小”或“不变”)。
(4)若在标准状况下,甲装置有22.4 L O2参加反应,则乙装置中转化SO2和NO的物质的量共有____ mol;丙装置中阴极析出铜的质量为___ g。

(1)燃料电池放电过程中负极的电极反应式
(2)乙装置中物质A是
(3)如果粗铜中含有锌、银等杂质,丙装置中反应一段时间,CuSO4溶液的浓度将
(4)若在标准状况下,甲装置有22.4 L O2参加反应,则乙装置中转化SO2和NO的物质的量共有
您最近一年使用:0次



