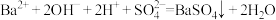关于电解 水溶液,下列叙述正确的是( )
水溶液,下列叙述正确的是( )
 水溶液,下列叙述正确的是( )
水溶液,下列叙述正确的是( )| A.电解时在阳极得到氯气,在阴极得到金属钠 |
| B.若在阳极附近的溶液中滴入浓KI淀粉试液,溶液呈蓝色 |
| C.若在阴极附近的溶液中滴入酚酞试液,溶液仍无色 |
| D.电解一段时间后,将全部电解液转移到烧杯中,加入适量盐酸充分搅拌后溶液可恢复原状况 |
更新时间:2019-12-16 12:02:35
|
相似题推荐
单选题
|
适中
(0.65)
名校
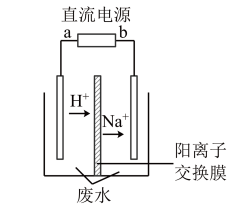
【推荐1】在微生物作用下电解有机废水(含CH3COOH),可获得清洁能源H2,其原理如图所示,下列有关说法不正确的是
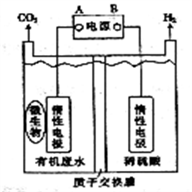
| A.电极B极为负极 |
| B.与电源A极相连的惰性电极上发生的反应为:CH3COOH-8e-+H2O=2CO2↑+8H+ |
| C.通电后,H+通过质子交换膜向右移动,最终右侧溶液PH减小 |
| D.通电后,若有0.1molH2生成,则转移0.2mol电子 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
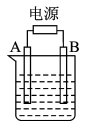
【推荐2】用如图装置实验,下列叙述不正确 的是
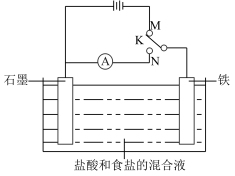

| A.K与N连接时,组成原电池装置 |
| B.K与N连接时,石墨电极产生气泡 |
| C.K与M连接时,一段时间后溶液的pH减小 |
| D.K与M连接时,石墨电极的反应为:2Cl--2e-=Cl2↑ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】如下图所示,下列关于实验现象的描述正确的是( )
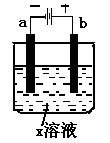

| a电极 | b电极 | x溶液 | 实验现象 | |
| A | 石墨 | 石墨 | CuCl2 | a电极质量增加,b电极放出无色气体 |
| B | Fe | 石墨 | KNO3 | a电极质量增加,b电极放出无色气体 |
| C | Fe | Cu | CuSO4 | a电极质量增加,b电极质量减少 |
| D | 石墨 | 石墨 | HCl | A电极放出无色气体,b电极放出无色气体 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】应用电解法对煤进行脱硫(主要含硫物质为FeS2)处理的原理如图所示,X、Y均为惰性电极。
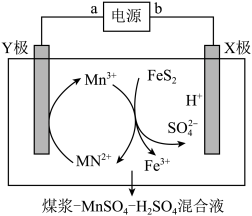
下列说法错误

下列说法错误
| A.b为负极 |
| B.电解初期,X极产生H2 |
| C.脱硫一段时间后混合液的pH增大 |
D.混合液中发生反应FeS2+15Mn3++8H2O=Fe3++2SO +15Mn2++16H+ +15Mn2++16H+ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】如图所示五层膜材料常用于汽车玻璃中的电致变色系统,其工作原理是在外接电源下,通过在膜材料内部发生氧化还原反应,实现对器件的光透过率进行多级可逆性调节。
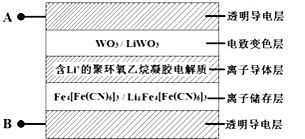
(已知:WO3和Li4Fe4[Fe(CN)6]3均为无色透明,LiWO3和Fe4[Fe(CN)6]3均为蓝色)下列有关说法正确的是

(已知:WO3和Li4Fe4[Fe(CN)6]3均为无色透明,LiWO3和Fe4[Fe(CN)6]3均为蓝色)下列有关说法正确的是
| A.当B外接电源负极时,膜的透射率降低,可以有效阻挡阳光 |
| B.当A接电源的正极时,此时Li+脱离离子存储层 |
| C.当B外接电源正极时,离子储存层发生反应为:Fe4[Fe(CN)6]3+4Li++4eˉ=Li4Fe4[Fe(CN)6]3 |
| D.该电致变色系统在较长时间的使用过程中,离子导体层中Li+的量可保持基本不变 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】将质量分数为5.2%的NaOH溶液1升(密度为1.06克/毫升)用铂电极电解,当溶液中的NaOH的质量分数改变了1.0%时停止电解,则此时溶液中应符合的关系是 ( )
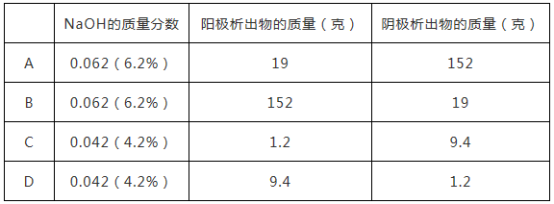

| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】用惰性电极电解硫酸铜溶液一段时间后,向溶液中加入1mol Cu(OH)2后恰好恢复到原来浓度,下列说法不正确的是 ( )
| A.阴极产物是Cu和H2 | B.阳极共产生11.2L的O2 |
| C.电解过程中溶液的pH值不断减小 | D.电解过程中电子转移数目4NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】三室式电渗析法处理含KNO3废水的原理如图所示,电极均为惰性电极,ab、cd均为离子交换膜,在直流电场的作用下,两膜中间的K+和 可通过离子交换膜,而两端隔室中的离子被阻挡不能进入中间隔室。
可通过离子交换膜,而两端隔室中的离子被阻挡不能进入中间隔室。
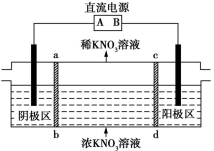
下列叙述正确的是
 可通过离子交换膜,而两端隔室中的离子被阻挡不能进入中间隔室。
可通过离子交换膜,而两端隔室中的离子被阻挡不能进入中间隔室。
下列叙述正确的是
A.通电后中间隔室的 向阳极迁移,阳极区溶液pH增大 向阳极迁移,阳极区溶液pH增大 |
B.A为直流电源负极,阴极反应为2H2O 4e-+O2↑+4H+,阴极区溶液pH减小 4e-+O2↑+4H+,阴极区溶液pH减小 |
C.该电解池的阳极反应为2H2O-4e- 4H++O2↑ 4H++O2↑ |
| D.当电路中通过1 mol电子时,会有0.5 mol O2生成 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】用滴有氯化钠溶液的湿润的滤纸分别做甲、乙两个实验,下列判断正确的是
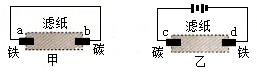

| A.a极上发生还原反应 |
| B.铁片腐蚀速率:乙>甲 |
| C.d为阴极,发生的反应为:Fe-2e→Fe2+ |
| D.b极上发生的反应为:O2 + 2H2O + 4e → 4OH- |
您最近一年使用:0次

 溶液中滴加稀氨水:
溶液中滴加稀氨水: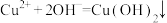
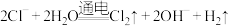
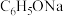 溶液中通入少量
溶液中通入少量 :
:
 和
和 溶液以体积比1∶1混合:
溶液以体积比1∶1混合: