现有三种可溶性物质A、B、C,其中A、B属于盐,C属于碱,它们溶于水后电离产生的所有离子如下表所示:
请根据下列叙述回答问题:
(1)C的化学式为___ 。
(2)A溶液与B溶液反应可生成气体,则该反应的离子方程式为___ 。
(3)A、B溶液与C溶液反应可分别生成白色沉淀D和E,其中D可溶于稀硝酸。
①B的化学式为___ ,鉴别溶液中B的阴离子的试剂为___ 。
②D溶于稀硝酸的离子方程式为___ 。
③D与E的混合物ag,加入足量盐酸,完全反应生成的气体在标准状况下体积为VL,则E在混合物中的质量分数的表达式为___ 。
| 阳离子 | Na+ H+ Ba2+ |
| 阴离子 | OH- CO32- SO42- |
请根据下列叙述回答问题:
(1)C的化学式为
(2)A溶液与B溶液反应可生成气体,则该反应的离子方程式为
(3)A、B溶液与C溶液反应可分别生成白色沉淀D和E,其中D可溶于稀硝酸。
①B的化学式为
②D溶于稀硝酸的离子方程式为
③D与E的混合物ag,加入足量盐酸,完全反应生成的气体在标准状况下体积为VL,则E在混合物中的质量分数的表达式为
更新时间:2019-12-20 08:37:23
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】净水剂能够改善水质,给人们的生活、健康带来很大的益处。
(1)明矾[KAl(SO4)2·12H2O]是常见净水剂。KAl(SO4)2在水中的电离 方程式为___ 。明矾净水是因为在水中生成胶状Al(OH)3,胶状Al(OH)3具有___________ 的作用。
(2)碱式氯化铝[Al2(OH)nCl6﹣n]是高效净水剂,实验室模拟利用铝土矿(主要含有Al2O3,还含少量Fe2O3及其他不溶杂质)制取碱式氯化铝的过程如图:
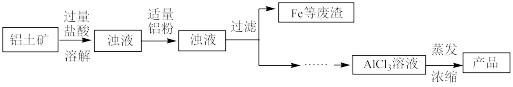
①溶解铝土矿过程中,Al2O3发生反应的离子 方程式为_____ 。溶解过程中需不断搅拌,目的是_____ 。
②已知氧化性:Fe3+ > H+ > Fe2+ > Al3+,加入适量铝粉,目的一是将Fe3+还原为Fe,反应的离子方程式为____ ,为了确保目的一的实现,用文字描述加入适量铝粉的目的二是________ 。
③蒸发浓缩过程中生成Al2(OH)nCl6﹣n固体,请补充且配平其反应的离子 方程式: 2Al3+ + □____ + (6﹣n)Cl﹣=Al2(OH)nCl6﹣n + nH+ 。
④蒸发浓缩所需的玻璃仪器有酒精灯和_____ 。
(1)明矾[KAl(SO4)2·12H2O]是常见净水剂。KAl(SO4)2在水中的
(2)碱式氯化铝[Al2(OH)nCl6﹣n]是高效净水剂,实验室模拟利用铝土矿(主要含有Al2O3,还含少量Fe2O3及其他不溶杂质)制取碱式氯化铝的过程如图:

①溶解铝土矿过程中,Al2O3发生反应的
②已知氧化性:Fe3+ > H+ > Fe2+ > Al3+,加入适量铝粉,目的一是将Fe3+还原为Fe,反应的离子方程式为
③蒸发浓缩过程中生成Al2(OH)nCl6﹣n固体,请补充且配平其反应的
④蒸发浓缩所需的玻璃仪器有酒精灯和
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】“分类研究”是重要的学习与科研方法。现有下列11种物质:①铝,②纯醋酸,③CO2,④Ca(HCO3)2,⑤NaOH,⑥硫酸镁溶液,⑦熔融状态NaC1,⑧NaHSO4,⑨液氯,⑩乙醇,⑪氢氧化铁胶体。
(1)上述物质中属于非电解质的有___________ (填序号);这些物质中能导电的有___________ (填序号)。
(2)④在水中的电离方程式为___________ 。
(3)上述物质中有两种物质在水溶液中发生的反应可用离子反应H++OH-=H2O表示,请写出该离子反应对应的其中一个化学方程式___________ 。
(1)上述物质中属于非电解质的有
(2)④在水中的电离方程式为
(3)上述物质中有两种物质在水溶液中发生的反应可用离子反应H++OH-=H2O表示,请写出该离子反应对应的其中一个化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】多硫化物是含多硫离子(Sx2-)的化合物,可用作废水处理剂、硫化剂等。回答下列问题:
(1)多硫化钠(Na2S5)可由H2S与Na2S在一定条件下反应制得,该反应的还原产物为___________ ,Na2S5中含有的化学键类型是______________________ 。
(2)多硫化物MS4溶液在碱性条件下可高效处理高浓度含CN-电镀废水,CN-被氧化成毒性较小的SCN-,S2-转化为S2-。
①M的离子与S2-具有相同的核外电子排布,则M在周期表中的位置是___________ 。
②CN-的电子式为______________________ 。
③处理废水的离子方程式为______________________ 。
(3)过硫化铵[(NH4)2S2]可用作硫化试剂,为探究其性质,某研究小组进行如下实验:取含1.00g(NH4)2S2的溶液加入足量稀硫酸酸化,得到0.32g淡黄色不溶物A和氢化物B。
①A是___________ ,生成的B在标准状况的体积为___________ mL。
②利用(NN4)2S2溶液中的活性硫能将硫锡矿中的难溶物硫化亚锡(II)(SnS)氧化成硫代锡(IV)酸铵[(NH4)2SnS3]而溶解,写出反应的离子方程式___________ 。
(1)多硫化钠(Na2S5)可由H2S与Na2S在一定条件下反应制得,该反应的还原产物为
(2)多硫化物MS4溶液在碱性条件下可高效处理高浓度含CN-电镀废水,CN-被氧化成毒性较小的SCN-,S2-转化为S2-。
①M的离子与S2-具有相同的核外电子排布,则M在周期表中的位置是
②CN-的电子式为
③处理废水的离子方程式为
(3)过硫化铵[(NH4)2S2]可用作硫化试剂,为探究其性质,某研究小组进行如下实验:取含1.00g(NH4)2S2的溶液加入足量稀硫酸酸化,得到0.32g淡黄色不溶物A和氢化物B。
①A是
②利用(NN4)2S2溶液中的活性硫能将硫锡矿中的难溶物硫化亚锡(II)(SnS)氧化成硫代锡(IV)酸铵[(NH4)2SnS3]而溶解,写出反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】海水提纯精盐的过程是用化学沉淀法去除粗盐中的杂质离子Ca2+、Mg2+和SO ,请完成下题:
,请完成下题:
(1)下面是粗盐提纯的部分操作步骤,请补充③处实验步骤:
①用天平称取5.0g粗盐,放入100ml烧杯中,然后加入20mL蒸馏水,用玻璃棒搅拌,使粗
盐全部溶解,得到粗盐水。
②向粗盐水中滴加过量的BaCl2溶液,使SO 与Ba2+完全反应生成BaSO4将烧杯静置。
与Ba2+完全反应生成BaSO4将烧杯静置。
③_______
④向粗盐水中滴加过量的NaOH溶液,使Mg2+与OH-完全反应生成Mg(OH)2沉淀,然后滴加过量的饱和Na2CO3溶液,使Ca2+、Ba2+与CO 完全反应生成沉淀。
完全反应生成沉淀。
⑤…
(2)有学生设计出如下粗盐提纯工艺流程图
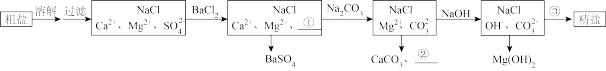
①上述流程图中③处加入的试剂是_______ 。(填名称)
②写出流程中③处发生的离子反应方程式_______ ,_______ 。
(3)方案评价
化学沉淀法中沉淀剂BaCl2和Na2CO3加入的顺序能否交换?_______ 。(填“能”或“否”)
 ,请完成下题:
,请完成下题:(1)下面是粗盐提纯的部分操作步骤,请补充③处实验步骤:
①用天平称取5.0g粗盐,放入100ml烧杯中,然后加入20mL蒸馏水,用玻璃棒搅拌,使粗
盐全部溶解,得到粗盐水。
②向粗盐水中滴加过量的BaCl2溶液,使SO
 与Ba2+完全反应生成BaSO4将烧杯静置。
与Ba2+完全反应生成BaSO4将烧杯静置。③
④向粗盐水中滴加过量的NaOH溶液,使Mg2+与OH-完全反应生成Mg(OH)2沉淀,然后滴加过量的饱和Na2CO3溶液,使Ca2+、Ba2+与CO
 完全反应生成沉淀。
完全反应生成沉淀。⑤…
(2)有学生设计出如下粗盐提纯工艺流程图
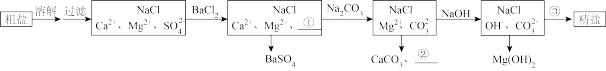
①上述流程图中③处加入的试剂是
②写出流程中③处发生的离子反应方程式
(3)方案评价
化学沉淀法中沉淀剂BaCl2和Na2CO3加入的顺序能否交换?
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】某无色透明溶液中可能大量存在Ba2+、Al3+、Fe3+中的一种或几种。请回答下列问题:
(1)不用做任何实验就可以肯定溶液中不存在的离子是___________
(2)取少量原溶液,加入过量稀硫酸,有白色沉淀生成说明原溶液中肯定存在的离子是___________ ,有关反应的离子方程式为___________
(3)取(2)的滤液加入过量的氨水,出现白色沉淀,说明原溶液中肯定存在的离子是___________ ,生成沉淀的离子方程式为___________ 。
(4)原溶液中可能大量存在的阴离子是___________ (填序号)。
A.Cl- B.NO C.CO
C.CO D.OH-
D.OH-
(1)不用做任何实验就可以肯定溶液中不存在的离子是
(2)取少量原溶液,加入过量稀硫酸,有白色沉淀生成说明原溶液中肯定存在的离子是
(3)取(2)的滤液加入过量的氨水,出现白色沉淀,说明原溶液中肯定存在的离子是
(4)原溶液中可能大量存在的阴离子是
A.Cl- B.NO
 C.CO
C.CO D.OH-
D.OH-
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】有一未知的无色溶液,只可能含有以下离子中的若干种:H+、NH4+、K+、Mg2+、Cu2+、Al3+、NO3-、CO32-、SO42-,现取三份100 mL溶液进行如下实验:
①第一份加入足量AgNO3溶液后,有白色沉淀产生。
②第二份加入足量BaCl2溶液后,有白色沉淀产生,经洗涤、干燥后,沉淀质量为6.99 g。
③第三份逐滴滴加NaOH溶液,测得沉淀与NaOH溶液的体积关系如图所示。

根据上述实验,完成下列问题:
(1)原溶液中一定不存在的离子是______________ 。
(2)25~35段发生反应的离子方程式为__________ 。
(3)35~40段发生反应的离子方程式为__________ 。
(4)实验所加的NaOH的浓度为________ 。
(5)原溶液中NO3-的物质的量为n(NO3-),根据提供的图象和数据,试计算n(NO3-)的取值范围为________ 。
①第一份加入足量AgNO3溶液后,有白色沉淀产生。
②第二份加入足量BaCl2溶液后,有白色沉淀产生,经洗涤、干燥后,沉淀质量为6.99 g。
③第三份逐滴滴加NaOH溶液,测得沉淀与NaOH溶液的体积关系如图所示。

根据上述实验,完成下列问题:
(1)原溶液中一定不存在的离子是
(2)25~35段发生反应的离子方程式为
(3)35~40段发生反应的离子方程式为
(4)实验所加的NaOH的浓度为
(5)原溶液中NO3-的物质的量为n(NO3-),根据提供的图象和数据,试计算n(NO3-)的取值范围为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】某无色待测液中可能含有 、
、 、
、 、
、 、
、 等阳离子。某同学进行如下实验:
等阳离子。某同学进行如下实验:
I.加入过量的稀盐酸,有白色沉淀生成。
II.过滤,取少许滤液,向其中加入过量的稀硫酸,又有白色沉淀生成。
III.另取少量步骤II中的滤液,加入 溶液至溶液呈碱性,加热,可产生使湿润的红色石蕊试纸变蓝色的气体。
溶液至溶液呈碱性,加热,可产生使湿润的红色石蕊试纸变蓝色的气体。
请回答下列问题:
(1)待测液中一定含有的离子是_______ ,一定不含有的离子是_______ 。
(2)还有一种离子不能确定是否存在,检验这种离子的实验时观察到的现象是_______ 。
(3)请你写出“步骤III”中产生气体的离子方程式_______ 。
 、
、 、
、 、
、 、
、 等阳离子。某同学进行如下实验:
等阳离子。某同学进行如下实验:I.加入过量的稀盐酸,有白色沉淀生成。
II.过滤,取少许滤液,向其中加入过量的稀硫酸,又有白色沉淀生成。
III.另取少量步骤II中的滤液,加入
 溶液至溶液呈碱性,加热,可产生使湿润的红色石蕊试纸变蓝色的气体。
溶液至溶液呈碱性,加热,可产生使湿润的红色石蕊试纸变蓝色的气体。请回答下列问题:
(1)待测液中一定含有的离子是
(2)还有一种离子不能确定是否存在,检验这种离子的实验时观察到的现象是
(3)请你写出“步骤III”中产生气体的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】i.某活动小组按如图所示进行实验操作,充分反应后:

(1)I中发生反应的离子方程式为_______ 。
(2)II中铜丝上观察到的现象是_______ 。反应的化学方程式为_______ 。
(3)结合I、II实验现象可知, 、
、 、
、 的还原性顺序为
的还原性顺序为_______ 。
ii.某兴趣小组在课外活动中,对某溶液进行了多次检测,其中三次检测结果如下表所示,请回答:
(4)三次检测结果中第_______ 次检测结果不正确。
(5)在检测时,为了确定溶液中是否存在硫酸根离子、碳酸根离子和氯离子(提示: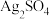 微溶于水),该小组进行了如下操作:
微溶于水),该小组进行了如下操作:
第一步向溶液中滴加过量的_______ (填化学式)溶液,其目的是检验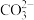 并将其除去;
并将其除去;
第二步加入过量的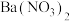 溶液,其目的是
溶液,其目的是_______ ;
第三步过滤,再向滤液中加入_______ (填化学式)溶液,发生反应的离子方程式为_______ 。

(1)I中发生反应的离子方程式为
(2)II中铜丝上观察到的现象是
(3)结合I、II实验现象可知,
 、
、 、
、 的还原性顺序为
的还原性顺序为ii.某兴趣小组在课外活动中,对某溶液进行了多次检测,其中三次检测结果如下表所示,请回答:
| 检测次数 | 溶液中检测出的物质 |
| 第一次 |  、 、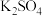 、 、 、 、 |
| 第二次 |  、 、 、 、 、 、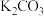 |
| 第三次 |  、 、 、 、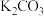 、 、 |
(5)在检测时,为了确定溶液中是否存在硫酸根离子、碳酸根离子和氯离子(提示:
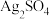 微溶于水),该小组进行了如下操作:
微溶于水),该小组进行了如下操作:第一步向溶液中滴加过量的
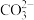 并将其除去;
并将其除去;第二步加入过量的
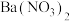 溶液,其目的是
溶液,其目的是第三步过滤,再向滤液中加入
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】对一份稀溶液作初步分析后发现,溶液无色、澄清,其可能含有SO42-、Na+、CO32-、H+、NO3-、HCO3-、Cl-等离子中的若干种。然后又作了如下分析,以确定这些离子是否大量存在。
①用石蕊试液检测该溶液时,溶液显红色。
②取2 mL溶液用BaCl2溶液和稀硝酸进行检验,结果生成了白色沉淀。
③对②中所得的混合物充分静置后,取其上层澄清的液体用AgNO3溶液和稀硝酸进行检验,结果又生成了白色沉淀。
请回答下列问题:
(1)原溶液中一定存在的离子是__________ ,一定不存在的离子是____________ 。
(2)在上述实验操作中,有错误的步骤是(填代号)______ 。对该错误改正的方法是(要作较详细的说明)__________________________________________________ 。
(3)到目前为止,不能肯定在原溶液中是否存在的离子是___________________ 。
①用石蕊试液检测该溶液时,溶液显红色。
②取2 mL溶液用BaCl2溶液和稀硝酸进行检验,结果生成了白色沉淀。
③对②中所得的混合物充分静置后,取其上层澄清的液体用AgNO3溶液和稀硝酸进行检验,结果又生成了白色沉淀。
请回答下列问题:
(1)原溶液中一定存在的离子是
(2)在上述实验操作中,有错误的步骤是(填代号)
(3)到目前为止,不能肯定在原溶液中是否存在的离子是
您最近一年使用:0次



