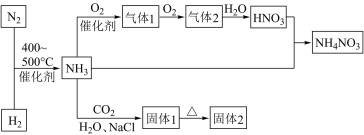
关于下列各图的叙述错误的是

化学方程式 | 平衡常数K |
|
|
|
|
|
|
|
|
A.已知1molCO燃烧放出的热为283kJ,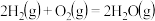 ; ; 则 则 表示CO和 表示CO和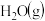 生成 生成 和 和 的能量变化 的能量变化 |
B.常温下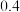  HB溶液和 HB溶液和  溶液等体积混合后溶液的 溶液等体积混合后溶液的 ,则混合溶液中离子浓度的大小顺序为: ,则混合溶液中离子浓度的大小顺序为: |
C.常温下, 和 和 反应生成HX的平衡常数如表所示,仅依据K的变化,就可以说明在相同条件下,平衡时 反应生成HX的平衡常数如表所示,仅依据K的变化,就可以说明在相同条件下,平衡时 从 从 到 到 的转化率逐减小,且HX的还原性逐渐减弱 的转化率逐减小,且HX的还原性逐渐减弱 |
D. 中曲线表示常温下向弱酸HA的稀溶液中加水稀释过程中, 中曲线表示常温下向弱酸HA的稀溶液中加水稀释过程中, 的变化情况 的变化情况 |
2019高三·全国·专题练习 查看更多[3]
2019年秋高三化学复习强化练习—— 盖斯定律及应用夯基提能2020届高三化学选择题对题专练——选修4化学反应原理——弱电解质的电离及影响因素 (强化练习)(已下线)练习2 盖斯定律与化学反应热的计算-2020-2021学年【补习教材·寒假作业】高二化学(人教版2019)
更新时间:2019-12-28 19:19:18
|
相似题推荐
单选题
|
较难
(0.4)
名校
【推荐1】下列说法正确的是
| A.常温下,物质的量浓度均为0.1mol·L−1 Na2CO3和NaHCO3等体积混合后的溶液中:2c(OH-)-2c(H+)=c(H2CO3)+c(HCO3-)-c(CO32-) |
| B.ΔH<0,ΔS>0的反应都是自发反应;ΔH>0,ΔS>0的反应任何条件都是非自发反应 |
| C.电离平衡、水解平衡、难溶电解质的溶解平衡都是动态平衡 |
D.在一定温度下,固定体积为2 L密闭容器中,发生反应:2SO2(g)+O2(g) 2SO3(g) △H<0,当υ(SO2)= υ(SO3)时,说明该反应已达到平衡状态 2SO3(g) △H<0,当υ(SO2)= υ(SO3)时,说明该反应已达到平衡状态 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】已知常温下0.1mol/L NaHSO3溶液pH<7,将10mL 0.1mol/LBa(OH)2溶液缓慢滴加到10mL 0.1mol/L NaHSO3溶液中,下列说法不正确的是( )
| A.滴加过程中,溶液中白色沉淀不断增加 |
| B.常温下0.1 mol/L NaHSO3溶液中HSO3-电离程度大于水解程度 |
| C.当加入Ba(OH)2溶液体积为7.5 mL时,溶液中离子浓度大小为:c(Na+)>c(SO32-)>c(OH-)>c(H+) |
| D.当加入的Ba(OH)2溶液体积小于5 mL时,溶液中的反应为:2HSO3- + Ba2+ + 2OH- = BaSO3↓ + 2H2O + SO32- |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】CO2催化加氢制甲醇有利于减少CO2的排放,实现“碳达峰”,其反应可表示为CO2(g)+3H2(g)=CH3OH(g)+H2O(g) ΔH= -49kJ·mol-1,今年2月我国科研团队在CO2电化学还原反应机理的研究上取得新突破,明确两电子转移CO2电化学还原反应的控速步骤为CO2吸附过程。CO2催化加氢制甲醇的反应通过如下步骤来实现:
①CO2(g)+H2(g)=CO(g)+H2O(g) △H1=41kJ·mol-1
②CO(g)+2H2(g)=CH3OH(g) △H2
反应过程中各物质的相对能量变化情况如图所示。

下列说法不正确的是
①CO2(g)+H2(g)=CO(g)+H2O(g) △H1=41kJ·mol-1
②CO(g)+2H2(g)=CH3OH(g) △H2
反应过程中各物质的相对能量变化情况如图所示。

下列说法不正确的是
| A.步骤①反应的△S>0 |
| B.步骤②反应中形成新共价键的键能之和大于反应中断裂旧共价键的键能之和 |
| C.升高温度,各步骤的正、逆反应速率均增大 |
| D.CO2催化加氢制甲醇的总反应速率由步骤②决定 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】将2 mol  和3 mol
和3 mol  置于密闭容器中,在250℃下只发生如下两个反应:
置于密闭容器中,在250℃下只发生如下两个反应:

 kJ/mol
kJ/mol

 kJ/mol
kJ/mol
一段时间后, 和
和 恰好全部消耗,共放出303 kJ热量。
恰好全部消耗,共放出303 kJ热量。
已知:部分化学键的键能如下表所示
则X的值为
 和3 mol
和3 mol  置于密闭容器中,在250℃下只发生如下两个反应:
置于密闭容器中,在250℃下只发生如下两个反应:
 kJ/mol
kJ/mol
 kJ/mol
kJ/mol一段时间后,
 和
和 恰好全部消耗,共放出303 kJ热量。
恰好全部消耗,共放出303 kJ热量。已知:部分化学键的键能如下表所示
| 化学键 |  |  |  (ClF中) (ClF中) |  ( ( 中) 中) |
| 键能/(kJ/mol) | 157 | 243 | 248 | X |
| A.172 | B.202 | C.238 | D.258 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐3】脱除汽车尾气中的NO和CO包括以下两个反应:
Ⅰ.
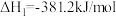
Ⅱ.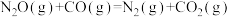
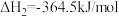
将恒定组成的NO和CO混合气通入不同温度的反应器,相同时间内检测物质浓度,结果如题13图所示。下列说法正确的是
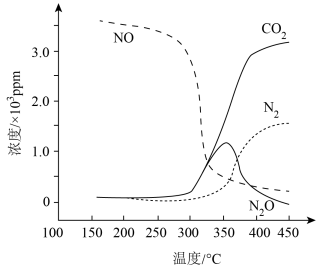
Ⅰ.

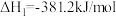
Ⅱ.
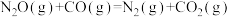
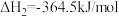
将恒定组成的NO和CO混合气通入不同温度的反应器,相同时间内检测物质浓度,结果如题13图所示。下列说法正确的是

A.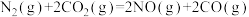 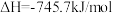 |
| B.使用合适催化剂,能提高NO的平衡转化率 |
| C.其他条件不变,增大体系的压强,NO的平衡转化率增大 |
| D.350℃~420℃范围内,温度升高,反应Ⅰ速率增大的幅度大于反应Ⅱ速率增大的幅度 |
您最近一年使用:0次