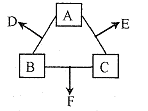
研究氮及其化合物的性质,可以有效改善人类的生存环境。氮元素化合价——物质类别关系图如下。

回答下列问题:
(1)在催化剂和加热的条件下,物质A生成NO是工业制硝酸的重要反应,化学方程式是:__________
(2)在加热条件下,物质C的浓溶液与碳单质反应,写出反应的化学方程式:_______________ ;
(3)实验室中,检验溶液中含有NH4+的操作方法是:__________________________ ;
(4)物质B为红棕色气体,写出该物质与水反应的离子方程式_____________ ,当反应消耗3.36L (标准状况) 物质B时,转移电子的物质的量为__________________________ 。
(5)将32g铜与140 mL一定浓度的C溶液反应,铜完全溶解产生的气体在标准状况下的体积为11.2L。
①参加反应的C的物质的量为__________________________ ;
②待产生的气体全部释放后,向溶液中加入VmLamol·L-1的NaOH溶液,恰好使溶液中的Cu2+全部转化成沉淀,则原C溶液的浓度为________ mol·L-1
③欲使铜与C反应生成的气体在NaOH溶液中全部转化为NaNO3,至少需要通入O2_____ mol。

回答下列问题:
(1)在催化剂和加热的条件下,物质A生成NO是工业制硝酸的重要反应,化学方程式是:
(2)在加热条件下,物质C的浓溶液与碳单质反应,写出反应的化学方程式:
(3)实验室中,检验溶液中含有NH4+的操作方法是:
(4)物质B为红棕色气体,写出该物质与水反应的离子方程式
(5)将32g铜与140 mL一定浓度的C溶液反应,铜完全溶解产生的气体在标准状况下的体积为11.2L。
①参加反应的C的物质的量为
②待产生的气体全部释放后,向溶液中加入VmLamol·L-1的NaOH溶液,恰好使溶液中的Cu2+全部转化成沉淀,则原C溶液的浓度为
③欲使铜与C反应生成的气体在NaOH溶液中全部转化为NaNO3,至少需要通入O2
更新时间:2019-12-27 14:09:17
|
相似题推荐
解答题-实验探究题
|
较难
(0.4)
【推荐1】某研究小组用氯酸钾为原料制备较高纯度的亚氯酸钾(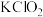 )。按如下流程开展实验:
)。按如下流程开展实验:

已知:①装置A反应需控制温度60℃左右,当试剂X为 和少量
和少量 时,在酸性情况下,氯离子是会先和氯酸根发生化学反应,进而生成二氧化氯和氯气:
时,在酸性情况下,氯离子是会先和氯酸根发生化学反应,进而生成二氧化氯和氯气:
生成物中氯气可以和过氧化氢快速反应生成氯离子:
② 在强碱性条件下易分解;
在强碱性条件下易分解; 气体在温度过高,浓度过大时易分解,在碱性条件下则会发生歧化反应。
气体在温度过高,浓度过大时易分解,在碱性条件下则会发生歧化反应。
(1)装置C的名称是______________ ,装置A中加入少量 的作用
的作用______________ 。
(2)下列说法不正确 的是_____。
(3)装置B内的吸收液:氢氧化钾与过氧化氢的混合液。配置两者浓度,比例需恰当,理由是______________ 。
(4)取装置A中反应后母液1L蒸发至500 后,过滤,滤液可循环利用,过滤得到的晶体可进行回收利用制备硫酸氢钾,流程如图所示。
后,过滤,滤液可循环利用,过滤得到的晶体可进行回收利用制备硫酸氢钾,流程如图所示。

反应母液的主要成分表
蒸发浓缩至500 ,冷却至室温测得
,冷却至室温测得 浓度为0.2
浓度为0.2 。蒸发过程中,滤液中其他离子浓度变化如下图所示。
。蒸发过程中,滤液中其他离子浓度变化如下图所示。

根据以上数据分析,过滤获得的晶体的成分的化学式______________ ,要制备硫酸氢钾,需加入试剂X为______________ 。
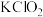 )。按如下流程开展实验:
)。按如下流程开展实验:
已知:①装置A反应需控制温度60℃左右,当试剂X为
 和少量
和少量 时,在酸性情况下,氯离子是会先和氯酸根发生化学反应,进而生成二氧化氯和氯气:
时,在酸性情况下,氯离子是会先和氯酸根发生化学反应,进而生成二氧化氯和氯气:
生成物中氯气可以和过氧化氢快速反应生成氯离子:

②
 在强碱性条件下易分解;
在强碱性条件下易分解; 气体在温度过高,浓度过大时易分解,在碱性条件下则会发生歧化反应。
气体在温度过高,浓度过大时易分解,在碱性条件下则会发生歧化反应。(1)装置C的名称是
 的作用
的作用(2)下列说法
| A.装置A采用水浴加热控制温度,既可加速反应又能防止温度太高引起双氧水大量分解 |
B.若试剂X中 或 或 单独使用,从最终获得亚氯酸钾的纯度来看应选择 单独使用,从最终获得亚氯酸钾的纯度来看应选择 |
| C.装置B中双氧水作氧化剂,但需要加入稳定剂,同时用冰水浴来抑制过氧化氢的分解 |
D.真空泵的作用是使整个制备装置处于负压状态,使装置A中不断吸入的空气,既使得反应溶液混合更均匀,同时还可稀释生成 ,防止浓度过大而分解 ,防止浓度过大而分解 |
(3)装置B内的吸收液:氢氧化钾与过氧化氢的混合液。配置两者浓度,比例需恰当,理由是
(4)取装置A中反应后母液1L蒸发至500
 后,过滤,滤液可循环利用,过滤得到的晶体可进行回收利用制备硫酸氢钾,流程如图所示。
后,过滤,滤液可循环利用,过滤得到的晶体可进行回收利用制备硫酸氢钾,流程如图所示。
反应母液的主要成分表
| 离子 |  |  |  |  |
含量( ) ) | 6.0 | 8.0 | 0.1 | 7.0 |
 ,冷却至室温测得
,冷却至室温测得 浓度为0.2
浓度为0.2 。蒸发过程中,滤液中其他离子浓度变化如下图所示。
。蒸发过程中,滤液中其他离子浓度变化如下图所示。
根据以上数据分析,过滤获得的晶体的成分的化学式
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐2】中学化学中的一些常见物质有如图转化关系。其中A、H为空气中的主要成分,气体B能使湿润的红色石蕊试纸变蓝,气体D遇到A很快变成红棕色E,C是黑色金属氧化物,I是紫红色金属单质。X为常见液体(部分反应条件及生成物没有全部列出)。
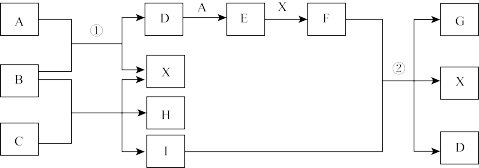
回答下列问题:
(1)B的化学式为________ C的化学式为___________ D的化学式为___________
(2)B的实验室制法的化学方程式____________________
(3)写出反应①的化学方程式_______________________ 。
(4)写出反应②的离子方程式_______________________ 。

回答下列问题:
(1)B的化学式为
(2)B的实验室制法的化学方程式
(3)写出反应①的化学方程式
(4)写出反应②的离子方程式
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐3】现有金属单质A、B、C、D和气体甲、乙、丙及物质E、F、G、H、I,它们之间能发生如下反应(图中有些反应的产物和反应的条件没有全部标出)。
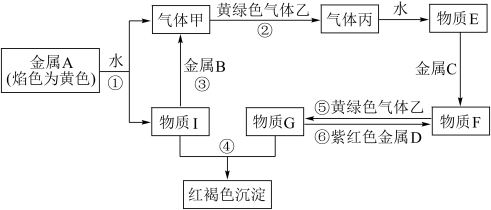
请根据以上信息回答下列问题:
(1)写出下列物质的化学式: B____________ ;F_____________ ;H____________ 。
(2)写出反应①的离子方程式:_____________________________ ;
写出反应⑥的离子方程式:_____________________________ 。
(3)气体乙与SO2气体都具有漂白性,将等体积的气体乙和SO2通入到水中,得到的溶液是否具有漂白性?___ (填“是”或“否”),反应的化学方程式:______________________________________________________ 。

请根据以上信息回答下列问题:
(1)写出下列物质的化学式: B
(2)写出反应①的离子方程式:
写出反应⑥的离子方程式:
(3)气体乙与SO2气体都具有漂白性,将等体积的气体乙和SO2通入到水中,得到的溶液是否具有漂白性?
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐1】氨氧化法是工业生产中制取硝酸的主要途径,某同学用该原理在实验室探究硝酸的制备和性质,设计了如下图所示的装置。

(1)若分液漏斗中氨水的浓度为9.0mol·L-1,配制该浓度的氨水100mL,用到的玻璃仪器有100mL容量瓶、烧杯、量筒、玻璃棒、__________ 。
(2)甲装置不需要加热即能同时产生氨气和氧气,烧瓶内固体X为_________ 。
(3)乙装置的作用是__________ ;写出受热时丙装置发生反应的化学方程式为______________ 。
(4)当戊中观察到___________ 现象,则说明已制得硝酸;某同学按上图组装仪器并检验气密性后进行实验,没有观察到此现象,请分析实验失败的可能原因___________ ,如何改进装置__________ 。
(5)改进后待反应结束,将丁装置倒立在盛水的水槽中,会观察到的现象是_______________ ;为测定试管丁内硝酸溶液的浓度,从中取10mL溶液于锥形瓶中,用0.1 mol·L-1的NaOH溶液滴定,滴定前发现滴定管尖嘴处有少量气泡,请选择排出气泡的正确操作是______________ 。


(1)若分液漏斗中氨水的浓度为9.0mol·L-1,配制该浓度的氨水100mL,用到的玻璃仪器有100mL容量瓶、烧杯、量筒、玻璃棒、
(2)甲装置不需要加热即能同时产生氨气和氧气,烧瓶内固体X为
(3)乙装置的作用是
(4)当戊中观察到
(5)改进后待反应结束,将丁装置倒立在盛水的水槽中,会观察到的现象是

您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
【推荐2】下列物质存在如下图所示的转化关系(反应条件、部分产物未标出),已知某物质X是一种正盐,E是强酸
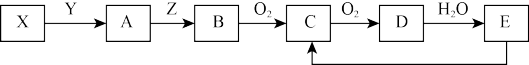
试回答下列问题:
(1)若Y为强酸,且B为黄色固体单质
①从组成物质的元素化合价变化角度预测C可能具有的性质_______________
②一定条件下E转化为C有多种途径,写出其中一种转化的化学反应方程式_______________________ 。
(2)若Y为强碱,且B为空气中含量最高的气态单质
①写出实验室制取A的化学方程式______________________________________ 。
②若A→B的转化常用来检验Z气体管道的是否漏气,用该方法检验的现象是____________________ ,其化学反应方程式_________________________________________ 。
③C、D都是大气污染物,它们对环境造成的危害表现在_______ 。
A.引起酸雨 B.引起温室效应
C.形成光化学烟雾 D.引起水体富营养化
④将x mL C、y mL D混合于同一试管中,将试管倒置于水中,同时通入z mL O2充分反应后,试管内气体全部消失,则x:y:z不可能是_______________
A 1:1:1 B 2:1:1
C 3:7:4 D 1:5:2
(3)无论Y为强酸或强碱均符合上述转化,则物质X的化学式_______________

试回答下列问题:
(1)若Y为强酸,且B为黄色固体单质
①从组成物质的元素化合价变化角度预测C可能具有的性质
②一定条件下E转化为C有多种途径,写出其中一种转化的化学反应方程式
(2)若Y为强碱,且B为空气中含量最高的气态单质
①写出实验室制取A的化学方程式
②若A→B的转化常用来检验Z气体管道的是否漏气,用该方法检验的现象是
③C、D都是大气污染物,它们对环境造成的危害表现在
A.引起酸雨 B.引起温室效应
C.形成光化学烟雾 D.引起水体富营养化
④将x mL C、y mL D混合于同一试管中,将试管倒置于水中,同时通入z mL O2充分反应后,试管内气体全部消失,则x:y:z不可能是
A 1:1:1 B 2:1:1
C 3:7:4 D 1:5:2
(3)无论Y为强酸或强碱均符合上述转化,则物质X的化学式
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐1】亚硝酰氯(NOCl,熔点:-64.5 ℃,沸点:-5.5 ℃)为红褐色液体或黄色气体,具有刺鼻恶臭味,遇水剧烈水解生成氮的两种氧化物与氯化氢,易溶于浓硫酸。常可用于合成清洁剂、触媒剂及中间体等。实验室可由氯气与一氧化氮在常温常压下合成。其制备装置如图所示(其中III、IV中均为浓硫酸):
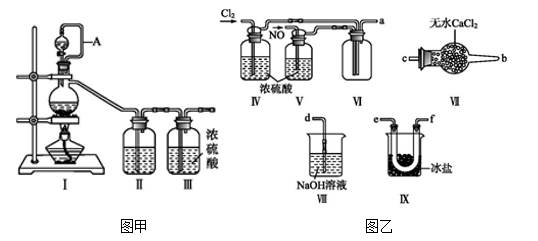
(1)用图甲中装置制备纯净干燥的原料气,补充下表中所缺少的药品。
(2)将制得的NO和Cl2通入图乙对应装置制备NOCl。
①装置连接顺序为a→________ (按气流自左向右方向,用小写字母表示)。
②装置Ⅳ、Ⅴ除可进一步干燥NO、Cl2外,另一个作用是____________ 。
③有人认为可以将装置Ⅳ中浓硫酸合并到装置Ⅴ中,撤除装置Ⅳ,直接将NO、Cl2通入装置Ⅴ中,你同意此观点吗?________ (填同意或不同意),原因是________________________________ 。
④实验开始的时候,先通入氯气,再通入NO,原因为________________ 。
(3)有人认为多余的氯气可以通过下列装置暂时储存后再利用,请选择可以用作氯气的储气的装置______ ;
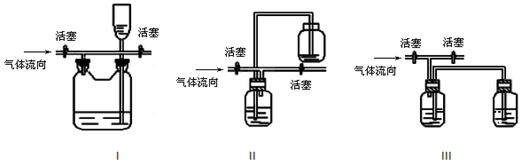
(4)装置Ⅶ吸收尾气时,NOCl发生反应的化学方程式为_______________________ 。
(5)有人认为装置Ⅶ中氢氧化钠溶液只能吸收氯气和NOCl,不能吸收NO,经过查阅资料发现用高锰酸钾溶液可以吸收NO气体,因此在装置Ⅶ氢氧化钠溶液中加入高锰酸钾,反应产生黑色沉淀,写出该反应的离子方程式:__________________________________ 。
(6)制得的NOCl中可能含有少量N2O4杂质,为测定产品纯度进行如下实验:称取1.6625 g样品溶于50.00 ml NaOH溶液中,加入几滴K2CrO4溶液作指示剂,用足量硝酸酸化的0.40mol/LAgNO3溶液滴定至产生砖红色沉淀,消耗AgNO3溶液50.00ml。
①样品的纯度为__________ %(保留1位小数)
②已知常温下,Ksp(AgCl)=1.8×10-10,Ksp(Ag2CrO4)=2×10-12,若在滴定终点时测得溶液中Cr2O42-的浓度是5.0×10-3 mol/L,此时溶液中Cl-浓度是_________ 。

(1)用图甲中装置制备纯净干燥的原料气,补充下表中所缺少的药品。
| 装置Ⅰ | 装置Ⅱ | ||
| 烧瓶中 | 分液漏斗中 | ||
| 制备纯净Cl2 | MnO2 | 浓盐酸 | ① |
| 制备纯净NO | Cu | 稀硝酸 | ② |
(2)将制得的NO和Cl2通入图乙对应装置制备NOCl。
①装置连接顺序为a→
②装置Ⅳ、Ⅴ除可进一步干燥NO、Cl2外,另一个作用是
③有人认为可以将装置Ⅳ中浓硫酸合并到装置Ⅴ中,撤除装置Ⅳ,直接将NO、Cl2通入装置Ⅴ中,你同意此观点吗?
④实验开始的时候,先通入氯气,再通入NO,原因为
(3)有人认为多余的氯气可以通过下列装置暂时储存后再利用,请选择可以用作氯气的储气的装置

(4)装置Ⅶ吸收尾气时,NOCl发生反应的化学方程式为
(5)有人认为装置Ⅶ中氢氧化钠溶液只能吸收氯气和NOCl,不能吸收NO,经过查阅资料发现用高锰酸钾溶液可以吸收NO气体,因此在装置Ⅶ氢氧化钠溶液中加入高锰酸钾,反应产生黑色沉淀,写出该反应的离子方程式:
(6)制得的NOCl中可能含有少量N2O4杂质,为测定产品纯度进行如下实验:称取1.6625 g样品溶于50.00 ml NaOH溶液中,加入几滴K2CrO4溶液作指示剂,用足量硝酸酸化的0.40mol/LAgNO3溶液滴定至产生砖红色沉淀,消耗AgNO3溶液50.00ml。
①样品的纯度为
②已知常温下,Ksp(AgCl)=1.8×10-10,Ksp(Ag2CrO4)=2×10-12,若在滴定终点时测得溶液中Cr2O42-的浓度是5.0×10-3 mol/L,此时溶液中Cl-浓度是
您最近一年使用:0次
【推荐2】某实验小组欲探究浓硝酸的性质。
Ⅰ.木炭与浓硝酸反应:
(1)甲同学设计了图1装置,认为若有红棕色气体产生就说明木炭与浓硝酸发生了反应。写出木炭与浓硝酸反应的化学方程式____________________________ 。
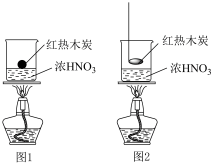
(2)乙同学认为红棕色气体不能作为木炭与浓硝酸反应的证据,其理由是________ 。
(3)乙同学设计了图2装置实验,木炭能燃烧,并产生红棕色气体。针对该实验现象,乙同学做出如下假设:
假设a:_____________________________ ;
假设b:红热木炭使HNO3分解产生NO2,NO2可能具有助燃性,木炭燃烧;
假设c:红热木炭使HNO3分解产生O2,木炭与O2反应燃烧;
假设d:红热木炭使HNO3分解产生NO2和O2,共同影响木炭的燃烧;……
(4)设计实验证明假设b成立,请将实验方案补充完整。
①实验方法:_____________________________________________________ 。
实验现象:木炭在该气体中持续燃烧,火焰迅速变亮,集气瓶中气体颜色变浅直至无色,产生的气体能使澄清石灰水变浑浊,且遇空气不变色。
②根据实验现象写出木炭与此气体反应的化学方程式__________________ 。
Ⅱ.设计硝酸在不同条件下分解实验,方案见下表:
(5)分析上述现象,得出使硝酸成功分解的关键是____________________________ 。
Ⅰ.木炭与浓硝酸反应:
(1)甲同学设计了图1装置,认为若有红棕色气体产生就说明木炭与浓硝酸发生了反应。写出木炭与浓硝酸反应的化学方程式

(2)乙同学认为红棕色气体不能作为木炭与浓硝酸反应的证据,其理由是
(3)乙同学设计了图2装置实验,木炭能燃烧,并产生红棕色气体。针对该实验现象,乙同学做出如下假设:
假设a:
假设b:红热木炭使HNO3分解产生NO2,NO2可能具有助燃性,木炭燃烧;
假设c:红热木炭使HNO3分解产生O2,木炭与O2反应燃烧;
假设d:红热木炭使HNO3分解产生NO2和O2,共同影响木炭的燃烧;……
(4)设计实验证明假设b成立,请将实验方案补充完整。
①实验方法:
实验现象:木炭在该气体中持续燃烧,火焰迅速变亮,集气瓶中气体颜色变浅直至无色,产生的气体能使澄清石灰水变浑浊,且遇空气不变色。
②根据实验现象写出木炭与此气体反应的化学方程式
Ⅱ.设计硝酸在不同条件下分解实验,方案见下表:
| 装置 |  |  |  |
| 操作及现象 | 先点燃i处酒精灯,溶液沸腾后没有观察到红棕色气体产生。然后撤走i处酒精灯,点燃ii处酒精灯并加热试管中部,很快看到大量红棕色气体产生 | 光照8小时 溶液不变黄 | 光照几分钟后看到液面上方出现红棕色,溶液变黄 |
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐3】A、B、C三种非金属元素的质子数之和为16,它们的单质在一定条件下两两化合可以生成三种常见的化合物D、E、F。D、F的一个分子中只含有10个电子,常温下D是一种液体,E的相对分子量比D大。
(1)B的元素名称是______ ,C单质的结构式是______ 。
(2)A、B两元素还能形成一种比D相对分质量大16的化合物,请写出该化合物的一种用途______ ;A、C两元素也还能形成一种比E相对分子大16的化合物,请写出实验室制备该化合物反应的化学方程式__________________ 。
(3)E、F在一定条件下可以发生反应生成C元素的单质和D,该反应中氧化产物与还原产物的物质的量之比为_______ 。
(4)A、B、C三种元素能组成一种原子个数比为3:4:2的常见离子化合物,0.1mol·L-1的该化合物的水溶液中,溶液显_____ 性(填“酸”、“碱”、“中”),用离子方程式解释原因___________ ,
该溶液中离子浓度由大到小的顺序是____________ 。

(1)B的元素名称是
(2)A、B两元素还能形成一种比D相对分质量大16的化合物,请写出该化合物的一种用途
(3)E、F在一定条件下可以发生反应生成C元素的单质和D,该反应中氧化产物与还原产物的物质的量之比为
(4)A、B、C三种元素能组成一种原子个数比为3:4:2的常见离子化合物,0.1mol·L-1的该化合物的水溶液中,溶液显
该溶液中离子浓度由大到小的顺序是
您最近一年使用:0次







 该反应的化学方程式
该反应的化学方程式

