1)22.0g K2R中含有0.4mol钾离子,则该物质的摩尔质量为________ ,R的相对原子质量为________ 。
(2)在恒温条件下的密闭容器中,中间有一可自由滑动的隔板(厚度不计)将容器分成两部分,当在左边充入1 mol N2,右边充入CO和CO2的混合气体共8g时,隔板处于如图位置。

①隔板左右两边气体的气体的分子数之比为______ 。
②右边混合气体中CO和CO2物质的量分别为________ 、________ ,该混合气体平均相对分子质量为______ 。
(3)现有20°C的饱和硫酸铜溶液,其质量分数为16%、密度为1.25g/cm3。则:
①20°C时,硫酸铜的溶解度为________ ;
②该饱和硫酸铜溶液的物质的量浓度为____ ;
③实验室需要250mL 0.5mol/LCuSO4溶液。在配制该溶液时需要称取胆矾(CuSO4·5H2O)的质量为____ ;
④取20mL 0.5mol/LCuSO4溶液恰好与50mLNaOH溶液反应,使Cu2+完全转化为沉淀。请计算氢氧化钠溶液的物质的量浓度(写出过程)____ 。
(2)在恒温条件下的密闭容器中,中间有一可自由滑动的隔板(厚度不计)将容器分成两部分,当在左边充入1 mol N2,右边充入CO和CO2的混合气体共8g时,隔板处于如图位置。

①隔板左右两边气体的气体的分子数之比为
②右边混合气体中CO和CO2物质的量分别为
(3)现有20°C的饱和硫酸铜溶液,其质量分数为16%、密度为1.25g/cm3。则:
①20°C时,硫酸铜的溶解度为
②该饱和硫酸铜溶液的物质的量浓度为
③实验室需要250mL 0.5mol/LCuSO4溶液。在配制该溶液时需要称取胆矾(CuSO4·5H2O)的质量为
④取20mL 0.5mol/LCuSO4溶液恰好与50mLNaOH溶液反应,使Cu2+完全转化为沉淀。请计算氢氧化钠溶液的物质的量浓度(写出过程)
更新时间:2019-12-16 20:23:24
|
相似题推荐
计算题
|
适中
(0.65)
名校
【推荐1】(1)标准状况下VL氨气溶解在1L水中(水的密度近似为1g/mL),所得溶液的密度为ρg/mL,则该溶液的溶质的物质的量浓度为______ 。
(2)在11P+15CuSO4+24H2O=5Cu3P+6H3PO4+15H2SO4中,每1molCuSO4可以氧化磷的物质的量是______ 。
(3)两个同容积的密封容器A、B,常温下,A中充入agA气体,B中充入agCH4气体,A与B内的压强之比是4:11,则A的摩尔质量为______ 。
(4)20mLCaCl2溶液加水稀释至100mL,稀释后的溶液中Cl-离子的物质的量浓度为1mol/L,则稀释前CaCl2的物质的量浓度为______ 。
(5)在一定温度和压强下,3L气体A2跟9L体积的气体B2完全化合生成6L体积某气体C,则该气体C的化学式为(用A、B表示)______ 。
(2)在11P+15CuSO4+24H2O=5Cu3P+6H3PO4+15H2SO4中,每1molCuSO4可以氧化磷的物质的量是
(3)两个同容积的密封容器A、B,常温下,A中充入agA气体,B中充入agCH4气体,A与B内的压强之比是4:11,则A的摩尔质量为
(4)20mLCaCl2溶液加水稀释至100mL,稀释后的溶液中Cl-离子的物质的量浓度为1mol/L,则稀释前CaCl2的物质的量浓度为
(5)在一定温度和压强下,3L气体A2跟9L体积的气体B2完全化合生成6L体积某气体C,则该气体C的化学式为(用A、B表示)
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】化学计量在化学中占有重要地位,请回答下列问题:
(1)现有mg某气体,它由双原子分子构成,其摩尔质量为Mg/mol。若阿伏加德罗常数用NA表示,则:
①该气体的物质的量为________ ;
②该气体所含原子总数为_______________ 个;
③该气体在标准状况下的体积为__________ 。
(2)与标准状况下V LCO2所含氧原子数目相同的水的质量是_______ (用分式表示)。
(3)在一定的温度和压强下,1体积气体X2跟3体积气体Y2化合生成2体积化合物,则该化合物的化学式是______________ 。
(4)某盐混合溶液中含有离子:Na+、Mg2+、Cl-、SO42-,测得Na+、Mg2+和Cl-的物质的量浓度依次为:0.2mol/L、0.25mol/L、0.4 mol/L,则c(SO42-)=__________ 。
(1)现有mg某气体,它由双原子分子构成,其摩尔质量为Mg/mol。若阿伏加德罗常数用NA表示,则:
①该气体的物质的量为
②该气体所含原子总数为
③该气体在标准状况下的体积为
(2)与标准状况下V LCO2所含氧原子数目相同的水的质量是
(3)在一定的温度和压强下,1体积气体X2跟3体积气体Y2化合生成2体积化合物,则该化合物的化学式是
(4)某盐混合溶液中含有离子:Na+、Mg2+、Cl-、SO42-,测得Na+、Mg2+和Cl-的物质的量浓度依次为:0.2mol/L、0.25mol/L、0.4 mol/L,则c(SO42-)=
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐3】在下面的横线上填上适当的内容。
(1)6.02×1024个Na+约含有________ mol Na+,其质量为________ g。
(2)0.5mol CH4约含有________ 个CH4,其含有的电子数为________ mol。
(3)49 g H3PO4共含有________ mol原子。
(4)3.01×1024个 与
与________ mol  的质量相同。
的质量相同。
(5)15.6g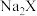 中含有0.4mol
中含有0.4mol ,则X的相对原子质量为
,则X的相对原子质量为__________ 。
(6)常温常压下,用等质量的 、
、 、
、 、
、 四种气体分别吹出四个气球,其中气体为
四种气体分别吹出四个气球,其中气体为 的是
的是________ (填序号)。
A. B.
B. C.
C. D.
D.
(1)6.02×1024个Na+约含有
(2)0.5mol CH4约含有
(3)49 g H3PO4共含有
(4)3.01×1024个
 与
与 的质量相同。
的质量相同。(5)15.6g
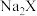 中含有0.4mol
中含有0.4mol ,则X的相对原子质量为
,则X的相对原子质量为(6)常温常压下,用等质量的
 、
、 、
、 、
、 四种气体分别吹出四个气球,其中气体为
四种气体分别吹出四个气球,其中气体为 的是
的是A.
 B.
B. C.
C. D.
D.
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】填空:
(1)2molSO3和3molSO2的分子数之比为___________ ,原子数之比___________ ;某氯化物(MC12)的质量为19g,含有0.4molCl-,则M的摩尔质量为___________ 。
(2)标准状况下,N2和O2组成的混合气体0.5mol,其体积为___________ ;常温常压下,相同体积的CH4和NH3质量之比为___________ ,质子数之比为___________ 。
(3)现有标准状况下CO和CO2混合气体6.72L,其质量为10.8g,则此混合气体中,CO和CO2的分子数之比是___________ 。
(1)2molSO3和3molSO2的分子数之比为
(2)标准状况下,N2和O2组成的混合气体0.5mol,其体积为
(3)现有标准状况下CO和CO2混合气体6.72L,其质量为10.8g,则此混合气体中,CO和CO2的分子数之比是
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】现有以下物质:①H2SO4;②液氨;③KOH固体;④熔融KHSO4;⑤Fe(OH)3胶体;⑥银;⑦SO2;⑧CH3COOH;⑨蔗糖;⑩苯;⑪酒精。请回答下列问题:
(1)以上物质中能导电的是_______ (填序号),以上物质中属于电解质的是_______ (填序号)。以上物质中属于非电解质的是_______ (填序号)。
(2)某物质A加热时按化学方程式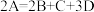 分解,产物均为气体,测得相同条件下由生成物组成的混合物气体对
分解,产物均为气体,测得相同条件下由生成物组成的混合物气体对 的相对密度为40,则反应物A的摩尔质量为
的相对密度为40,则反应物A的摩尔质量为_______ 。
(3)质量比为11:7:16的 、CO、
、CO、 ,它们所含分子数之比为
,它们所含分子数之比为_______ ,所含氧原子数之比为_______ 。
(4)标准状况下有①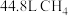 ,②
,② 个
个 分子,③
分子,③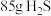 三种气体,对这三种气体的物质的量从大到小的顺序是
三种气体,对这三种气体的物质的量从大到小的顺序是_______ 。(填序号)
(5)在标准状况下,用干燥的烧瓶装满一瓶氯化氢和氢气的混合气体倒置于水槽中,此时烧瓶中盐酸的物质的量浓度是_______ mol/L。(假设烧瓶内的液体不扩散出水槽)
(6)标准状况下,将V L的氨气溶于0.2L的水中,所得溶液的密度为d g·cm-3,此氨水的物质的量浓度是_______ mol/L;已知25%的氨水的密度为ρ1g/cm3,5%的氨水的密度为ρ2g/ cm3,ρ1<ρ2,若将上述两种溶液等体积混合,所得氨水的质量分数_______ 15%(填>、<或=)。
(1)以上物质中能导电的是
(2)某物质A加热时按化学方程式
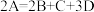 分解,产物均为气体,测得相同条件下由生成物组成的混合物气体对
分解,产物均为气体,测得相同条件下由生成物组成的混合物气体对 的相对密度为40,则反应物A的摩尔质量为
的相对密度为40,则反应物A的摩尔质量为(3)质量比为11:7:16的
 、CO、
、CO、 ,它们所含分子数之比为
,它们所含分子数之比为(4)标准状况下有①
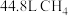 ,②
,② 个
个 分子,③
分子,③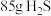 三种气体,对这三种气体的物质的量从大到小的顺序是
三种气体,对这三种气体的物质的量从大到小的顺序是(5)在标准状况下,用干燥的烧瓶装满一瓶氯化氢和氢气的混合气体倒置于水槽中,此时烧瓶中盐酸的物质的量浓度是
(6)标准状况下,将V L的氨气溶于0.2L的水中,所得溶液的密度为d g·cm-3,此氨水的物质的量浓度是
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐1】(1)0.5mol C2H2O4的质量是_______ g,约含______ 个C2H2O4分子,含______ mol氧原子。
(2)38.4g SO2在标准状况下的体积为___________ L,该气体在标准状况下的密度是______________ 。
(3)在标准状况下,将_______ L NH3溶于水得到0.5 mol·L-1的氨水250 mL;配制100 mL 0.2 mol·L-1CuSO4溶液,需要CuSO4·5H2O________ g。
(4)液态化合物XY2在一定量O2中恰好完全燃烧(XY2(液)+ 3O2(气)= XO2(气)+ 2YO2(气)),冷却后,在标准状况下测得生成物的体积是672mL,密度是2.56g/L,则:
①反应前O2的体积是___________ mL。 ②化合物XY2的摩尔质量是___________ 。
③若XY2分子中X、Y两元素的质量之比为3:16,则X、Y两元素分别是_________ 和________ 。(写元素符号)。
(2)38.4g SO2在标准状况下的体积为
(3)在标准状况下,将
(4)液态化合物XY2在一定量O2中恰好完全燃烧(XY2(液)+ 3O2(气)= XO2(气)+ 2YO2(气)),冷却后,在标准状况下测得生成物的体积是672mL,密度是2.56g/L,则:
①反应前O2的体积是
③若XY2分子中X、Y两元素的质量之比为3:16,则X、Y两元素分别是
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】医院处方药“复方电解质注射液”可作为水、电解质的补充源,注射液中含有NaCl、MgCl2和KCl三种无机盐,其中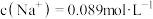 。
。
(1)若实验室药配制该电解质注射液500mL,所需的玻璃仪器有:玻璃板、烧杯和_______ ,需用托盘天平称量氯化钠固体___________ g;
(2)已知该注射液中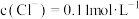 ,
,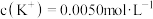 ,则
,则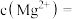
________  。
。
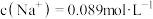 。
。(1)若实验室药配制该电解质注射液500mL,所需的玻璃仪器有:玻璃板、烧杯和
(2)已知该注射液中
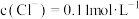 ,
,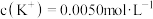 ,则
,则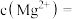
 。
。
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐3】将24.4gNaOH固体溶于水,配成100mL溶液,其密度为1.22g/mL,请回答下列问题。
(1)从该溶液中取出10mL,其中NaOH的物质的量浓度为________ ,NaOH的质量分数为___________ ,溶液的密度为________ ,含NaOH的物质的量为_________ ;将取出的10mL溶液加水稀释到100mL,稀释后溶液中NaOH的物质的量浓度为_______ 。
(2)用等体积的0.2mol·Lˉ1的BaCl2溶液,可使相同体积的Na2SO4、KAl(SO4)2、Fe2(SO4)3三种溶液中的SO42ˉ完全沉淀,则三种硫酸盐的物质的量浓度之比为____ 。
(1)从该溶液中取出10mL,其中NaOH的物质的量浓度为
(2)用等体积的0.2mol·Lˉ1的BaCl2溶液,可使相同体积的Na2SO4、KAl(SO4)2、Fe2(SO4)3三种溶液中的SO42ˉ完全沉淀,则三种硫酸盐的物质的量浓度之比为
您最近一年使用:0次



