(1)按要求写出电子式:CO2_________ COCl2_________ NaCN______ N2H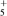
_______
(2)元素周期表中“对角线规则”是指处于周期表中对角线位置(左上和右下方)的两元素,其性质具有相似性,例如:Be和Al处于对角线位置。写出Be与氢氧化钠溶液反应的化学方程式:_________________________________ 。
(3)写出氢,氧,钠,硫四种元素组成的两种酸式盐发生复分解反应的离子方程式:___________________ 。
(2)元素周期表中“对角线规则”是指处于周期表中对角线位置(左上和右下方)的两元素,其性质具有相似性,例如:Be和Al处于对角线位置。写出Be与氢氧化钠溶液反应的化学方程式:
(3)写出氢,氧,钠,硫四种元素组成的两种酸式盐发生复分解反应的离子方程式:
更新时间:2020-01-03 10:47:15
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】铝及其化合物在生产生活中具有重要的作用。
(1)铝属于活泼金属却能在空气中稳定存在,原因是(用化学用语及相关文字说明)___ 。
(2)铝电池性能优越,在现代生产、生活中有广泛的应用。铝—空气电池以其环保、安全而受到越来越多的关注,其原理如图所示。
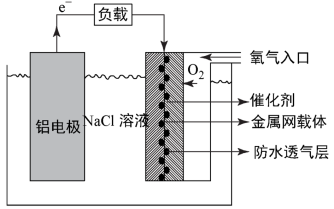
该电池的正极反应方程式为___ ,当铝电极质量减少9克,则另一极通入的氧气的体积在标准状况下为___ 。
(3)AlCl3与NaN3在高温下反应可制得高温结构陶瓷氮化铝(AlN),且生成N2。写出反应化学方程式为___ 。
(4)在元素周期表中,砷位于铝的下一周期,与氮元素同主族,写出AsH3分子的电子式为___ ,相同压强下,AsH3的沸点___ NH3(填“大于”或“小于”)。
(1)铝属于活泼金属却能在空气中稳定存在,原因是(用化学用语及相关文字说明)
(2)铝电池性能优越,在现代生产、生活中有广泛的应用。铝—空气电池以其环保、安全而受到越来越多的关注,其原理如图所示。

该电池的正极反应方程式为
(3)AlCl3与NaN3在高温下反应可制得高温结构陶瓷氮化铝(AlN),且生成N2。写出反应化学方程式为
(4)在元素周期表中,砷位于铝的下一周期,与氮元素同主族,写出AsH3分子的电子式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】1998年中国十大科技成果之一是合成氮化镓纳米材料,已知镓(Ga)的原子结构示意图如图所示,则:

(1)x的值为_______ ;
(2)镓元素的化学性质与下列哪种元素的化学性质最相似_______ (在A、B、C图中选择,填字母);
A. B.
B.  C.
C.
(3)氯化镓的化学式为_______ ,请写出氯原子的结构示意图_______ ,氯离子的电子式_______ 。

(1)x的值为
(2)镓元素的化学性质与下列哪种元素的化学性质最相似
A.
 B.
B.  C.
C.
(3)氯化镓的化学式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】请根据已知信息回答下列各问:
I.已知H3PO2(次磷酸)是一元酸,H3PO2水溶液中存在H3PO2分子。
(1)写出H3PO2溶液与足量NaOH溶液反应的离子方程式___________ 。
(2)磷酸(H3PO4)、亚磷酸(H3PO3)、次磷酸都是重要的化工产品。已知:1mol磷酸、亚磷酸、次磷酸最多消耗NaOH的物质的量依次为3mol、2mol、1mol。则Na2HPO4、NaH2PO2、Na2HPO3中属于酸式盐的是___________ (填化学式)。
II.NaHSO4可用作清洁剂、防腐剂等。
(3)下列关于NaHSO4的说法正确的是___________ 。
a.NaHSO4固体不能导电
b.NaHSO4溶液的导电性一定强于CH3COOH溶液
c.NaHSO4属于电解质
d.NaHSO4溶液显中性
(4)NaHSO4溶液与NaHCO3溶液反应的离子方程式为___________ 。
III.有以下物质:
①石墨、②铁、③蔗糖、④一氧化碳、⑤氯化铁固体、⑥碳酸氢钠固体、⑦氢氧化钡溶液、⑧纯醋酸、⑨熔融氯化钠、⑩液态氯化氢
(5)以上物质属于电解质的是___________ 。
(6)写出用⑤的饱和溶液制备Fe(OH)3胶体的离子反应方程式:___________ 。
(7)将物质⑥配制成溶液,逐滴加入⑦溶液中至Ba2+恰好沉淀完全,写出离子方程式:_____ 。
I.已知H3PO2(次磷酸)是一元酸,H3PO2水溶液中存在H3PO2分子。
(1)写出H3PO2溶液与足量NaOH溶液反应的离子方程式
(2)磷酸(H3PO4)、亚磷酸(H3PO3)、次磷酸都是重要的化工产品。已知:1mol磷酸、亚磷酸、次磷酸最多消耗NaOH的物质的量依次为3mol、2mol、1mol。则Na2HPO4、NaH2PO2、Na2HPO3中属于酸式盐的是
II.NaHSO4可用作清洁剂、防腐剂等。
(3)下列关于NaHSO4的说法正确的是
a.NaHSO4固体不能导电
b.NaHSO4溶液的导电性一定强于CH3COOH溶液
c.NaHSO4属于电解质
d.NaHSO4溶液显中性
(4)NaHSO4溶液与NaHCO3溶液反应的离子方程式为
III.有以下物质:
①石墨、②铁、③蔗糖、④一氧化碳、⑤氯化铁固体、⑥碳酸氢钠固体、⑦氢氧化钡溶液、⑧纯醋酸、⑨熔融氯化钠、⑩液态氯化氢
(5)以上物质属于电解质的是
(6)写出用⑤的饱和溶液制备Fe(OH)3胶体的离子反应方程式:
(7)将物质⑥配制成溶液,逐滴加入⑦溶液中至Ba2+恰好沉淀完全,写出离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】肼(N2H4)是一种重要的液态火箭燃料,具有弱碱性和强还原性.工业上利用尿素[CO(NH2)2]、NaClO在NaOH溶液中发生反应生成水合肼(N2H4•H2O)、Na2CO3等产物.请回答:
(1)上述生成水合肼的反应中尿素是________ ( 填“氧化剂”或“还原剂”),反应的化学方程式为________ .
(2)肼与盐酸反应可生成N2H6Cl2 , N2H6Cl2的水溶液显________ 性( 填“酸”或“碱”或“中”),用离子方程式表示其原因________ .
(3)查资料得,在高温下肼可将锅炉内壁表面的铁锈转化为致密的氧化膜.取3.2g肼与96g该铁锈样品(可看作是Fe2O3)在高温下恰好完全反应生成氮气等产物,写出该反应的化学方程式________ .
若要设计实验方案检验上述反应生成固体产物中的金属阳离子,补充完整下列实验步骤:
①所得固体溶入浓盐酸中; ②________
(1)上述生成水合肼的反应中尿素是
(2)肼与盐酸反应可生成N2H6Cl2 , N2H6Cl2的水溶液显
(3)查资料得,在高温下肼可将锅炉内壁表面的铁锈转化为致密的氧化膜.取3.2g肼与96g该铁锈样品(可看作是Fe2O3)在高温下恰好完全反应生成氮气等产物,写出该反应的化学方程式
若要设计实验方案检验上述反应生成固体产物中的金属阳离子,补充完整下列实验步骤:
①所得固体溶入浓盐酸中; ②
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】阅读下段语句,“我国海水制盐具有悠久的历史。从海水中制得的氯化钠除食用外,还用作工业原料,如生产①烧碱、②纯碱、③金属钠、④氯气、⑤漂白液(主要成分:NaCl和NaClO)、⑥次氯酸(化学式:HClO)等含氯化工产品”。
(1)语句中的化学物质中,属于电解质的是_______ (填序号),可以导电的是_______ (填序号)。
(2)语句中漂白液在酸性条件下发生归中反应生成氯气,反应的离子方程式为_______ 。
(3)从海水获得较纯净的氯化钠的简要流程如下:

①流程图中试剂1、试剂2和试剂3,可行的组合是_______ 。
A.NaOH溶液 溶液
溶液 溶液
溶液
B. 溶液NaOH溶液
溶液NaOH溶液 溶液
溶液
C. 溶液
溶液 溶液NaOH溶液
溶液NaOH溶液
D.NaOH溶液 溶液
溶液 溶液
溶液
②试剂4的化学式为_______ 。
③操作的名称:_______ 。
(4)若纯碱溶液中 与盐酸溶液中的HCl按4∶7反应的离子方程式为
与盐酸溶液中的HCl按4∶7反应的离子方程式为_______ 。
(1)语句中的化学物质中,属于电解质的是
(2)语句中漂白液在酸性条件下发生归中反应生成氯气,反应的离子方程式为
(3)从海水获得较纯净的氯化钠的简要流程如下:

①流程图中试剂1、试剂2和试剂3,可行的组合是
A.NaOH溶液
 溶液
溶液 溶液
溶液B.
 溶液NaOH溶液
溶液NaOH溶液 溶液
溶液C.
 溶液
溶液 溶液NaOH溶液
溶液NaOH溶液D.NaOH溶液
 溶液
溶液 溶液
溶液②试剂4的化学式为
③操作的名称:
(4)若纯碱溶液中
 与盐酸溶液中的HCl按4∶7反应的离子方程式为
与盐酸溶液中的HCl按4∶7反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】回答下列问题:
(1)锂和镁在元素周期表中有特殊“对角线”关系,它们的性质相似。下列有关锂及其化合物的叙述不正确的是___ 。
A.Li2SO4难溶于水
B.Li与N2反应产物是Li3N
C.LiOH难溶于水
D.LiOH与Li2CO3受热都易分解
(2)与铝位于对角线位置的第二周期元素是Be,能区别Be(OH)2和Mg(OH)2的一种试剂是___ ,反应的离子方程式为___ 。
(3)门捷列夫在研究元素周期表时,科学地预言了11种尚未发现的元素,为它们在周期表中留下空位。例如,他预测在铝的下方有一个与铝类似的元素“类铝”,后来被法国化学家于1875年发现,命名为镓。它在周期表中的位置是___ 。
(4)关于与镓同主族的第六周期元素性质的推测中不正确的是___ 。
A.单质是银白色较软的金属
B.其氢氧化物是两性氢氧化物
C.在化合物中显+3价
D.单质与盐酸的反应比铝剧烈
(5)写出短周期主族元素中原子半径最大的原子的单质在空气中加热条件下反应产物的电子式___ 。
(1)锂和镁在元素周期表中有特殊“对角线”关系,它们的性质相似。下列有关锂及其化合物的叙述不正确的是
A.Li2SO4难溶于水
B.Li与N2反应产物是Li3N
C.LiOH难溶于水
D.LiOH与Li2CO3受热都易分解
(2)与铝位于对角线位置的第二周期元素是Be,能区别Be(OH)2和Mg(OH)2的一种试剂是
(3)门捷列夫在研究元素周期表时,科学地预言了11种尚未发现的元素,为它们在周期表中留下空位。例如,他预测在铝的下方有一个与铝类似的元素“类铝”,后来被法国化学家于1875年发现,命名为镓。它在周期表中的位置是
(4)关于与镓同主族的第六周期元素性质的推测中不正确的是
A.单质是银白色较软的金属
B.其氢氧化物是两性氢氧化物
C.在化合物中显+3价
D.单质与盐酸的反应比铝剧烈
(5)写出短周期主族元素中原子半径最大的原子的单质在空气中加热条件下反应产物的电子式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】下列8种化学符号: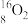 、
、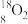 、
、 、
、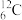 、
、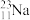 、
、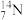 、
、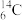 、
、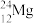 。
。
(1)表示核素的符号共______ 种。
(2)互为同位素的是________________ 。
(3)质量相同的H216O和D216O所含中子数之比为________ 。
根据周期表对角线规则,金属Be与Al单质及其化合物性质相似。试回答下列问题:
(4)写出Be与NaOH溶液反应生成Na2[Be(OH)4]的离子方程式:__________________ 。
(5)Be(OH)2与Mg(OH)2可用____________________ 试剂鉴别。
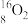 、
、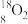 、
、 、
、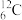 、
、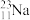 、
、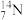 、
、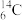 、
、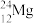 。
。(1)表示核素的符号共
(2)互为同位素的是
(3)质量相同的H216O和D216O所含中子数之比为
根据周期表对角线规则,金属Be与Al单质及其化合物性质相似。试回答下列问题:
(4)写出Be与NaOH溶液反应生成Na2[Be(OH)4]的离子方程式:
(5)Be(OH)2与Mg(OH)2可用
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】目前已发现,在元素周期表中某些元素与右下方的主族元素的有些性质相似,这种相似性被称为对角线规则。据此回答下列问题:
(1)铍的最高价氧化物对应水化物的化学式是______ ,属于两性化合物,证明这一结论的有关离子方程式为______ 、______ 。
(2)若已知反应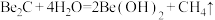 ,则
,则 与足量强碱溶液反应的离子方程式为
与足量强碱溶液反应的离子方程式为______ 。
(3)科学家证实, 属于共价化合物,请设计一个简单实验证明,方法是
属于共价化合物,请设计一个简单实验证明,方法是______ 。用电子式表示 的形成过程:
的形成过程:______ 。
(1)铍的最高价氧化物对应水化物的化学式是
(2)若已知反应
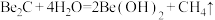 ,则
,则 与足量强碱溶液反应的离子方程式为
与足量强碱溶液反应的离子方程式为(3)科学家证实,
 属于共价化合物,请设计一个简单实验证明,方法是
属于共价化合物,请设计一个简单实验证明,方法是 的形成过程:
的形成过程:
您最近一年使用:0次



