按要求写出:
(1)溴化钾电子式_____________________ 。
(2)硫化钠电子式_____________________ 。
(3)二氧化碳的电子式______________ 。
(4)铵根离子的电子式_____________ 。
(5)氮气的电子式______________ 。
(6)甲烷的结构式____________ 。
(1)溴化钾电子式
(2)硫化钠电子式
(3)二氧化碳的电子式
(4)铵根离子的电子式
(5)氮气的电子式
(6)甲烷的结构式
更新时间:2019-06-11 14:58:37
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】元素单质及其化合物有广泛用途,请根据周期表中第三周期元素相关知识回答下列问题:
(1)第三周期元素的原子所形成的简单离子中:半径最大的阴离子是__ ;氧化性最强的阳离子是__ .
(2)下列事实可以作为S和Cl非金属性强弱的判断依据的是__ (选填序号)
a.Cl的最高正价比S高 b.可用浓H2SO4制HCl
c.HCl的酸性比H2S强 d.Cl2与H2S反应生成S.
(3)硅元素最外层有__ 种能量不同的电子;SiCl4的空间构型和CH4相同,写出SiCl4的电子式:__ .
(4)PH3和NH3的某些化学性质相似.下列对晶体PH4I性质的推测,错误的是__ (选填序号)
a.PH4I是一种共价化合物 b.PH4I能与烧碱溶液反应
c.PH4I加热后会发生升华 d.PH4I溶液能与溴水反应.
(5)二氯化二硫(S2C12)可用作橡胶工业的硫化剂,它的分子结构与H2O2相似.下列有关说法不正确的是__ (选填序号)
a.S2C12分子中有4对共用电子对
b.S2C12分子中没有非极性键
c.S2C12分子中,S为+1价,Cl为﹣1价
d.S2C12分子中各原子均为8电子稳定结构.
(1)第三周期元素的原子所形成的简单离子中:半径最大的阴离子是
(2)下列事实可以作为S和Cl非金属性强弱的判断依据的是
a.Cl的最高正价比S高 b.可用浓H2SO4制HCl
c.HCl的酸性比H2S强 d.Cl2与H2S反应生成S.
(3)硅元素最外层有
(4)PH3和NH3的某些化学性质相似.下列对晶体PH4I性质的推测,错误的是
a.PH4I是一种共价化合物 b.PH4I能与烧碱溶液反应
c.PH4I加热后会发生升华 d.PH4I溶液能与溴水反应.
(5)二氯化二硫(S2C12)可用作橡胶工业的硫化剂,它的分子结构与H2O2相似.下列有关说法不正确的是
a.S2C12分子中有4对共用电子对
b.S2C12分子中没有非极性键
c.S2C12分子中,S为+1价,Cl为﹣1价
d.S2C12分子中各原子均为8电子稳定结构.
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】下列原子结构示意图是否正确?如有错误,指出错误的原因并改正。
F
_______ ;Na
_______ ;Mg
_______ ;Si
_______ ;S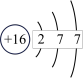
_______ 。
F





您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】按要求回答下列问题:
(1)写出漂白粉中有效成分的化学式___________ 。
(2)写出中子数为8的碳原子符号___________ 。
(3)镁离子的结构示意图___________ 。
(4)工业上用覆铜板制作印刷电路板,对应的离子方程式为___________ 。
(5)写出实验室制取氧气反应的化学方程式___________ 。
(1)写出漂白粉中有效成分的化学式
(2)写出中子数为8的碳原子符号
(3)镁离子的结构示意图
(4)工业上用覆铜板制作印刷电路板,对应的离子方程式为
(5)写出实验室制取氧气反应的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】钠元素在自然界中普遍存在。
(1)画出钠的原子结构示意图___________ ,根据原子结构示意图,钠具有___________ (填“氧化性”或“还原性”)
(2)钠与水反应的实验现象的原因有:
A.钠与水界面各部分产生H2的量不同,所受推力不均匀;
B.钠的密度比水小;
C.钠与水反应放热,使熔点低的钠熔化成小球;
D.钠不断与水反应,直到反应完全;
E.生成的氢氧化钠使酚酞试液变红。
请在下发填写。描述的现象相对应的原因。
(3)写出钠与水反应的化学方程式:___________ 。
(4)金属钠着火时用___________进行灭火
(1)画出钠的原子结构示意图
(2)钠与水反应的实验现象的原因有:
A.钠与水界面各部分产生H2的量不同,所受推力不均匀;
B.钠的密度比水小;
C.钠与水反应放热,使熔点低的钠熔化成小球;
D.钠不断与水反应,直到反应完全;
E.生成的氢氧化钠使酚酞试液变红。
请在下发填写。描述的现象相对应的原因。
| 实验现象 | 原因(填以上序号) |
| 钠浮在水面上 | |
| 熔成闪亮的小球 | |
| 小球向各个方向迅速游动,并发出“嘶嘶”的声音 | |
| 小球逐渐变小以后完全消失 | |
| 在反应后的溶液中滴入酚酞试液显红色 |
(3)写出钠与水反应的化学方程式:
(4)金属钠着火时用___________进行灭火
| A.水 | B.泡沫灭火器 | C.干粉灭火器 | D.干燥的沙土 |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】完成下列化学用语。
(1)Mn原子的电子排布式:___________ 。
(2) 的离子结构示意图为
的离子结构示意图为___________ 。
(3)Co的价电子排布图为___________ 。
(4) 系统命名:
系统命名:___________ 。
(5)4,4-二甲基-2-戊醇的结构简式为___________ 。
(6) 分子中最多有
分子中最多有___________ 个原子在同一平面内。
(1)Mn原子的电子排布式:
(2)
 的离子结构示意图为
的离子结构示意图为(3)Co的价电子排布图为
(4)
 系统命名:
系统命名:(5)4,4-二甲基-2-戊醇的结构简式为
(6)
 分子中最多有
分子中最多有
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】回答下列问题:
(1) 元素基态原子的最外层有
元素基态原子的最外层有 个未成对电子,次外层有
个未成对电子,次外层有 个电子,其元素符号为
个电子,其元素符号为_______ ;其价电子排布图为_______ 。
(2) 元素的负一价离子和
元素的负一价离子和 元素的正一价离子的电子层结构都与氩相同,
元素的正一价离子的电子层结构都与氩相同, 的元素符号为
的元素符号为_______ , 离子的结构示意图为
离子的结构示意图为_______ 。
(3) 元素的正三价离子的
元素的正三价离子的 能级为半充满,
能级为半充满, 的元素符号为
的元素符号为_______ ,其基态原子的电子排布式为_______ ,其原子的结构示意图为_______ 。
(4) 元素基态原子的
元素基态原子的 层全充满,
层全充满, 层没有成对电子且只有一个未成对电子,
层没有成对电子且只有一个未成对电子, 的元素符号为
的元素符号为_______ ,其基态原子的电子排布式为_______ 。
(5) 元素的原子最外层电子排布式为
元素的原子最外层电子排布式为 ,则
,则
_______ ;原子中能量最高的是_______ 电子,核外电子排布图为_______ 。
(1)
 元素基态原子的最外层有
元素基态原子的最外层有 个未成对电子,次外层有
个未成对电子,次外层有 个电子,其元素符号为
个电子,其元素符号为(2)
 元素的负一价离子和
元素的负一价离子和 元素的正一价离子的电子层结构都与氩相同,
元素的正一价离子的电子层结构都与氩相同, 的元素符号为
的元素符号为 离子的结构示意图为
离子的结构示意图为(3)
 元素的正三价离子的
元素的正三价离子的 能级为半充满,
能级为半充满, 的元素符号为
的元素符号为(4)
 元素基态原子的
元素基态原子的 层全充满,
层全充满, 层没有成对电子且只有一个未成对电子,
层没有成对电子且只有一个未成对电子, 的元素符号为
的元素符号为(5)
 元素的原子最外层电子排布式为
元素的原子最外层电子排布式为 ,则
,则
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】工业上可以用NaCl溶液制取重要的化工原料纯碱,此化工流程还需要一定量的CO2和NH3。
(1)NH3的分子构型是_______ ,用电子式表示NH3分子的形成过程_______ 。
(2)工业上合成氨气需要使用氮气,氮原子的结构示意图是_______ ,氮气分子的结构式是_______ 。
(3)羰基硫COS的分子构型与CO2分子相似,可以看作CO2分子中的1个氧原子被硫原子取代。COS的电子式是_______ ,它是_______ (填“极性”或“非极性”)分子。
(1)NH3的分子构型是
(2)工业上合成氨气需要使用氮气,氮原子的结构示意图是
(3)羰基硫COS的分子构型与CO2分子相似,可以看作CO2分子中的1个氧原子被硫原子取代。COS的电子式是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】下表为元素周期表的一部分,请参照元素①—⑧在表中的位置,用化学用语回答下列问题:

(1)②在元素周期表中的位置是______________________ 。
(2)②的最简单氢化物分子的空间结构呈___________ ,③的单质的结构式为___________ ,③、⑤两种元素形成的既含离子键又含非极性共价键的化合物的电子式为___________ 。
(3)④、⑤、⑥的简单离子半径由大到小的顺序为______________________ 。(填离子符号)。
(4)②、⑥、⑦的最高价氧化物的水化物的酸性由强到弱的顺序是___________ (填化学式)。
(5)⑤、⑥的最高价氧化物的水化物相互反应的离子方程式为___________ 。

(1)②在元素周期表中的位置是
(2)②的最简单氢化物分子的空间结构呈
(3)④、⑤、⑥的简单离子半径由大到小的顺序为
(4)②、⑥、⑦的最高价氧化物的水化物的酸性由强到弱的顺序是
(5)⑤、⑥的最高价氧化物的水化物相互反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】价类二维图是学习元素及其化合物知识的重要模型。它是以元素化合价为纵坐标,物质类别为横坐标的二维平面图象。如图为氯元素的价类二维图。

(1)氯元素在周期表中的位置___________ ,写出③的化学式___________ ,①中含有的化学键类型为___________ ,请用电子式表示物质⑤的形成过程___________ 。
(2)写出实验室用二氧化锰固体与浓盐酸制备物质②的离子方程式___________ ,在该反应中浓盐酸体现了___________ 性。若制备标准状况下5.6L的物质②,则被氧化的HCl的质量为___________ 克。
(3)管道工人通常用浓氨水检查输送②的管道是否漏气,反应方程式为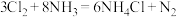 ,请用单线桥法表示出该反应转移电子的方向和数目
,请用单线桥法表示出该反应转移电子的方向和数目___________ 。

(1)氯元素在周期表中的位置
(2)写出实验室用二氧化锰固体与浓盐酸制备物质②的离子方程式
(3)管道工人通常用浓氨水检查输送②的管道是否漏气,反应方程式为
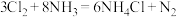 ,请用单线桥法表示出该反应转移电子的方向和数目
,请用单线桥法表示出该反应转移电子的方向和数目
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】按照组成元素可将有机物分为烃和烃的衍生物。
I.某些烃分子的模型如图所示:

回答下列问题:
(1)乙的分子式为_______ ,用习惯命名法命名,戊的名称是_______ 。
(2)写出丁完全燃烧的化学方程式_______ 。
(3)甲与O2的反应可将化学能转化为电能,其工作原理如下图所示,图中甲从_______ (填A或B)通入,a极附近溶液pH将_______ (填升高,降低或不变),b极的电极反应式是_______

II.烃可以通过化学反应制得烃的衍生物,例如由丙烯可以制得丙烯酸(CH2=CHCOOH)、乳酸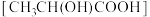 等。
等。
(4)乳酸中官能团的名称是_______ 。
(5)丙烯酸可以使酸性高锰酸钾溶液褪色,该反应类型为_______ 。
(6)3.6g乳酸与足量钠反应,能生成标准状况下H2的体积为_______ L。
(7)如下图所示的物质含有_______ 个碳原子。

I.某些烃分子的模型如图所示:

回答下列问题:
(1)乙的分子式为
(2)写出丁完全燃烧的化学方程式
(3)甲与O2的反应可将化学能转化为电能,其工作原理如下图所示,图中甲从

II.烃可以通过化学反应制得烃的衍生物,例如由丙烯可以制得丙烯酸(CH2=CHCOOH)、乳酸
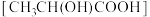 等。
等。(4)乳酸中官能团的名称是
(5)丙烯酸可以使酸性高锰酸钾溶液褪色,该反应类型为
(6)3.6g乳酸与足量钠反应,能生成标准状况下H2的体积为
(7)如下图所示的物质含有

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】写出下列物质的结构式
①CH4_____________ ② NH3__________ ③ Cl2_____________
①CH4
您最近一年使用:0次




