回答下列问题:
(1)锂和镁在元素周期表中有特殊“对角线”关系,它们的性质相似。下列有关锂及其化合物的叙述不正确的是___ 。
A.Li2SO4难溶于水
B.Li与N2反应产物是Li3N
C.LiOH难溶于水
D.LiOH与Li2CO3受热都易分解
(2)与铝位于对角线位置的第二周期元素是Be,能区别Be(OH)2和Mg(OH)2的一种试剂是___ ,反应的离子方程式为___ 。
(3)门捷列夫在研究元素周期表时,科学地预言了11种尚未发现的元素,为它们在周期表中留下空位。例如,他预测在铝的下方有一个与铝类似的元素“类铝”,后来被法国化学家于1875年发现,命名为镓。它在周期表中的位置是___ 。
(4)关于与镓同主族的第六周期元素性质的推测中不正确的是___ 。
A.单质是银白色较软的金属
B.其氢氧化物是两性氢氧化物
C.在化合物中显+3价
D.单质与盐酸的反应比铝剧烈
(5)写出短周期主族元素中原子半径最大的原子的单质在空气中加热条件下反应产物的电子式___ 。
(1)锂和镁在元素周期表中有特殊“对角线”关系,它们的性质相似。下列有关锂及其化合物的叙述不正确的是
A.Li2SO4难溶于水
B.Li与N2反应产物是Li3N
C.LiOH难溶于水
D.LiOH与Li2CO3受热都易分解
(2)与铝位于对角线位置的第二周期元素是Be,能区别Be(OH)2和Mg(OH)2的一种试剂是
(3)门捷列夫在研究元素周期表时,科学地预言了11种尚未发现的元素,为它们在周期表中留下空位。例如,他预测在铝的下方有一个与铝类似的元素“类铝”,后来被法国化学家于1875年发现,命名为镓。它在周期表中的位置是
(4)关于与镓同主族的第六周期元素性质的推测中不正确的是
A.单质是银白色较软的金属
B.其氢氧化物是两性氢氧化物
C.在化合物中显+3价
D.单质与盐酸的反应比铝剧烈
(5)写出短周期主族元素中原子半径最大的原子的单质在空气中加热条件下反应产物的电子式
19-20高一下·四川广安·开学考试 查看更多[2]
更新时间:2020-04-17 20:10:51
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】钠是一种非常活泼、具有广泛应用的金属。回答下列问题:
(1)钠原子的结构示意图为________ ,在化学反应中容易________ (填“得到”或“失去”)电子。
(2)钠的一种常见淡黄色氧化物,常用作呼吸面具的供氧剂。该物质与 反应的化学反应方程式为
反应的化学反应方程式为________ 。
(3)观察法也是学习化学的重要方法,金属钠放置在空气中观察到下列现象。
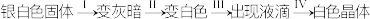
①反应I后固体变灰暗,该固体的化学式为________ ,将少量灰暗色固体投入 溶液中,观察到的实验现象为
溶液中,观察到的实验现象为________ 。
②反应II后得到的固体为NaOH,NaOH在水中的电离方程式为________ 。
③下列属于白色晶体用途的是________ (填字母)。
A.制肥皂 B.造纸 C.烘焙蛋糕 D.用于治疗胃酸过多症
(1)钠原子的结构示意图为
(2)钠的一种常见淡黄色氧化物,常用作呼吸面具的供氧剂。该物质与
 反应的化学反应方程式为
反应的化学反应方程式为(3)观察法也是学习化学的重要方法,金属钠放置在空气中观察到下列现象。
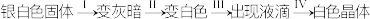
①反应I后固体变灰暗,该固体的化学式为
 溶液中,观察到的实验现象为
溶液中,观察到的实验现象为②反应II后得到的固体为NaOH,NaOH在水中的电离方程式为
③下列属于白色晶体用途的是
A.制肥皂 B.造纸 C.烘焙蛋糕 D.用于治疗胃酸过多症
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】 用途广泛,可用于医药、印染、漂白及用作分析试剂等。实验室模拟工业制备
用途广泛,可用于医药、印染、漂白及用作分析试剂等。实验室模拟工业制备 并检验其纯度的实验流程如图所示。
并检验其纯度的实验流程如图所示。

回答下列问题:
(1)生成 的化学方程式为
的化学方程式为_______ 。钠在空气中燃烧现象为_______ 。
(2)样液中加入 后产生一种无色无味的气体单质,该气体的名称为
后产生一种无色无味的气体单质,该气体的名称为_______ 。
(3)写出 与
与 反应的方程式
反应的方程式_______ 。已知白色沉淀为 ,说明
,说明 样品中含有杂质,为防止杂质的生成需对空气进行预处理,预处理的措施是
样品中含有杂质,为防止杂质的生成需对空气进行预处理,预处理的措施是_______ 。
 用途广泛,可用于医药、印染、漂白及用作分析试剂等。实验室模拟工业制备
用途广泛,可用于医药、印染、漂白及用作分析试剂等。实验室模拟工业制备 并检验其纯度的实验流程如图所示。
并检验其纯度的实验流程如图所示。
回答下列问题:
(1)生成
 的化学方程式为
的化学方程式为(2)样液中加入
 后产生一种无色无味的气体单质,该气体的名称为
后产生一种无色无味的气体单质,该气体的名称为(3)写出
 与
与 反应的方程式
反应的方程式 ,说明
,说明 样品中含有杂质,为防止杂质的生成需对空气进行预处理,预处理的措施是
样品中含有杂质,为防止杂质的生成需对空气进行预处理,预处理的措施是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】某课外实验小组从煤油中取出一块钠,用滤纸吸干其表面的煤油,用刀切下数块,分别进行实验研究。
(1)钠块切面处迅速变暗,反应的化学方程式为_______ 。
(2)将一小块钠放入坩埚中加热,反应的化学方程式为_______ 。
(3)将加热过的一小块钠放入盛有氯气的集气瓶中,反应的化学方程式为_______ 。
(4)将一小块Na投入到盛有适量水的烧杯中,反应的化学方程式为_______ 。反应放出大量热,依据的现象是_______ 。
(5)将一小块Na投入到盛有适量硫酸铜溶液的烧杯中,观察到溶液中出现蓝色沉淀,写出产生蓝色沉淀的化学方程式_______ 。
(1)钠块切面处迅速变暗,反应的化学方程式为
(2)将一小块钠放入坩埚中加热,反应的化学方程式为
(3)将加热过的一小块钠放入盛有氯气的集气瓶中,反应的化学方程式为
(4)将一小块Na投入到盛有适量水的烧杯中,反应的化学方程式为
(5)将一小块Na投入到盛有适量硫酸铜溶液的烧杯中,观察到溶液中出现蓝色沉淀,写出产生蓝色沉淀的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】根据周期表对角线原则,金属Be与铝单质及其化合物的性质相似,又知AlCl3熔、沸点较低,易升华,试回答下列问题:
(1)写出Be与NaOH溶液反应的离子方程式_________ 。Be2+、Li+、H+ 微粒半径从小到大的顺序为:______ ;
(2)Be(OH)2和Mg(OH)2可用试剂______ 鉴别;其离子方程式为____________ 。
(3)BeCl2是______ (填“离子化合物”或“共价化合物”), BeCl2水溶液呈酸性,水解的离子方程式为__________ 。
(1)写出Be与NaOH溶液反应的离子方程式
(2)Be(OH)2和Mg(OH)2可用试剂
(3)BeCl2是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】氨硼烷(NH3BH3)含氢量高、热稳定性好,是一种具有潜力的固体储氢材料。回答下列问题:
(1)H、B、N中,原子半径最大的是_______ 。根据对角线规则,B的一些化学性质与元素_______ 的相似。
(2)NH3BH3分子中,N-B化学键称为_______ 键,其电子对由_______ 提供。
(3)NH3BH3分子中,与N原子相连的H呈正电性(Hδ+),与B原子相连的H呈负电性(Hδ-),电负性从大到小顺序是_______ 。与NH3BH3原子总数相等的等电子体是_______ (写分子式)。
(1)H、B、N中,原子半径最大的是
(2)NH3BH3分子中,N-B化学键称为
(3)NH3BH3分子中,与N原子相连的H呈正电性(Hδ+),与B原子相连的H呈负电性(Hδ-),电负性从大到小顺序是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】下图是元素周期表的一部分
(1)元素⑩原子结构示意图为____________ 。
(2)元素③④⑤的电负性由大到小的顺序为____________ (填化学用语,下同),其简单离子半径由大到小的顺序为_______________ 。⑤与⑧气态氢化物中稳定性较强的是________ 。
(3)某些不同族元素的性质也有一定的相似性,如上表中元素⑦与元素②的单质及其化合物有相似的性质。写出元素②的最高价氧化物与NaOH溶液反应的离子方程式___________________________________________________________ 。
(4)根据下列五种元素的第一至第四电离能数据(单位:kJ·mol-1),回答下面各题:
①在周期表中,最可能处于同一主族的是____________ 。(填元素代号)
②T元素最可能是______ (填“s”、“p”、“d”、“ds”等)区元素;若T为第二周期元素,Z是第三周期元素中原子半径最小的主族元素,则T、Z形成的化合物分子键角为________ 。
(5)金刚砂(SiC)的结构与金刚石相似,硬度与金刚石相当,则金刚砂的晶胞中含有________ 个硅原子,________ 个碳原子,其中硅原子的杂化方式为________ 。
| ① | |||||||||||||||||
| ② | ③ | ④ | ⑤ | ||||||||||||||
| ⑥ | ⑦ | ⑧ | |||||||||||||||
| ⑨ | ⑩ |
(1)元素⑩原子结构示意图为
(2)元素③④⑤的电负性由大到小的顺序为
(3)某些不同族元素的性质也有一定的相似性,如上表中元素⑦与元素②的单质及其化合物有相似的性质。写出元素②的最高价氧化物与NaOH溶液反应的离子方程式
(4)根据下列五种元素的第一至第四电离能数据(单位:kJ·mol-1),回答下面各题:
| 元素代号 | I1 | I2 | I3 | I4 |
| Q | 2080 | 4000 | 6100 | 9400 |
| R | 500 | 4600 | 6900 | 9500 |
| S | 740 | 1500 | 7700 | 10500 |
| T | 580 | 1800 | 2700 | 11600 |
| U | 420 | 3100 | 4400 | 5900 |
①在周期表中,最可能处于同一主族的是
②T元素最可能是
(5)金刚砂(SiC)的结构与金刚石相似,硬度与金刚石相当,则金刚砂的晶胞中含有
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】氮、磷、砷(As)、锑(Sb)、铋(Bi)、镆(Mc)为元素周期表中原子序数依次增大的同族元素。回答下列问题:
(1)N2的电子式为___________
(2)砷在元素周期表中的位置___________ ,
(3)2017年5月9日,中国科学院发布了113号、115号、117号及118号四种元素的中文名称,其中镆元素的“镆”取自古代剑名“镆铘”,Mc的质子数为___________ 。
(4)已知:含1molP原子的白磷转化为黑磷要放出39.3kJ的能量;转化为红磷要放出17.6kJ的能量;由此推知,其中最稳定的磷单质是___________ 。(填物质名称)
(5)氮和磷氢化物性质的比较:热稳定性:NH3___________ PH3(填“>”或“<”),沸点:N2H4___________ P2H4(填“>”或“<”)
(6)PH3和NH3与卤化氢的反应相似,产物的结构和性质也相似,写出PH3与HI反应产物的电子式___________ 。
(1)N2的电子式为
(2)砷在元素周期表中的位置
(3)2017年5月9日,中国科学院发布了113号、115号、117号及118号四种元素的中文名称,其中镆元素的“镆”取自古代剑名“镆铘”,Mc的质子数为
(4)已知:含1molP原子的白磷转化为黑磷要放出39.3kJ的能量;转化为红磷要放出17.6kJ的能量;由此推知,其中最稳定的磷单质是
(5)氮和磷氢化物性质的比较:热稳定性:NH3
(6)PH3和NH3与卤化氢的反应相似,产物的结构和性质也相似,写出PH3与HI反应产物的电子式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】金属镓(Ga)应用广泛,在半导体和光电材料、合金、磁性材料等领域都有重要应用。镓与铝是同主族元素,性质相似。
(1)铝在元素周期表中的位置是_________ 。
(2)GaAs 是一种重要的半导体材料。As 与 Ga 同周期,As 与 N 同主族。
①下列事实不能用元素周期律解释的是___________ (填字母)。
a. 碱性:Ga (OH)3> Al (OH)3 b. 非金属性:As>Ga c. 酸性:H3AsO4>H3AsO3
②GaAs 中,As 元素化合价为-3 价,用原子结构理论解释原因_________________ 。
③废弃含 GaAs 半导体材料可以用浓硝酸溶解 GaAs,生成 H3AsO4和 Ga3+,写出该反应的化学方程式_________ 。
(3)工业上获取镓的方法之一是从闪锌矿冶锌后的残渣(主要含有 Zn、Pb、Fe、Ga 等元素)中提取,某科研单位设计下述流程提取镓,已知:Ga 在碱性溶液中以[Ga(OH)4]- 形式存在。
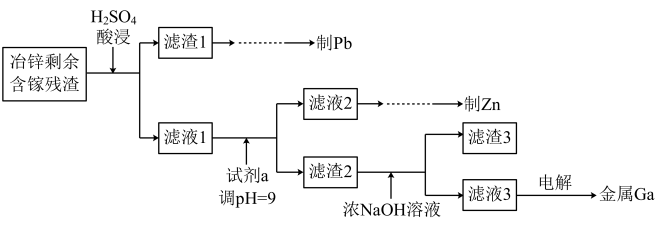
①试剂 a 是_____ 。
②写出得到滤液 3 的离子方程式_______________ 。
③写出电解制镓时的阴极电极反应式__________________ 。
(1)铝在元素周期表中的位置是
(2)GaAs 是一种重要的半导体材料。As 与 Ga 同周期,As 与 N 同主族。
①下列事实不能用元素周期律解释的是
a. 碱性:Ga (OH)3> Al (OH)3 b. 非金属性:As>Ga c. 酸性:H3AsO4>H3AsO3
②GaAs 中,As 元素化合价为-3 价,用原子结构理论解释原因
③废弃含 GaAs 半导体材料可以用浓硝酸溶解 GaAs,生成 H3AsO4和 Ga3+,写出该反应的化学方程式
(3)工业上获取镓的方法之一是从闪锌矿冶锌后的残渣(主要含有 Zn、Pb、Fe、Ga 等元素)中提取,某科研单位设计下述流程提取镓,已知:Ga 在碱性溶液中以[Ga(OH)4]- 形式存在。

①试剂 a 是
②写出得到滤液 3 的离子方程式
③写出电解制镓时的阴极电极反应式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】下表是ⅥA族部分元素的相关性质。
请回答下列问题:
(1)硒的熔点范围可能是______________________ 。
(2)碲的化合价可能有______________________ 。
(3)硫、硒、碲的氢化物水溶液的酸性由强至弱的顺序是________ (填化学式)。
(4)氢硒酸有较强的________ (填“氧化性”或“还原性”),因此放在空气中易变质,其可能发生的化学方程式为_______________________________________ 。
(5)工业上Al2Te3可用来制备H2Te,完成下列化学方程式:
________ Al2Te3+( ) ===2Al(OH)3↓+________ H2Te↑
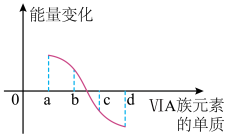
(6)氧族元素单质与H2反应过程中的能量变化如图所示,其中a、b、c、d分别表示氧族中某一元素的单质。则b代表________ ,d代表________ (均写单质名称)。
元素 性质 | 8O | 16S | 34Se | 52Te |
| 单质熔点(℃) | -218.4 | 113 | 450 | |
| 单质沸点(℃) | -183 | 444.6 | 685 | 1 390 |
| 主要化合价 | -2 | -2、+4、+6 | -2、+4、+6 | |
| 原子半径 | 逐渐增大 | |||
| 单质与H2反应情况 | 点燃时易化合 | 加热 化合 | 加热 难化合 | 不能直 接化合 |
请回答下列问题:
(1)硒的熔点范围可能是
(2)碲的化合价可能有
(3)硫、硒、碲的氢化物水溶液的酸性由强至弱的顺序是
(4)氢硒酸有较强的
(5)工业上Al2Te3可用来制备H2Te,完成下列化学方程式:
(6)氧族元素单质与H2反应过程中的能量变化如图所示,其中a、b、c、d分别表示氧族中某一元素的单质。则b代表

您最近一年使用:0次



