下列有关金属元素特征的叙述正确的是( )
| A.金属元素的原子只有还原性,离子只有氧化性 |
| B.金属元素在一般化合物中只显正价 |
| C.金属元素在不同的化合物中的化合价均不同 |
| D.金属元素的单质在常温下均为金属晶体 |
更新时间:2020-01-08 09:19:40
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】在空气中能发生致密氧化膜保护金属本身不再被腐蚀的是
| A.金 | B.铁 | C.铝 | D.钠 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列有关金属及其化合物的说法正确的是
| A.Na久置于空气中最终生成NaHCO3 |
| B.金属单质在化学反应中往往体现出还原性 |
| C.金属元素在自然界中都是以化合态形式存在的 |
| D.Mg比Al活泼,更易与NaOH溶液反应生成H2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】草酸钴晶体是制备钴的氧化物的重要原料。18.3g草酸钴晶体(CoC2O4·2H2O)在隔绝空气受热时的质量变化曲线如图所示,240℃及以上所得固体均为钴氧化物(其中Co的化合价为+2或+3)。下列说法正确的是


| A.到A点时草酸钴晶体失去2个H2O |
| B.C点剩余固体的化学成分为Co3O4 |
C.若B点时通入氧气,则会发生反应3CoC2O4+2O2 Co3O4+6CO2 Co3O4+6CO2 |
D.C点到D点发生反应的化学方程式为CoCO3 CoO+CO2↑ CoO+CO2↑ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】我国科学家合成一种超强酸 M(结构如图所示),可广泛应用于有机合成,其中 R、X、Y、Z、W 为原子序数依次增大的短周期主族元素,Y 和 W 位于同族,下列说法正确的是
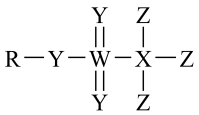
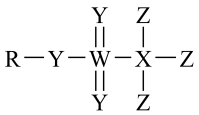
| A.化合物 WY2是一种直线形分子 |
| B.不考虑端位原子,M 中 Y、W、X 三种原子采用的杂化方式均不相同 |
| C.M 中含有极性键、非极性键 |
| D.将 M 中 Z 元素替换为短周期同主族其他元素,M 酸性减弱 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】现有四种短周期元素的原子半径及主要化合价数据如下表所示:
下列叙述不正确的是( )
| 元素 | 甲 | 乙 | 丙 | 丁 |
| 原子半径/nm | 0.186 | 0.102 | 0.152 | 0.074 |
| 主要化合价 | +1 | +6、-2 | +1 | -2 |
| A.甲单质的熔点比丙单质的熔点高 |
| B.甲单质可用电解其熔融盐的方法冶炼而得 |
| C.常温下,丁的两种氢化物均为液体 |
| D.乙的简单离子是四种元素各自形成的简单离子中半径最大的 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列表示不正确的是
A.次氯酸的电子式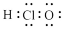 |
B.丁烷的球棍模型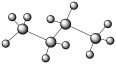 |
C.乙烯的结构简式 |
D. 离子核外有 离子核外有 个电子, 个电子, 原子质子数可表示为 原子质子数可表示为 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】利用某分子筛作催化剂, 可脱除废气中的NO和
可脱除废气中的NO和 ,生成两种无毒物质,其反应历程如图所示。下列说法正确的是
,生成两种无毒物质,其反应历程如图所示。下列说法正确的是

 可脱除废气中的NO和
可脱除废气中的NO和 ,生成两种无毒物质,其反应历程如图所示。下列说法正确的是
,生成两种无毒物质,其反应历程如图所示。下列说法正确的是
A.X是 和 和 |
B.上述历程的总反应为 |
C.过程①说明 不能用浓硫酸干燥,可用氯化钙干燥 不能用浓硫酸干燥,可用氯化钙干燥 |
D. 、 、 、 、 中的质子数、电子数均相同 中的质子数、电子数均相同 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】下列叙述正确的是
①熔点:Al>Na>K
②沸点:NH3<PH3<AsH3
③原子半径:C>N>O
④酸性:HNO3>H3PO4>H2SO4
⑤F-与Na+具有相同的电子层结构
⑥含有阳离子的物质一定含阴离子
⑦由于氢键的存在,热稳定性.:HF>H2O>H2S
①熔点:Al>Na>K
②沸点:NH3<PH3<AsH3
③原子半径:C>N>O
④酸性:HNO3>H3PO4>H2SO4
⑤F-与Na+具有相同的电子层结构
⑥含有阳离子的物质一定含阴离子
⑦由于氢键的存在,热稳定性.:HF>H2O>H2S
| A.①③⑤ | B.②⑤⑦ | C.③⑤⑥ | D.②④⑦ |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列有关性质的比较,不正确的是
A.晶体熔点: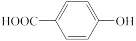 > >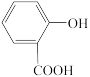 | B.硬度:金刚石>碳化硅>晶体硅 |
| C.晶体熔点:Na>Mg>Al | D.晶体熔点:NaF>NaCl>NaBr>NaI |
您最近一年使用:0次

 和
和 都可以与
都可以与 形成配位键
形成配位键 为三元酸,
为三元酸, 呈两性
呈两性

