下列叙述正确的是
①熔点:Al>Na>K
②沸点:NH3<PH3<AsH3
③原子半径:C>N>O
④酸性:HNO3>H3PO4>H2SO4
⑤F-与Na+具有相同的电子层结构
⑥含有阳离子的物质一定含阴离子
⑦由于氢键的存在,热稳定性.:HF>H2O>H2S
①熔点:Al>Na>K
②沸点:NH3<PH3<AsH3
③原子半径:C>N>O
④酸性:HNO3>H3PO4>H2SO4
⑤F-与Na+具有相同的电子层结构
⑥含有阳离子的物质一定含阴离子
⑦由于氢键的存在,热稳定性.:HF>H2O>H2S
| A.①③⑤ | B.②⑤⑦ | C.③⑤⑥ | D.②④⑦ |
更新时间:2020-08-03 22:56:54
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】下列叙述中,正确的是
| A.原子半径:Cl>S>O | B.还原性:Li>Na>K |
| C.稳定性:HF>HCl>HBr | D.酸性:HClO>H2SO4 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】元素周期表是元素周期律的具体表现形式,是学习化学的一种重要工具。过去,门捷列夫曾用元素周期律预言未知元素并得到了证实。下列关于元素周期律的叙述中不正确的是


| A.Na、Mg、Al最外层电子数依次增多,单核离子的氧化性依次增强 |
| B.P、S、Cl最高正化合价依次升高,对应气态氢化物的稳定性依次增强 |
| C.同周期元素的原子半径以VIIA族的为最大 |
| D.Na、Mg、Al的氢氧化物的碱性依次减弱 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】短周期元素W、X、Y、Z的原子序数依次增大。其中W的阴离子的核外电子数与X、Y、Z原子的核外内层电子数相同。X的一种核素在考古时常用来鉴定一些文物的年代,工业上采用液态空气分馏方法来生产Y的单质,而Z不能形成双原子分子。根据以上叙述,下列说法中一定正确的是( )
A.元素非金属性比较为: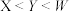 |
| B.W、X、Y、Z原子的核外最外层电子数的总和为20 |
| C.W与Y可形成既含极性共价键又含非极性共价键的化合物 |
| D.由W与X组成的化合物的沸点总低于由W与Y组成的化合物的沸点 |
您最近一年使用:0次
【推荐1】下列判断正确的是
| A.第一电离能:N>C>O |
B.沸点:邻羟基苯甲酸>对羟基苯甲酸(见图)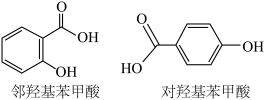 |
| C.甲烷分子中H-C-H键角大于氨气分子中H-N-H键角 |
| D.1 mol金刚石晶体和1 mol SiO2晶体存在的共价键数目相同 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】短周期主族元素X、Y、Z、W的原子序数依次增大,X、Y同周期并相邻,Y是组成水的元素之一,Z在同周期主族元素中金属性最强,W原子在同周期主族元素中原子半径最小,下列判断正确的是
| A.Z位于元素周期表的p区 | B.简单氢化物沸点:X>Y |
| C.Z与W形成的化合物是离子化合物 | D.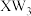 的空间构型与VSEPR构型一致 的空间构型与VSEPR构型一致 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】要使金属晶体熔化必须破坏其中的金属键。金属晶体熔、沸点高低和硬度大小一般取决于金属键的强弱。由此判断下列说法正确的是
| A.金属镁的熔点高于金属铝 |
| B.碱金属单质的熔、沸点从Li到Cs是逐渐升高的 |
| C.金属镁的硬度小于金属钙 |
| D.金属铝的硬度大于金属钠 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】主族元素X、Y、Z、M、N分布在前三个周期,其原子序数依次增大,其中Z是地壳中最多的元素,Y、M、N的最外层电子数之和为10,且Y的最外层电子数等于M和N的最外层电子数之和。下列说法正确的是
| A.X、Y、Z三种元素既可形成共价化合物,也可形成离子化合物 |
| B.原子半径:N > M > Z > Y > X |
| C.单质的熔点:M > N |
| D.简单氢化物的稳定性:Y > Z |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列因果关系成立的是
| A.因为金刚石C—C键能>晶体硅Si—Si键能,所以金刚石的熔沸点比晶体硅高 |
| B.因为M(I2)>M(Br2),所以分子间作用力I2>Br2,I2的化学性质比Br2稳定 |
| C.因为NaCl晶体中存在大量的阴、阳离子,所以NaCl晶体的导电性比Na强 |
| D.因为冰是固体,水是液体,所以冰的密度比水大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列物质性质的变化与化学键强弱无关的是
| A.HF、HCl、HBr、HI的热稳定性依次减弱 |
| B.NaF、NaCl、NaBr、NaI的熔点依次降低 |
| C.Li、Na、K、Rb 的熔点逐渐降低 |
| D.F2、C12、Br2、I2的熔、沸点逐渐升高 |
您最近一年使用:0次

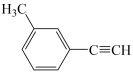 中共平面的原子数目最多为15个
中共平面的原子数目最多为15个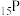 原子的核外电子排布式写成
原子的核外电子排布式写成 ,则违背了泡利原理
,则违背了泡利原理 、
、 、
、 、
、 、
、 的熔点依次降低
的熔点依次降低
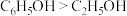

 的相对分子质量
的相对分子质量