现有KNO3样品(含有少量杂质KCl、K2SO4),选择适当的试剂除去杂质,从而得到纯净的KNO3晶体,相应的实验流程如图所示。
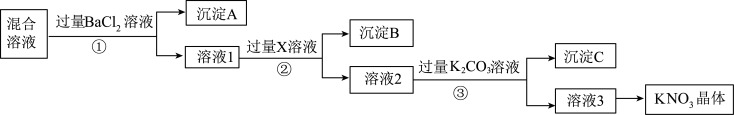
请回答下列问题:
(1)写出实验流程中下列物质的化学式:试剂X__ ,沉淀C__ 、__ 。
(2)上述实验流程中①②③步均要进行的实验操作是__ (填操作名称)。
(3)生成沉淀A的离子方程式是__ 。
(4)此实验方案存在缺陷,还应__ ,之后若要获得纯净的KNO3晶体,需进行的实验操作是__ 、__ (填操作名称)。

请回答下列问题:
(1)写出实验流程中下列物质的化学式:试剂X
(2)上述实验流程中①②③步均要进行的实验操作是
(3)生成沉淀A的离子方程式是
(4)此实验方案存在缺陷,还应
更新时间:2020-01-09 18:11:25
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
【推荐1】离子反应广泛用于化学研究、工业生产、食品检验、环境保护等方面。
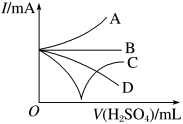
(1)向0.01mol·L-1 Ba(OH)2溶液中匀速逐滴加入0.01mol·L-1 H2SO4溶液直至过量,整个过程中混合溶液的导电能力(用I表示)可近似地用下图中的____________ (填字母)曲线表示,发生反应的离子方程式为__________________________________ 。
(2)提纯后的粗盐中,还含有MgCl2、Na2SO4和CaCl2等可溶性杂质,欲通过下列流程得到较纯净的NaCl固体。
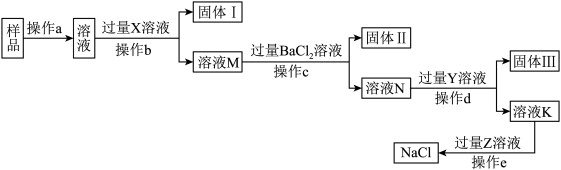
①操作a、操作d均用到玻璃棒,作用分别是____________ 、____________ 。
②固体Ⅲ是________ (填化学式),加入过量Z溶液的目的是________________ 。
③操作e的名称是____________________ 。
④检验制得的NaCl晶体中是否含有Na2SO4的方法是__________________ 。
(1)向0.01mol·L-1 Ba(OH)2溶液中匀速逐滴加入0.01mol·L-1 H2SO4溶液直至过量,整个过程中混合溶液的导电能力(用I表示)可近似地用下图中的

(2)提纯后的粗盐中,还含有MgCl2、Na2SO4和CaCl2等可溶性杂质,欲通过下列流程得到较纯净的NaCl固体。

①操作a、操作d均用到玻璃棒,作用分别是
②固体Ⅲ是
③操作e的名称是
④检验制得的NaCl晶体中是否含有Na2SO4的方法是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】Ⅰ.用零价铁(Fe)去除水体中的硝酸盐( )已成为环境修复研究的热点之一。
)已成为环境修复研究的热点之一。
(1)Fe还原水体中 的反应原理如图所示。
的反应原理如图所示。
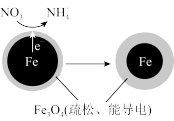
正极的电极反应式是_______ 。
(2)将足量铁粉投入水体中,经24小时测定 的去除率和pH,结果如下:
的去除率和pH,结果如下:
pH=4.5时, 的去除率低。其原因是
的去除率低。其原因是_______ 。
(3)实验发现:在初始pH=4.5的水体中投入足量铁粉的同时,补充一定量的Fe2+可以明显提高 的去除率。对Fe2+的作用提出两种假设:
的去除率。对Fe2+的作用提出两种假设:
Ⅰ.Fe2+直接还原 ;Ⅱ.Fe2+破坏FeO(OH)氧化层。
;Ⅱ.Fe2+破坏FeO(OH)氧化层。
① 对比实验,结果如图所示,可得到的结论是_______ 。

②同位素示踪法证实Fe2+能与FeO(OH)反应生成Fe3O4。结合该反应的离子方程式,解释加入Fe2+提高 去除率的原因:
去除率的原因:_______ 。
II.高铁酸钠Na2FeO4是一种新型净水剂。
(4)高铁酸钠主要通过如下反应制取:2Fe(OH)3+3NaClO+4NaOH= 2Na2FeO4+3X+5H2O,则X的化学式为_______ 。
(5)高铁酸钠具有强氧化性,与水反应生成Fe(OH)3胶体能够吸附水中悬浮杂质,请写出高铁酸钠与水反应的离子方程式_______ 。
 )已成为环境修复研究的热点之一。
)已成为环境修复研究的热点之一。(1)Fe还原水体中
 的反应原理如图所示。
的反应原理如图所示。
正极的电极反应式是
(2)将足量铁粉投入水体中,经24小时测定
 的去除率和pH,结果如下:
的去除率和pH,结果如下:| 初始pH | pH=2.5 | pH=4.5 |
 的去除率 的去除率 | 接近100% | <50% |
| 24小时pH | 接近中性 | 接近中性 |
| 铁的最终物质形态 | 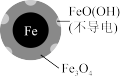 |  |
 的去除率低。其原因是
的去除率低。其原因是(3)实验发现:在初始pH=4.5的水体中投入足量铁粉的同时,补充一定量的Fe2+可以明显提高
 的去除率。对Fe2+的作用提出两种假设:
的去除率。对Fe2+的作用提出两种假设:Ⅰ.Fe2+直接还原
 ;Ⅱ.Fe2+破坏FeO(OH)氧化层。
;Ⅱ.Fe2+破坏FeO(OH)氧化层。① 对比实验,结果如图所示,可得到的结论是

②同位素示踪法证实Fe2+能与FeO(OH)反应生成Fe3O4。结合该反应的离子方程式,解释加入Fe2+提高
 去除率的原因:
去除率的原因:II.高铁酸钠Na2FeO4是一种新型净水剂。
(4)高铁酸钠主要通过如下反应制取:2Fe(OH)3+3NaClO+4NaOH= 2Na2FeO4+3X+5H2O,则X的化学式为
(5)高铁酸钠具有强氧化性,与水反应生成Fe(OH)3胶体能够吸附水中悬浮杂质,请写出高铁酸钠与水反应的离子方程式
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】高氯酸是一种酸性极强的无机含氧酸,可用于制备高氯酸盐、人造金刚石提纯等方面。查阅资料得到以下有关高氯酸的信息:
工业上生产高氯酸的同时还生产了亚氯酸钠,工业流程如下:
(1)操作①的名称是____________ ,操作②的名称是___________ 。
(2)反应器Ⅰ中发生反应的化学方程式为________________________ 。
(3)反应器Ⅱ中发生反应的离子方程式为__________________________ 。
(4)若反应器Ⅱ中SO2以H2O2代替也可达到同样的目,此时发生反应的离子方程式为___________ 。
(5)若想得到201 kg的 HClO4纯品,至少需要NaClO3_________ kg。
(6)工业上也可用铂作阳极、铜作阴极电解盐酸制得高氯酸,在阳极区可得到20%的高氯酸。写出阳极的电极反应式(其中盐酸与高氯酸以化学式出现)______________________________ 。
名称 | 分子式 | 外观 | 沸点 |
高氯酸 | HClO4 | 无色液体 | 130℃ |
工业上生产高氯酸的同时还生产了亚氯酸钠,工业流程如下:
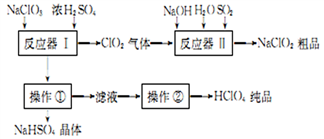
(1)操作①的名称是
(2)反应器Ⅰ中发生反应的化学方程式为
(3)反应器Ⅱ中发生反应的离子方程式为
(4)若反应器Ⅱ中SO2以H2O2代替也可达到同样的目,此时发生反应的离子方程式为
(5)若想得到201 kg的 HClO4纯品,至少需要NaClO3
(6)工业上也可用铂作阳极、铜作阴极电解盐酸制得高氯酸,在阳极区可得到20%的高氯酸。写出阳极的电极反应式(其中盐酸与高氯酸以化学式出现)
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】氯碱厂电解饱和食盐水制取NaOH的工艺流程示意图如下,请完成相关填空。

依据上图,完成下列填空:
(1)在电解过程中,与电源负极相连的电极附近,溶液pH_____ (选填“不变”“升高”或“下降”)。
(2)工业食盐含CaCl2、MgCl2等杂质。精制过程发生反应的化学方程式_____ 、_____ 。
(3)如果粗盐中 含量较高,必须添加钡试剂除去
含量较高,必须添加钡试剂除去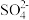 ,该钡试剂可以是
,该钡试剂可以是_____ 。
a、Ba(OH)2 b、Ba(NO3)2 c、BaCl2
(4)为有效除去Ca2+、Mg2+、 ,加入试剂的合理顺序为
,加入试剂的合理顺序为_______ 。
a、先加NaOH,后加Na2CO3,再加钡试剂
b、先加NaOH,后加钡试剂,再加稀盐酸,最后加Na2CO3
c、先加钡试剂,后加NaOH,再加Na2CO3,最后加稀盐酸
(5)脱盐工序中利用NaOH和NaCl在溶解度上的差异,通过_____ 、冷却结晶、_____ (填写操作名称)洗涤、烘干除去NaCl。

依据上图,完成下列填空:
(1)在电解过程中,与电源负极相连的电极附近,溶液pH
(2)工业食盐含CaCl2、MgCl2等杂质。精制过程发生反应的化学方程式
(3)如果粗盐中
 含量较高,必须添加钡试剂除去
含量较高,必须添加钡试剂除去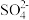 ,该钡试剂可以是
,该钡试剂可以是a、Ba(OH)2 b、Ba(NO3)2 c、BaCl2
(4)为有效除去Ca2+、Mg2+、
 ,加入试剂的合理顺序为
,加入试剂的合理顺序为a、先加NaOH,后加Na2CO3,再加钡试剂
b、先加NaOH,后加钡试剂,再加稀盐酸,最后加Na2CO3
c、先加钡试剂,后加NaOH,再加Na2CO3,最后加稀盐酸
(5)脱盐工序中利用NaOH和NaCl在溶解度上的差异,通过
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】现有含有少量NaCl、 Na2SO4、Na2CO3等杂质的NaNO3溶液,选择适当的试剂除去杂质,得到纯净的NaNO3固体,实验流程如下图所示。
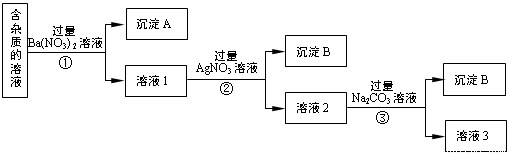
(1)沉淀A的主要成分是___________ 、___________ (填化学式)。
(2)①②③中均进行的分离操作是___________ 。
(3)溶液3经过处理可以得到NaNO3固体,溶液3中肯定含有的杂质是___________ ,为了除去杂质,可向溶液3中加入适量的___________ 。
(4)实验探究小组在实验中需要用到456 mL1 mol•L-1的HNO3溶液,但是在实验室中只发现一瓶8 mol•L-1的HNO3溶液,该小组用8mol•L-1的HNO3溶液配制所需溶液。
①实验中所需的玻璃仪器包括___________ 、量筒、烧杯、___________ 、胶头滴管等。
②下列实验操作中导致配制的溶液浓度偏高的是___________ 。
A.取用8mol•L-1的HNO3溶液溶液时仰视量筒刻度线
B.量取用的量筒水洗后未进行任何操作
C.8mol•L-1的HNO3溶液从量筒转移至烧杯后用水洗涤量筒并全部转移至烧杯
D.定容时仰视刻度线
③该实验中需要量取8mol•L-1的HNO3溶液___________ mL。

(1)沉淀A的主要成分是
(2)①②③中均进行的分离操作是
(3)溶液3经过处理可以得到NaNO3固体,溶液3中肯定含有的杂质是
(4)实验探究小组在实验中需要用到456 mL1 mol•L-1的HNO3溶液,但是在实验室中只发现一瓶8 mol•L-1的HNO3溶液,该小组用8mol•L-1的HNO3溶液配制所需溶液。
①实验中所需的玻璃仪器包括
②下列实验操作中导致配制的溶液浓度偏高的是
A.取用8mol•L-1的HNO3溶液溶液时仰视量筒刻度线
B.量取用的量筒水洗后未进行任何操作
C.8mol•L-1的HNO3溶液从量筒转移至烧杯后用水洗涤量筒并全部转移至烧杯
D.定容时仰视刻度线
③该实验中需要量取8mol•L-1的HNO3溶液
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】氯化钠可用于食品、制药、氯碱工业等许多领域。实验室中利用下列装置从海水提取纯净的氯化钠。海水中主要离子及浓度见下表:

回答下列问题:
(1)盛放 溶液的仪器名称为
溶液的仪器名称为_______ 。
(2)在95℃下对30mL海水进行加热搅拌,同时缓慢滴加约2mLlmol·L-1BaCl2溶液,加热10min后取下,确定沉淀完全的实验方法是_______ ,能否_______ (填“能”或“否”)用 代替
代替 做沉淀剂。
做沉淀剂。
(3)减压过滤(第一次)出泥沙与 ,加热滤液至沸,分别加入2mL3mol·L-1NaOH溶液和2mL饱和
,加热滤液至沸,分别加入2mL3mol·L-1NaOH溶液和2mL饱和 溶液,10min后减压过滤(第二次)。进行两次过滤而不是合并一次过滤的主要目的是:①防止泥沙溶于NaOH溶液;②防止发生沉淀转化
溶液,10min后减压过滤(第二次)。进行两次过滤而不是合并一次过滤的主要目的是:①防止泥沙溶于NaOH溶液;②防止发生沉淀转化_______ (写出离子方程式)。工业上不宜选择用 同时除去
同时除去 和
和 ,可能的合理考虑是
,可能的合理考虑是_______ (填序号),
A. 价格较高 B.
价格较高 B.  的溶解度比较低
的溶解度比较低
C. 属于二元强碱 D.
属于二元强碱 D.  恰好沉淀完全时,
恰好沉淀完全时, 不能完全沉淀
不能完全沉淀
(4)在滤液中滴加2mol·L-1盐酸,直至溶液pH在2~3之间,搅拌。有人认为调节溶液酸碱性呈中性即可,这样做的后果是_______ 。
| 离子 | Cl- | Na+ | Mg2+ | SO42- | Ca2+ | K+ |
| 浓度(×10-3mol/L) | 546 | 468 | 53.3 | 28.1 | 10.4 | 9.97 |

回答下列问题:
(1)盛放
 溶液的仪器名称为
溶液的仪器名称为(2)在95℃下对30mL海水进行加热搅拌,同时缓慢滴加约2mLlmol·L-1BaCl2溶液,加热10min后取下,确定沉淀完全的实验方法是
 代替
代替 做沉淀剂。
做沉淀剂。(3)减压过滤(第一次)出泥沙与
 ,加热滤液至沸,分别加入2mL3mol·L-1NaOH溶液和2mL饱和
,加热滤液至沸,分别加入2mL3mol·L-1NaOH溶液和2mL饱和 溶液,10min后减压过滤(第二次)。进行两次过滤而不是合并一次过滤的主要目的是:①防止泥沙溶于NaOH溶液;②防止发生沉淀转化
溶液,10min后减压过滤(第二次)。进行两次过滤而不是合并一次过滤的主要目的是:①防止泥沙溶于NaOH溶液;②防止发生沉淀转化 同时除去
同时除去 和
和 ,可能的合理考虑是
,可能的合理考虑是A.
 价格较高 B.
价格较高 B.  的溶解度比较低
的溶解度比较低C.
 属于二元强碱 D.
属于二元强碱 D.  恰好沉淀完全时,
恰好沉淀完全时, 不能完全沉淀
不能完全沉淀(4)在滤液中滴加2mol·L-1盐酸,直至溶液pH在2~3之间,搅拌。有人认为调节溶液酸碱性呈中性即可,这样做的后果是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】钴及其化合物广泛应用于航天、电池、磁性合金等高科技领域,我国钴资源贫乏,再生钴资源的回收利用是解决钴资源供给的重要途径。一种利用含钴废料(主要成分为 ,含少量
,含少量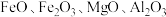 、有机物)制取
、有机物)制取 的工艺流程如图:
的工艺流程如图: ,回答下列问题:
,回答下列问题:
(1)“焙烧”的主要目的是_______ 。
(2)“浸取”过程中 发生反应的离子方程式为
发生反应的离子方程式为_______ 。
(3)“沉淀”时先加入 溶液,
溶液, 的作用主要是
的作用主要是_______ ;再加入 溶液调节
溶液调节 为5.0,此时滤液中的
为5.0,此时滤液中的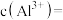
_______  。
。
(4)“萃取”用到的玻璃仪器主要有_______ 、烧杯,萃取原理可表述为: (水层)
(水层) (有机层)
(有机层)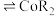 (有机层)
(有机层) (水层)。已知
(水层)。已知 萃取率随
萃取率随 变化如图所示,分析其变化原因
变化如图所示,分析其变化原因_______ 。水相中含有的阳离子有_______ 。 ,反应的离子方程式为
,反应的离子方程式为_______ 。
 ,含少量
,含少量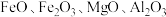 、有机物)制取
、有机物)制取 的工艺流程如图:
的工艺流程如图: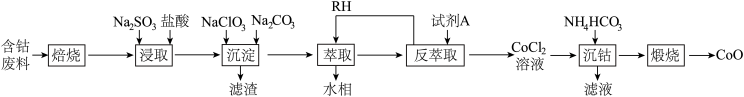
 ,回答下列问题:
,回答下列问题:| 金属离子 |  |  |  |  |  |
开始沉淀 的 的 | 7.5 | 1.8 | 3.4 | 9.1 | 6.5 |
沉淀完全 的 的 | 9.5 | 3.2 | 4.7 | 11.1 | 8.5 |
(1)“焙烧”的主要目的是
(2)“浸取”过程中
 发生反应的离子方程式为
发生反应的离子方程式为(3)“沉淀”时先加入
 溶液,
溶液, 的作用主要是
的作用主要是 溶液调节
溶液调节 为5.0,此时滤液中的
为5.0,此时滤液中的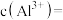
 。
。(4)“萃取”用到的玻璃仪器主要有
 (水层)
(水层) (有机层)
(有机层)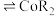 (有机层)
(有机层) (水层)。已知
(水层)。已知 萃取率随
萃取率随 变化如图所示,分析其变化原因
变化如图所示,分析其变化原因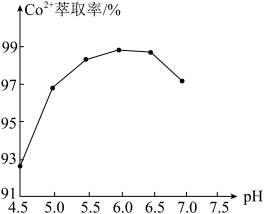
 ,反应的离子方程式为
,反应的离子方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】对于混合物的分离或提纯,常采用的方法有:过滤、蒸发、蒸馏、萃取、洗气、加热分解等。下列各组混和物的分离或提纯应采用什么方法?
①实验室中的石灰水久置,液面上常悬浮有CaCO3微粒。可用____ 的方法除去Ca(OH)2溶液中悬浮的CaCO3微粒。
②除去H2中的CO2,可用____ 的方法除去。
③粗盐中含有不溶性的泥沙、可溶性的氯化钙、氯化镁及一些硫酸盐.要将粗盐提纯,可先将粗盐溶解,按一定的顺序加入沉淀剂,再___ ;然后将溶液调成中性并___ 就可以得到较为纯净的氯化钠。
④除去氧化钙中的碳酸钙可用___ 的方法。
①实验室中的石灰水久置,液面上常悬浮有CaCO3微粒。可用
②除去H2中的CO2,可用
③粗盐中含有不溶性的泥沙、可溶性的氯化钙、氯化镁及一些硫酸盐.要将粗盐提纯,可先将粗盐溶解,按一定的顺序加入沉淀剂,再
④除去氧化钙中的碳酸钙可用
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐3】I.已知 和
和 两支试管所盛的溶液中共含有
两支试管所盛的溶液中共含有 、
、 、
、 、
、 、
、 、
、 六种离子,向试管
六种离子,向试管 的溶液中滴入酚酞试液呈粉红色。请回答下列问题:
的溶液中滴入酚酞试液呈粉红色。请回答下列问题:
(1)试管 的溶液中所含的上述离子有
的溶液中所含的上述离子有___________ 。
(2)若将试管 和试管
和试管 中的溶液按一定体积比混合过滤后,蒸干滤液可得到一种纯净物,则混合过程中发生反应的离子方程式为
中的溶液按一定体积比混合过滤后,蒸干滤液可得到一种纯净物,则混合过程中发生反应的离子方程式为___________ 、___________ 。(不考虑氢氧化银的存在)
(3)若向由试管 溶液中的阳离子组成的碳酸氢盐溶液中,滴入少量
溶液中的阳离子组成的碳酸氢盐溶液中,滴入少量 溶液,则发生反应的离子方程式为
溶液,则发生反应的离子方程式为___________ 。
II.为除去粗盐中的 、
、 、
、 以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):
以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):
称取粗盐
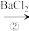
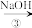
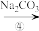
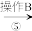 滤液
滤液
 精盐
精盐
(4)第①步中,操作 是
是___________ ,第⑤步中,操作
___________ ;
(5)第④步中,写出相应的离子方程式(设粗盐溶液中 的主要存在形式为CaCl2)
的主要存在形式为CaCl2)___________ ,___________ ;
(6)若先用盐酸调 再过滤,将对实验结果产生影响,其原因是
再过滤,将对实验结果产生影响,其原因是___________ 。
 和
和 两支试管所盛的溶液中共含有
两支试管所盛的溶液中共含有 、
、 、
、 、
、 、
、 、
、 六种离子,向试管
六种离子,向试管 的溶液中滴入酚酞试液呈粉红色。请回答下列问题:
的溶液中滴入酚酞试液呈粉红色。请回答下列问题:(1)试管
 的溶液中所含的上述离子有
的溶液中所含的上述离子有(2)若将试管
 和试管
和试管 中的溶液按一定体积比混合过滤后,蒸干滤液可得到一种纯净物,则混合过程中发生反应的离子方程式为
中的溶液按一定体积比混合过滤后,蒸干滤液可得到一种纯净物,则混合过程中发生反应的离子方程式为(3)若向由试管
 溶液中的阳离子组成的碳酸氢盐溶液中,滴入少量
溶液中的阳离子组成的碳酸氢盐溶液中,滴入少量 溶液,则发生反应的离子方程式为
溶液,则发生反应的离子方程式为II.为除去粗盐中的
 、
、 、
、 以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):
以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):称取粗盐
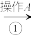
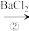
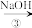
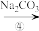
 滤液
滤液
 精盐
精盐(4)第①步中,操作
 是
是
(5)第④步中,写出相应的离子方程式(设粗盐溶液中
 的主要存在形式为CaCl2)
的主要存在形式为CaCl2)(6)若先用盐酸调
 再过滤,将对实验结果产生影响,其原因是
再过滤,将对实验结果产生影响,其原因是
您最近一年使用:0次



