将11.2g铁粉投入200mL的稀硫酸中,充分反应后,铁粉完全溶解。(假设反应后溶液体积不发生变化,写出计算过程)
⑴求标准状况下产生气体的体积。(已知:Fe+H2SO4=FeSO4+H2↑)_____________
⑵求反应后溶液中FeSO4的物质的量浓度。_________________
⑴求标准状况下产生气体的体积。(已知:Fe+H2SO4=FeSO4+H2↑)
⑵求反应后溶液中FeSO4的物质的量浓度。
更新时间:2020-01-08 09:22:43
|
相似题推荐
【推荐1】镁、铝、铁及其化合物在生产和生活中有广泛的应用。
(1)镁铝合金用在飞机制造业,现有3.90克镁铝合金溶于足量的2mol/L稀硫酸中生成0.2mol氢气,计算并确定镁铝合金中物质的量n(Mg): n(Al)=_________ ;
(2)硫铁矿的主要成分为FeS2(假设杂质只含SiO2)是生产硫酸的原料。取某硫铁矿10g在足量的空气中煅烧(4FeS2+11O2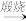 2Fe2O3 +8SO2),充分反应后冷却,称得固体质量为7.4g(杂质SiO2不反应)。该硫铁矿中FeS2的质量分数为
2Fe2O3 +8SO2),充分反应后冷却,称得固体质量为7.4g(杂质SiO2不反应)。该硫铁矿中FeS2的质量分数为_______________ 。铁锈的主要成分实为羟基氧化铁[化学式FeO(OH)]。将一块带锈铁片放入700mL 1.0mol/L的稀硝酸中充分反应,收集到标准状况下NO气体3.584 L,最终剩余2.020g铁。该过程中可能发生的反应有:
①Fe+4HNO3 →Fe(NO3)3+NO↑+2H2O
②3Fe+8HNO3 →3Fe(NO3)2+2NO↑+4H2O
③FeO(OH) +3HNO3 →Fe(NO3)3+2H2O
④Fe+2Fe(NO3)3 →3Fe(NO3)2
(3)试确定反应后溶液中溶质的成分与物质的量_________________ 。
(4)原带锈铁片中铁锈的质量分数__________________ 。
(1)镁铝合金用在飞机制造业,现有3.90克镁铝合金溶于足量的2mol/L稀硫酸中生成0.2mol氢气,计算并确定镁铝合金中物质的量n(Mg): n(Al)=
(2)硫铁矿的主要成分为FeS2(假设杂质只含SiO2)是生产硫酸的原料。取某硫铁矿10g在足量的空气中煅烧(4FeS2+11O2
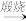 2Fe2O3 +8SO2),充分反应后冷却,称得固体质量为7.4g(杂质SiO2不反应)。该硫铁矿中FeS2的质量分数为
2Fe2O3 +8SO2),充分反应后冷却,称得固体质量为7.4g(杂质SiO2不反应)。该硫铁矿中FeS2的质量分数为①Fe+4HNO3 →Fe(NO3)3+NO↑+2H2O
②3Fe+8HNO3 →3Fe(NO3)2+2NO↑+4H2O
③FeO(OH) +3HNO3 →Fe(NO3)3+2H2O
④Fe+2Fe(NO3)3 →3Fe(NO3)2
(3)试确定反应后溶液中溶质的成分与物质的量
(4)原带锈铁片中铁锈的质量分数
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】CO2和KO2有下列反应:
4KO2+2CO2→2K2CO3+3O2
4KO2+4CO2+2H2O→4KHCO3+3O2
若9 mol CO2在密封舱内和KO2反应后生成9 mol O2,则反应前密封舱内H2O的量应该是________ ?列式计算。
4KO2+2CO2→2K2CO3+3O2
4KO2+4CO2+2H2O→4KHCO3+3O2
若9 mol CO2在密封舱内和KO2反应后生成9 mol O2,则反应前密封舱内H2O的量应该是
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】(1)标准状况下,将33.6LHCl气体溶于水配成2L溶液,所得盐酸的物质的量浓度为_______ 。
(2)标准状况下,3.4gNH3与_____ LO2气体所含电子数相同。
(3)核内中子数为N的R2+离子,质量数为A,则ng它的氧化物中所含质子的物质的量是_______ mol
(4)某物质A加热时按化学方程式2A=2B+C+3D分解,产物均为气体,测得由生成物组成的混合物气体对H2的相对密度为20,则反应物A的摩尔质量为______ 。
(5)标准状况下,NH3与CH4组成的混合气体的平均密度为0.75g/L,则NH3的体积分数为_______ 。
(2)标准状况下,3.4gNH3与
(3)核内中子数为N的R2+离子,质量数为A,则ng它的氧化物中所含质子的物质的量是
(4)某物质A加热时按化学方程式2A=2B+C+3D分解,产物均为气体,测得由生成物组成的混合物气体对H2的相对密度为20,则反应物A的摩尔质量为
(5)标准状况下,NH3与CH4组成的混合气体的平均密度为0.75g/L,则NH3的体积分数为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐1】把5.6g的Fe放入足量稀硫酸中,Fe完全反应。计算:
(1)5.6gFe的物质的量_________ ;
(2)生成H2的体积(标准状况)_________ 。
(1)5.6gFe的物质的量
(2)生成H2的体积(标准状况)
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】mg铁与一定量水蒸气在高温条件下充分反应,测得生成氢气8.96L,将所得固体混合物完全溶解于足量盐酸,又放出氢气2.24L(气体体积均已折算为标况下),向所得溶液中滴加KSCN溶液,溶液颜色无明显变化。计算:
(1)铁与水蒸气反应时生成的氧化产物质量是多少?_______
(2)最初所用铁粉的质量是多少?_________
(1)铁与水蒸气反应时生成的氧化产物质量是多少?
(2)最初所用铁粉的质量是多少?
您最近一年使用:0次



