A、B、C、D为石墨电极,E、F分别为短周期相邻两种活泼金属中的一种,且E能与NaOH溶液反应。按图示接通线路,反应一段时间。
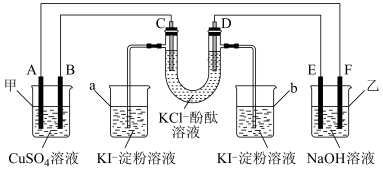
(1)判断装置的名称:甲池为_____ (填“电解池”或“原电池”,下同),乙池为____ 。
(2)B极为____ (填“正极”或“负极”或“阳极”或“阴极”,下同),电极反应式为______ ;F极为____ ,电极反应式为_______ 。
(3)烧杯中溶液会变蓝的是_____ (填“a”或“b”),U形管中溶液先变红的是_____ (填“C”或“D”)极,U形管中发生反应的化学方程式为_________ 。
(4)当烧杯中有38.1 g I2(KI足量)生成时,甲池中溶液的质量会减少_____ g。

(1)判断装置的名称:甲池为
(2)B极为
(3)烧杯中溶液会变蓝的是
(4)当烧杯中有38.1 g I2(KI足量)生成时,甲池中溶液的质量会减少
18-19高二·黑龙江大兴安岭地·期末 查看更多[4]
黑龙江省大兴安岭漠河县第一中学2018-2019学年高二上学期新高考教学质量检测化学试题人教版(2019)高二化学选择性必修1第四章 化学反应与电能 过素养 学科素养拓展训练(已下线)微专题35 电化学“多池和多室”串联问题及计算-备战2023年高考化学一轮复习考点微专题吉林省珲春市第二高级中学校2023-2024学年高二上学期期末考试化学试题
更新时间:2020-01-18 09:55:11
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】下图所示装置中,甲、乙、丙三个烧杯依次分别盛放足量的KI溶液、足量的CuSO4溶液和K2SO4溶液,电极均为石墨电极。接通电源,经过一段时间后,测得乙中c电极质量增加32 g。据此回答问题:

(1)电源的N端为_________ 极;
(2)电极b上发生的电极反应为______________________________________ ;
(3)电极f上生成的气体在标准状况下的体积______________ ;
(4)电解开始时,在甲烧杯的中央,滴几滴淀粉溶液,你能观察到的现象是____________________ ;
(5)电解前后溶液的pH变化情况,(填增大、减小或不变)甲溶液__________ ;乙溶液____________ 。

(1)电源的N端为
(2)电极b上发生的电极反应为
(3)电极f上生成的气体在标准状况下的体积
(4)电解开始时,在甲烧杯的中央,滴几滴淀粉溶液,你能观察到的现象是
(5)电解前后溶液的pH变化情况,(填增大、减小或不变)甲溶液
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】硒的原子序数为34,是硫的同主族元系,硒的单质及其化合物用途非常广泛。
(1)硫的原子结构示意图为_____________ 。
(2)Se2Cl2常用作分析试剂,其电子式为_____________ 。
(3)硒化铟是一种可应用于未来超算设备的新型半导体材料。已知铟(In)与铝同族且比铝多两个电子层。下列说法正确的是___________ (填字母)。
A. In的金属性比A1弱 B.原子半径:In>Se
C.In的金属性比Se强 D.硒化铟的化学式为InSe2
(4)工业上常从电冶铜的阳极泥中提取纳米硒。向浆化的阳极泥中通入氯气,Cu2Se被溶液中的HClO氧化为H2SeO3 及CuCl2,当生成1molH2SeO3时,消耗HClO的物质的量为______ mol。用氨水中和亚硒酸后得到亚硒酸铵,再向(NH4)2SeO3溶液中加入Na2SeO3可得到纳米硒,同时生成亚硫酸盐,(NH4)2SeO3与Na2S2O3反应生成纳米硒的离子方程式为_____________ 。
(1)硫的原子结构示意图为
(2)Se2Cl2常用作分析试剂,其电子式为
(3)硒化铟是一种可应用于未来超算设备的新型半导体材料。已知铟(In)与铝同族且比铝多两个电子层。下列说法正确的是
A. In的金属性比A1弱 B.原子半径:In>Se
C.In的金属性比Se强 D.硒化铟的化学式为InSe2
(4)工业上常从电冶铜的阳极泥中提取纳米硒。向浆化的阳极泥中通入氯气,Cu2Se被溶液中的HClO氧化为H2SeO3 及CuCl2,当生成1molH2SeO3时,消耗HClO的物质的量为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】在如图所示的实验装置中,E为一张用淀粉、碘化钾和酚酞的混合溶液润湿的滤纸,C、D为夹在滤纸两端的铂夹,X、Y分别为直流电源的两极。在A、B中装满KOH溶液后倒立于盛有KOH溶液的水槽中,再分别插入铂电极。切断电源开关S1,闭合开关S2,通直流电一段时间后,A、B现象如图所示。请回答下列问题:

(1)电源负极为________ (填“X”或“Y”)。
(2)在滤纸的D端附近,观察到的现象是___________________ 。
(3)写出电极反应式:B中______________ ,C中_________________ 。
(4)若电解一段时间后,A、B中均有气体包围电极。此时切断开关S2,闭合开关S1。若电流计指针偏转,写出有关的电极反应式(若指针“不偏转”,此题不必回答):
A极_____________________ ,B极_______________________ 。

(1)电源负极为
(2)在滤纸的D端附近,观察到的现象是
(3)写出电极反应式:B中
(4)若电解一段时间后,A、B中均有气体包围电极。此时切断开关S2,闭合开关S1。若电流计指针偏转,写出有关的电极反应式(若指针“不偏转”,此题不必回答):
A极
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】某实验小组依据甲烷燃烧的反应原理,设计如图所示的装置。

(1)甲池中负极的电极反应式为___________ 。
(2)乙池中A(石墨)电极的名称为___________ (填“正极”“负极”“阴极”或“阳极”),乙池中总反应为___________ 。
(3)若乙池中溶液体积为 ,当B电极质量增加
,当B电极质量增加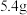 时,其
时,其 为
为___________ (忽略溶液体积变化);甲池中理论上消耗 的体积为
的体积为___________  (标准状况下);假设乙池、丙池中的溶液均足量,丙池中
(标准状况下);假设乙池、丙池中的溶液均足量,丙池中___________ (填“C”或“D”)极析出___________ g铜。

(1)甲池中负极的电极反应式为
(2)乙池中A(石墨)电极的名称为
(3)若乙池中溶液体积为
 ,当B电极质量增加
,当B电极质量增加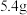 时,其
时,其 为
为 的体积为
的体积为 (标准状况下);假设乙池、丙池中的溶液均足量,丙池中
(标准状况下);假设乙池、丙池中的溶液均足量,丙池中
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】I.(1)钢铁容易生锈的主要原因是钢铁在炼制过程中混有少量的碳杂质,在潮湿的空气中容易形成原电池,发生电化学腐蚀。在酸性环境下,其正极反应式为_____________ ;在酸性很弱或中性条件下,其发生___________________ (填“析氢腐蚀”或“吸氧腐蚀”)。
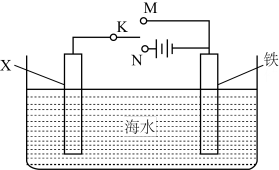
(2)利用如图装置,可以模拟铁的电化学防护。若X为碳棒,开关K置于N处,该电化学防护法称为____________________ ;若X为锌棒,开关K置于M处,________ (填“能”或“不能”)达到防止铁腐蚀 目的。
目的。
II.如图所示,其中甲池的总反应式为2CH3OH+3O2+4KOH=2K2CO3+6H2O,完成下列问题:
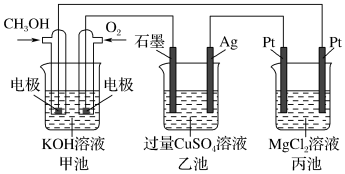
(1)甲池燃料电池的负极反应为___________________ 。
(2)乙池中石墨电极为___________ 极,发生_____________ 反应(填“氧化”或“还原”)写出乙池中电解总反应的化学方程式: ___________________ 。
(3)甲池中消耗224mL(标准状况下)O2,此时丙池中理论上最多产生________ g沉淀,此时乙池中溶液的体积为400mL,该溶液的pH=____________ 。
(2)利用如图装置,可以模拟铁的电化学防护。若X为碳棒,开关K置于N处,该电化学防护法称为
 目的。
目的。
II.如图所示,其中甲池的总反应式为2CH3OH+3O2+4KOH=2K2CO3+6H2O,完成下列问题:

(1)甲池燃料电池的负极反应为
(2)乙池中石墨电极为
(3)甲池中消耗224mL(标准状况下)O2,此时丙池中理论上最多产生
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】(1)加入双氧水能提高软锰矿(主要成分是MnO2)的浸出率,锰转化成Mn2+。写出酸性条件下双氧水提高软锰矿浸出率的离子方程式:_________ 。
(2)碘与氢氧化钠反应的生成物中含有IO3-,写出反应过程的离子方程式:___ 。
(3) 电镀污泥中的Cr2O3与加入的Na2CO3在空气中焙烧,Cr2O3被氧化为Na2CrO4,还有CO2逸出,写出该反应的化学方程式:_____________ 。
(4)某科研小组在实验室用较浓的KOH溶液直接吸收氯气,研究发现反应进行一段时间后开始出现KClO3并逐渐增多,产生KClO3的离子方程式是_______ 。
(5) 用氧缺位铁酸铜(CuFe2O4-x)作催化剂,利用太阳能热化学循环分解H2O也可制H2,其物质转化如图1所示。
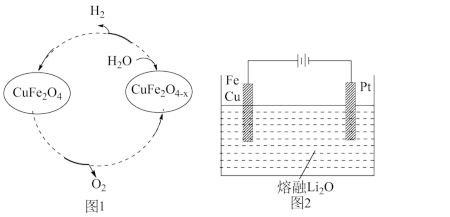
①氧缺位铁酸铜(CuFe2O4-x)与水反应的化学方程式为_________ 。
②CuFe2O4可用电化学方法得到,其原理如图2所示,则阳极的电极反应式为_________ 。
(2)碘与氢氧化钠反应的生成物中含有IO3-,写出反应过程的离子方程式:
(3) 电镀污泥中的Cr2O3与加入的Na2CO3在空气中焙烧,Cr2O3被氧化为Na2CrO4,还有CO2逸出,写出该反应的化学方程式:
(4)某科研小组在实验室用较浓的KOH溶液直接吸收氯气,研究发现反应进行一段时间后开始出现KClO3并逐渐增多,产生KClO3的离子方程式是
(5) 用氧缺位铁酸铜(CuFe2O4-x)作催化剂,利用太阳能热化学循环分解H2O也可制H2,其物质转化如图1所示。

①氧缺位铁酸铜(CuFe2O4-x)与水反应的化学方程式为
②CuFe2O4可用电化学方法得到,其原理如图2所示,则阳极的电极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】某课外小组设计如图1所示装置为电源对粗铜(含有Cu,少量Fe、Zn、Ag、Au等)进行精炼。(已知:装置I中发生的副反应为Fe电极直接与 溶液反应)
溶液反应)
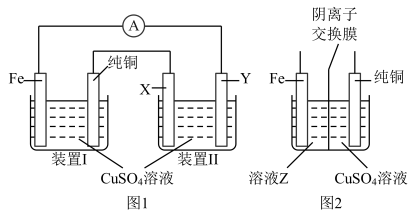
(1)装置I中Fe电极上发生反应的电极反应式为_______ 。
(2)当反应一段时间后,经测量发现,Fe电极质量减少0.80 g,纯铜电极质量增重0.96 g,则实际经过电流表的电子的物质的量为_______ mol,装置I的能量转化率为_______ 。(已知:装置I中 足量)
足量)
(3)有同学提议,为避免副反应的发生,应将装置I改为如图2所示装置,则溶液Z中溶质的化学式为_______ 。
(4)装置II中X电极材料的名称为_______ ,Y电极上的电极反应式为_______ ,一段时间后,装置II溶液中阳离子主要为 和
和_______ 。
 溶液反应)
溶液反应)
(1)装置I中Fe电极上发生反应的电极反应式为
(2)当反应一段时间后,经测量发现,Fe电极质量减少0.80 g,纯铜电极质量增重0.96 g,则实际经过电流表的电子的物质的量为
 足量)
足量)(3)有同学提议,为避免副反应的发生,应将装置I改为如图2所示装置,则溶液Z中溶质的化学式为
(4)装置II中X电极材料的名称为
 和
和
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】电池的发明和应用是化学家们对人类社会的重要贡献之一。
每一次化学电池技术的突破,都带来了电子设备革命性的发展。最近,我国在甲烷燃料电池的相关技术上获得了新突破,原理如下图所示。
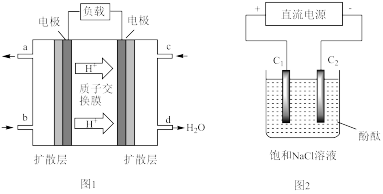
(1)甲烷燃料应从__________ 口通入(图1),发生的电极反应式 __________________ 。
(2)以石墨做电极电解饱和食盐水,如下图2所示。电解开始后在__________ 的周围(填“阴极”或“阳极”)先出现红色,该极的电极反应式为_______________ 。.
(3)以CuSO4溶液为电解质溶液进行粗铜(含Al、Zn、Ag、Pt、Au等杂质)的电解精炼,下列说法正确的是____ 。
a.利用阳极泥可回收Ag、Pt、Au等金属
b.粗铜接电源正极,发生氧化反应
c.溶液中Cu2+向阳极移动
d.电能全部转化为化学能
(4)人工肾脏可采用间接电化学方法除去代谢产物中的尿素[CO(NH2)2],原理如图。
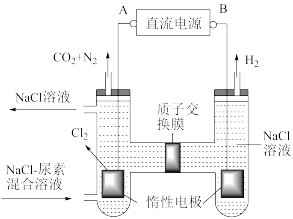
①电源的正极为________ (填“A”或“B”)。
②电解结束后,阴极室溶液的pH与电解前相比将________ (填“增大”、“减小”、“不变”);若两极共收集到气体6.72 L(标准状况),则除去的尿素为________ g(忽略气体的溶解)。
每一次化学电池技术的突破,都带来了电子设备革命性的发展。最近,我国在甲烷燃料电池的相关技术上获得了新突破,原理如下图所示。

(1)甲烷燃料应从
(2)以石墨做电极电解饱和食盐水,如下图2所示。电解开始后在
(3)以CuSO4溶液为电解质溶液进行粗铜(含Al、Zn、Ag、Pt、Au等杂质)的电解精炼,下列说法正确的是
a.利用阳极泥可回收Ag、Pt、Au等金属
b.粗铜接电源正极,发生氧化反应
c.溶液中Cu2+向阳极移动
d.电能全部转化为化学能
(4)人工肾脏可采用间接电化学方法除去代谢产物中的尿素[CO(NH2)2],原理如图。

①电源的正极为
②电解结束后,阴极室溶液的pH与电解前相比将
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】回答下列问题:
(1)图中X为电源,Y为浸透滴有酚酞试液的饱和食盐水的滤纸,滤纸中央滴有一滴KMnO4溶液,通电后Y中央的紫红色斑向d端扩散。

①Y中总反应的化学方程式为___ ,滤纸上c点附近会变___ 色。
②电解一段时间后,Z产生280mL的气体(标准状况下),此时Z中溶液的体积为500mL,假设溶液中还有AgNO3存在,则溶液中氢离子的物质的量是___ ,需加入___ g的__ (填化学式)可使溶液复原。
(2)用惰性电极电解200mL一定浓度的硫酸铜溶液,实验装置如图甲所示,电解过程中的实验数据如图乙所示,横坐标表示电解过程中转移电子的物质的量,纵坐标表示电解过程中产生气体的总体积(标准状况)。

①OQ段电解过程中生成O2的物质的量是___ 。
②下列说法不正确的是___ (填字母)。
A.电解过程中,a电极表面先有红色物质析出,后有气泡产生
B.b电极上发生的电极反应式为4OH--4e-=2H2O+O2↑
C.OP段表示H2和O2混合气体的体积变化
D.从P点到Q点时收集到的气体为H2和O2
(1)图中X为电源,Y为浸透滴有酚酞试液的饱和食盐水的滤纸,滤纸中央滴有一滴KMnO4溶液,通电后Y中央的紫红色斑向d端扩散。

①Y中总反应的化学方程式为
②电解一段时间后,Z产生280mL的气体(标准状况下),此时Z中溶液的体积为500mL,假设溶液中还有AgNO3存在,则溶液中氢离子的物质的量是
(2)用惰性电极电解200mL一定浓度的硫酸铜溶液,实验装置如图甲所示,电解过程中的实验数据如图乙所示,横坐标表示电解过程中转移电子的物质的量,纵坐标表示电解过程中产生气体的总体积(标准状况)。

①OQ段电解过程中生成O2的物质的量是
②下列说法不正确的是
A.电解过程中,a电极表面先有红色物质析出,后有气泡产生
B.b电极上发生的电极反应式为4OH--4e-=2H2O+O2↑
C.OP段表示H2和O2混合气体的体积变化
D.从P点到Q点时收集到的气体为H2和O2
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】回答下列问题
(1)某兴趣小组的同学认为,如果模拟工业上离子交换膜法制烧碱的方法,那么可以设想用如图装置电解硫酸钾溶液来制取氢气、氧气、硫酸和氢氧化钾。

①该电解槽的阴极反应式为___________ 。
②通电开始后,阳极附近溶液pH会___________ (填“变大”、“变小”或“不变”)
③出口A获得___________ 产品,离子交换膜b是___________ 离子交换膜(填“阳”或“阴”)。
(2)电化学在化学工业中有着广泛应用。根据图示电化学装置,回答下列问题:

①甲池通入乙烷(C2H6)一极的电极反应式为___________ 。
②乙池中,若X、Y都是石墨,A是饱和食盐水,乙池中的离子反应方程式为___________ 。
③若使用铜棒、铁质钥匙等材料用该装置实现在铁质钥匙表面镀一层金属铜,CuSO4溶液作电解液,则乙池中:铁质钥匙应放在___________ 极(填X或Y),电镀一段时间后,CuSO4溶液浓度___________ (“减小”“不变”“增大”)。
④乙池中,若X、Y都是石墨,A是足量AgNO3溶液,体积为2L,电解一段时间后,甲池消耗1.12LO2(标准状况下),则乙池溶液的pH为___________ (忽略溶液体积的变化)。
(3)工业上通过电解浓NaOH溶液制备Na2FeO4,其工作原理如图所示,则阳极的电极反应式为___________ ,当制备0.5molNa2FeO4时,阴极产生气体质量为___________ 。
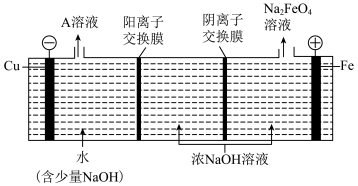
(1)某兴趣小组的同学认为,如果模拟工业上离子交换膜法制烧碱的方法,那么可以设想用如图装置电解硫酸钾溶液来制取氢气、氧气、硫酸和氢氧化钾。

①该电解槽的阴极反应式为
②通电开始后,阳极附近溶液pH会
③出口A获得
(2)电化学在化学工业中有着广泛应用。根据图示电化学装置,回答下列问题:

①甲池通入乙烷(C2H6)一极的电极反应式为
②乙池中,若X、Y都是石墨,A是饱和食盐水,乙池中的离子反应方程式为
③若使用铜棒、铁质钥匙等材料用该装置实现在铁质钥匙表面镀一层金属铜,CuSO4溶液作电解液,则乙池中:铁质钥匙应放在
④乙池中,若X、Y都是石墨,A是足量AgNO3溶液,体积为2L,电解一段时间后,甲池消耗1.12LO2(标准状况下),则乙池溶液的pH为
(3)工业上通过电解浓NaOH溶液制备Na2FeO4,其工作原理如图所示,则阳极的电极反应式为

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】如图是一个电化学过程的示意图,请按要求回答下列问题:

(1)甲池是_______ 装置(填“原电池”或“电解池”),乙池中B为________ 极。
(2)写出电极反应式:通入O2电极:______ 。
(3)反应一段时间后,甲池中消耗(标况下)CH4体积为1.12 L,则乙池中转移电子___________ mol。
(4)电解饱和食盐水是重要的化工产业,它被称为 “氯碱工业”。完成下列问题:
①写出电解饱和食盐水的化学反应方程式___________ 。

②上图为电解饱和食盐水工业中所采用的离子交换膜电解槽示意图,通电以后,Na+向右侧移动,可判断出电极2是___________ 极,在该电极周围的溶液中,NaOH浓度将会___________ (填“变大”或“减小”或“不变”);

(1)甲池是
(2)写出电极反应式:通入O2电极:
(3)反应一段时间后,甲池中消耗(标况下)CH4体积为1.12 L,则乙池中转移电子
(4)电解饱和食盐水是重要的化工产业,它被称为 “氯碱工业”。完成下列问题:
①写出电解饱和食盐水的化学反应方程式

②上图为电解饱和食盐水工业中所采用的离子交换膜电解槽示意图,通电以后,Na+向右侧移动,可判断出电极2是
您最近一年使用:0次




