乙酰乙酸乙酯是有机合成中非常重要的原料,实验室制备乙酰乙酸乙酯的反应原理、装置示意图和有关数据如下所示:
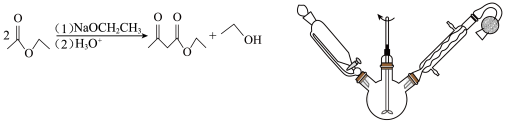
实验步骤:
Ⅰ.合成:向三颈烧瓶中加入9.8ml无水乙酸乙酯,迅速加入0.1g切细的金属钠。水浴加热反应液,缓慢回流约2h至金属钠全部反应完。停止加热,冷却后向反应混合物中加入50%乙酸至反应液呈弱酸性。
Ⅱ.分离与提纯:
①向反应混合物中加入等体积的饱和食盐水,分离得到有机层。
②水层用5mL无水乙酸乙酯萃取,分液。
③将①②所得有机层合并,洗涤、干燥、蒸馏得到乙酰乙酸乙酯粗产品。
④蒸馏粗产品得到乙酰乙酸乙酯3.9g。
(1)球形冷凝管中冷却水从______ (填“上”或“下”)口进入,上方干燥管中盛无水CaCl2,其作用是________ 。
(2)实验室制备乙酰乙酸乙酯时,通常在无水乙酸乙酯中加入微量的无水乙醇,其作用是___ 。
(3)分离与提纯操作①中使用的分离仪器是________ 。加入饱和食盐水的作用是 _______ 。
(4)分离与提纯操作③用饱和NaHCO3溶液洗涤的目的是_______ 。
(5)本实验的产率为_______ %(结果保留两位有效数字)。

| 密度/(g·cm-3) | 沸点/℃ | 水中 溶解性 | |
| 乙酸乙酯 | 0.90 | 77.2 | 难溶 |
| 乙酰乙酸乙酯 | 1.02 | 181 | 微溶 |
| 乙酸 | 1.05 | 118 | 易溶 |
Ⅰ.合成:向三颈烧瓶中加入9.8ml无水乙酸乙酯,迅速加入0.1g切细的金属钠。水浴加热反应液,缓慢回流约2h至金属钠全部反应完。停止加热,冷却后向反应混合物中加入50%乙酸至反应液呈弱酸性。
Ⅱ.分离与提纯:
①向反应混合物中加入等体积的饱和食盐水,分离得到有机层。
②水层用5mL无水乙酸乙酯萃取,分液。
③将①②所得有机层合并,洗涤、干燥、蒸馏得到乙酰乙酸乙酯粗产品。
④蒸馏粗产品得到乙酰乙酸乙酯3.9g。
(1)球形冷凝管中冷却水从
(2)实验室制备乙酰乙酸乙酯时,通常在无水乙酸乙酯中加入微量的无水乙醇,其作用是
(3)分离与提纯操作①中使用的分离仪器是
(4)分离与提纯操作③用饱和NaHCO3溶液洗涤的目的是
(5)本实验的产率为
更新时间:2020-01-20 15:49:21
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
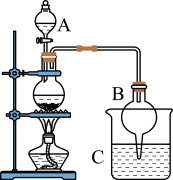
【推荐1】乙酸乙酯是应用最广的脂肪酸酯之一,是极好的工业溶剂,广泛应用于油墨、人造革生产中。某小组同学欲制取并分离提纯乙酸乙酯,制取实验装置设计如图:
已知:无水氯化钙可与乙醇形成微溶于水的CaCl2•6C2H5OH;
有关有机物的沸点:
请回答:
(1)仪器A的名称是_______ ,浓硫酸的作用为______ 。
(2)若用同位素18O标记乙醇中的氧原子,则CH3CH218OH与乙酸生成乙酸乙酯的化学方程式为______ ,该反应的类型属于______ 反应。
(3)该小组同学在实验时加入过量的乙醇的目的是______ 。
(4)球形干燥管B的作用是_____ ,C中放_____ 溶液。
(5)反应时需控制温度不能太高,可能是因为______ 。
(6)从C中分离出的乙酸乙酯中常含有一定量的乙醇、乙醚和水,应先加入______ 除去乙醇。
(7)除去乙醇后再加入______ (选择下列选项);然后进行蒸馏,收集_____ ℃左右的馏分得到较纯净产品。
A.生石灰 B.五氧化二磷 C.无水硫酸钠 D.浓硫酸
(8)乙酸乙酯的某种同分异构体分子中含有2个甲基,且能与碳酸氢钠溶液反应,则该物质的结构简式为_______ 。

已知:无水氯化钙可与乙醇形成微溶于水的CaCl2•6C2H5OH;
有关有机物的沸点:
| 试剂 | 乙醚 | 乙醇 | 乙酸 | 乙酸乙酯 |
| 沸点/℃ | 34.7 | 78.5 | 118 | 77.1 |
(1)仪器A的名称是
(2)若用同位素18O标记乙醇中的氧原子,则CH3CH218OH与乙酸生成乙酸乙酯的化学方程式为
(3)该小组同学在实验时加入过量的乙醇的目的是
(4)球形干燥管B的作用是
(5)反应时需控制温度不能太高,可能是因为
(6)从C中分离出的乙酸乙酯中常含有一定量的乙醇、乙醚和水,应先加入
(7)除去乙醇后再加入
A.生石灰 B.五氧化二磷 C.无水硫酸钠 D.浓硫酸
(8)乙酸乙酯的某种同分异构体分子中含有2个甲基,且能与碳酸氢钠溶液反应,则该物质的结构简式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】代沟是化学老师说什么你都不听,代价就是这道题你什么都不会!
I. A、B、C、D四种物质均含有同一种元素。A是常见的金属单质,C的水溶液呈黄色。A、B、C、D之间在一定条件下有如图所示转化关系:
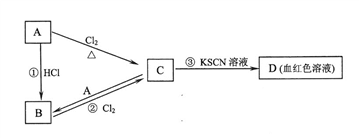
请回答下列问题:
(1)A的化学式是_____________________ 。
(2)反应①的反应类型为_____________ 反应(选填“化合”、“分解”、“置换”、“复分解”)。
(3)反应②的化学方程式是___________________________ 。
(4)C的水溶液与NaOH溶液混合后发生反应的离子方程式是______________________ 。
II. 实验室可以用如图所示装置制取乙酸乙酯。请回答下列问题:

(1)a试管中盛放的是饱和碳酸钠溶液,制得的乙酸乙酯在饱和碳酸钠溶液的________ (填“上”或“下”)层。
(2)制取乙酸乙酯的化学方程式是________________ ,该反应属于_______________ 反应(填反应类型)。左边试管中在加热前往往加入 ____________ 以用于防爆沸。
I. A、B、C、D四种物质均含有同一种元素。A是常见的金属单质,C的水溶液呈黄色。A、B、C、D之间在一定条件下有如图所示转化关系:

请回答下列问题:
(1)A的化学式是
(2)反应①的反应类型为
(3)反应②的化学方程式是
(4)C的水溶液与NaOH溶液混合后发生反应的离子方程式是
II. 实验室可以用如图所示装置制取乙酸乙酯。请回答下列问题:

(1)a试管中盛放的是饱和碳酸钠溶液,制得的乙酸乙酯在饱和碳酸钠溶液的
(2)制取乙酸乙酯的化学方程式是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】“酒是陈的香”是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用如图所示的装置制取乙酸乙酯。回答下列问题:
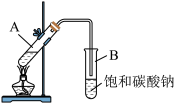
(1)装置B中导管要插在饱和碳酸钠溶液的液面上,不能插入溶液中,目的是__ ;饱和碳酸钠溶液的作用是___ (选字母,可多选)
A.中和乙酸 B.溶解乙醇 C.降低乙酸乙酯的溶解度 D.提高产量
(2)该反应属于__ (选字母,可多选)。
A.加成反应 B.取代反应 C.水解反应 D.酯化反应
(3)写出上述制取乙酸乙酯反应的化学反应方程式:___ 。

(1)装置B中导管要插在饱和碳酸钠溶液的液面上,不能插入溶液中,目的是
A.中和乙酸 B.溶解乙醇 C.降低乙酸乙酯的溶解度 D.提高产量
(2)该反应属于
A.加成反应 B.取代反应 C.水解反应 D.酯化反应
(3)写出上述制取乙酸乙酯反应的化学反应方程式:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】1,2-二溴乙烷可作汽油抗爆剂的添加剂,常温下它是无色液体,不溶于水,易溶于醇等有机溶剂。兴趣小组同学用12.0g溴和足量的乙醇制备1,2-二溴乙烷,实验装置如图所示。
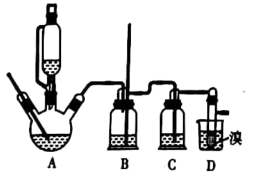
已知:①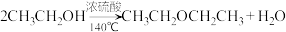 ;
;
②实验中常因温度过高而使乙醇和浓硫酸反应生成少量 和
和 ;
;
③有关数据列表如下:
回答下列问题:
(1)在A中按最佳体积比3∶1加入乙醇与浓硫酸,生成乙烯的化学反应方程式为______ 。
(2)装置B的作用是作安全瓶,瓶中盛水,除了可以防止倒吸以外,还可判断装置是否堵塞,若堵塞,则B中的现象是______ 。
(3)在装置C中加入NaOH溶液,其目的是______ 。
(4)将1,2-二溴乙烷粗产品置于分液漏斗中,加水、振荡后静置,产物应在______ (填“上”或“下”)层。若产物中有少量未反应的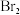 ,最好用
,最好用______ 溶液洗涤除去;若产物中有少量副产物乙醚,可用______ (填操作方法)的方法除去。
(5)反应过程中应用冷水冷却装置D,其主要目的是乙烯与溴反应时放热,冷却可避免溴的大量挥发;但又不能过度冷却(如用冰水),原因是______ 。
(6)实验结束后得到9.4g产品,则该实验中1,2-二溴乙烷的产率为______ (结果精确到0.1%)。

已知:①
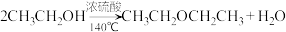 ;
;②实验中常因温度过高而使乙醇和浓硫酸反应生成少量
 和
和 ;
;③有关数据列表如下:
物质 | 乙醇 | 1,2-二溴乙烷 | 乙醚 |
状态 | 无色液体 | 无色液体 | 无色液体 |
密度/ | 0.79 | 2.2 | 0.71 |
沸点/℃ | 78.5 | 132 | 34.6 |
熔点/℃ | -130 | 9 | -116 |
(1)在A中按最佳体积比3∶1加入乙醇与浓硫酸,生成乙烯的化学反应方程式为
(2)装置B的作用是作安全瓶,瓶中盛水,除了可以防止倒吸以外,还可判断装置是否堵塞,若堵塞,则B中的现象是
(3)在装置C中加入NaOH溶液,其目的是
(4)将1,2-二溴乙烷粗产品置于分液漏斗中,加水、振荡后静置,产物应在
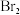 ,最好用
,最好用(5)反应过程中应用冷水冷却装置D,其主要目的是乙烯与溴反应时放热,冷却可避免溴的大量挥发;但又不能过度冷却(如用冰水),原因是
(6)实验结束后得到9.4g产品,则该实验中1,2-二溴乙烷的产率为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】环己烯是重要的化工原料。其实验室制备流程如图所示:
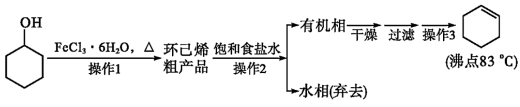
Ⅰ.环己烯的制备与提纯
(1)操作1的装置如图所示(加热和夹持装置已略去):
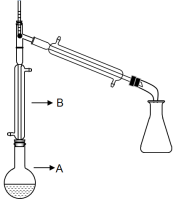
①烧瓶 中进行的可逆反应化学方程式为
中进行的可逆反应化学方程式为___________ 。
②仪器 的名称为
的名称为___________ ,作用是___________ 。
(2)操作2的名称是___________ 。
(3)将操作3(蒸馏)的步骤补齐:安装蒸馏装置___________ ,弃去前馏分,收集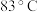 的馏分。
的馏分。
Ⅱ.环己烯含量的测定
在一定条件下,向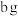 环己烯样品中加入
环己烯样品中加入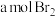 ,与环己烯充分反应后,剩余的
,与环己烯充分反应后,剩余的 与足量
与足量 作用生成
作用生成 ,向生成
,向生成 后的溶液中滴加少量淀粉溶液,再滴加
后的溶液中滴加少量淀粉溶液,再滴加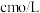 的
的 溶液,发生反应:
溶液,发生反应: ,恰好完全反应时,消耗
,恰好完全反应时,消耗 溶液的体积为
溶液的体积为 (以上数据均已扣除干扰因素)。
(以上数据均已扣除干扰因素)。
(4)样品中环己烯的质量分数为___________ (用字母表示)。
(5)下列情况会导致测定结果偏高的是___________ (填序号)。
a. 标准溶液部分被氧化
标准溶液部分被氧化
b.样品中含有苯酚杂质
c.在测定过程中部分环己烯挥发

Ⅰ.环己烯的制备与提纯
(1)操作1的装置如图所示(加热和夹持装置已略去):

①烧瓶
 中进行的可逆反应化学方程式为
中进行的可逆反应化学方程式为②仪器
 的名称为
的名称为(2)操作2的名称是
(3)将操作3(蒸馏)的步骤补齐:安装蒸馏装置
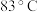 的馏分。
的馏分。Ⅱ.环己烯含量的测定
在一定条件下,向
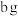 环己烯样品中加入
环己烯样品中加入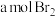 ,与环己烯充分反应后,剩余的
,与环己烯充分反应后,剩余的 与足量
与足量 作用生成
作用生成 ,向生成
,向生成 后的溶液中滴加少量淀粉溶液,再滴加
后的溶液中滴加少量淀粉溶液,再滴加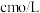 的
的 溶液,发生反应:
溶液,发生反应: ,恰好完全反应时,消耗
,恰好完全反应时,消耗 溶液的体积为
溶液的体积为 (以上数据均已扣除干扰因素)。
(以上数据均已扣除干扰因素)。(4)样品中环己烯的质量分数为
(5)下列情况会导致测定结果偏高的是
a.
 标准溶液部分被氧化
标准溶液部分被氧化b.样品中含有苯酚杂质
c.在测定过程中部分环己烯挥发
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】苯乙酸铜是合成优良催化剂、传感材料——纳米氧化铜的重要前驱体之一。下面是它的一种实验室合成路线:
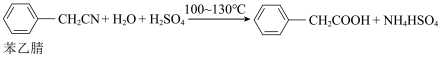
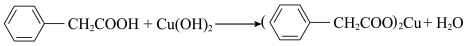
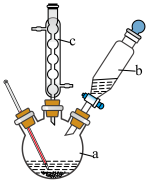
制备苯乙酸的装置示意图如下(加热和夹持装置等略):
已知:苯乙酸的熔点为76.5 ℃,微溶于冷水,溶于乙醇。
(1)在250 mL三口瓶a中加入70 mL70%硫酸。配制此硫酸时,加入蒸馏水与浓硫酸的先后顺序是_____________ 。
(2)将a中的溶液加热至100 ℃,缓缓滴加40 g苯乙腈到硫酸溶液中,然后升温至130 ℃继续反应。仪器c的名称及作用是______________ 。反应结束后加适量冷水,再分离出苯乙酸粗品。加入冷水的目的是______________ 。下列仪器中可用于分离苯乙酸粗品的是__________ (填编号)。
A.分液漏斗B.漏斗C.烧杯D.直形冷凝管E.玻璃棒
(3)提纯粗苯乙酸的方法是___________________ 。
(4)用CuCl2•2H2O和NaOH溶液制备适量Cu(OH)2沉淀,并多次用蒸馏水洗涤沉淀,判断沉淀洗干净的实验操作和现象是_______________________ 。
(5)将苯乙酸加入到乙醇与水的混合溶剂中,充分溶解后,加入Cu(OH)2搅拌30min,过滤,滤液静置一段时间,析出苯乙酸铜晶体,混合溶剂中乙醇的作用是_________________ 。
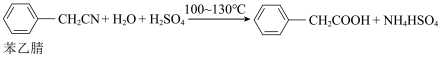
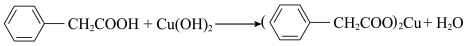
制备苯乙酸的装置示意图如下(加热和夹持装置等略):

已知:苯乙酸的熔点为76.5 ℃,微溶于冷水,溶于乙醇。
(1)在250 mL三口瓶a中加入70 mL70%硫酸。配制此硫酸时,加入蒸馏水与浓硫酸的先后顺序是
(2)将a中的溶液加热至100 ℃,缓缓滴加40 g苯乙腈到硫酸溶液中,然后升温至130 ℃继续反应。仪器c的名称及作用是
A.分液漏斗B.漏斗C.烧杯D.直形冷凝管E.玻璃棒
(3)提纯粗苯乙酸的方法是
(4)用CuCl2•2H2O和NaOH溶液制备适量Cu(OH)2沉淀,并多次用蒸馏水洗涤沉淀,判断沉淀洗干净的实验操作和现象是
(5)将苯乙酸加入到乙醇与水的混合溶剂中,充分溶解后,加入Cu(OH)2搅拌30min,过滤,滤液静置一段时间,析出苯乙酸铜晶体,混合溶剂中乙醇的作用是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】高锰酸钾具有强氧化性,广泛应用于化工、医药、金属冶炼等领域。实验室可通过固体碱溶氧化法制备高锰酸钾。回答下列问题:
(1)称取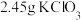 和
和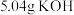 ,置于铁坩埚中并混合均匀,加热混合物至熔融。加热铁坩埚时,除图中的部分仪器外,还需要
,置于铁坩埚中并混合均匀,加热混合物至熔融。加热铁坩埚时,除图中的部分仪器外,还需要_______ (填仪器名称),不使用瓷坩埚的原因是_______ 。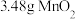 分多次加入熔融物中,继续加热,反应剧烈,最终得到墨绿色
分多次加入熔融物中,继续加热,反应剧烈,最终得到墨绿色 。该步反应的化学方程式为
。该步反应的化学方程式为_______ ,分多次加入 的原因是
的原因是_______ 。
(3)待铁坩埚冷却后,将其置于蒸馏水中共煮至固体全部溶解。趁热向浸取液中通入 ,使
,使 歧化为
歧化为 与
与 。用玻璃棒蘸取溶液于滤纸上,观察到
。用玻璃棒蘸取溶液于滤纸上,观察到_______ ,表明转化已完全。静置片刻,抽滤。该步骤若用 代替
代替 ,可能的后果是
,可能的后果是_______ 。
(4)水浴加热滤液至出现 晶膜,冷却后抽滤、干燥晶体。在该实验中采用水浴加热的主要优点是
晶膜,冷却后抽滤、干燥晶体。在该实验中采用水浴加热的主要优点是_______ 。下表是部分化合物溶解度随温度变化的数据,步骤(3)中 不宜通入过多,目的是
不宜通入过多,目的是_______ ,产品经纯化后称重,质量为3.60g。本实验中 的产率为
的产率为_______ %。
(1)称取
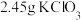 和
和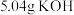 ,置于铁坩埚中并混合均匀,加热混合物至熔融。加热铁坩埚时,除图中的部分仪器外,还需要
,置于铁坩埚中并混合均匀,加热混合物至熔融。加热铁坩埚时,除图中的部分仪器外,还需要
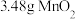 分多次加入熔融物中,继续加热,反应剧烈,最终得到墨绿色
分多次加入熔融物中,继续加热,反应剧烈,最终得到墨绿色 。该步反应的化学方程式为
。该步反应的化学方程式为 的原因是
的原因是(3)待铁坩埚冷却后,将其置于蒸馏水中共煮至固体全部溶解。趁热向浸取液中通入
 ,使
,使 歧化为
歧化为 与
与 。用玻璃棒蘸取溶液于滤纸上,观察到
。用玻璃棒蘸取溶液于滤纸上,观察到 代替
代替 ,可能的后果是
,可能的后果是(4)水浴加热滤液至出现
 晶膜,冷却后抽滤、干燥晶体。在该实验中采用水浴加热的主要优点是
晶膜,冷却后抽滤、干燥晶体。在该实验中采用水浴加热的主要优点是 不宜通入过多,目的是
不宜通入过多,目的是 的产率为
的产率为| 温度/℃ | 20 | 30 | 40 | 50 |
 | 110 | 114 | 117 | 121 |
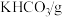 | 33.7 | 39.9 | 47.5 | 65.6 |
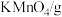 | 6.4 | 9.0 | 12.6 | 16.9 |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】图中为实验室制取氯气及性质验证的装置图,参考装置图回答下列问题:

(1)请指出仪器的名称:a:_______ b:_______ ,
(2)写出装置A中反应的化学方程式:_______ 。
(3)在装置D中可观察到的现象是_______ ,装置E中可观察到的现象是_______ 。
(4)装置B的作用为_______ ,装置C的作用为_______ ,小明同学认为该套装置应该添加装置F,其作用是_______ 。

(1)请指出仪器的名称:a:
(2)写出装置A中反应的化学方程式:
(3)在装置D中可观察到的现象是
(4)装置B的作用为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】氯苯是染料、医药、有机合成的中间体,是重要的有机化工产品。其合成反应原理是:C6H6+Cl2 C6H5Cl+HCl
C6H5Cl+HCl
某实验室制取氯苯的装置如图所示(加热和夹持装置已略去)。

请回答下列问题:
(1)仪器a、b组合成制取氯气的装置,反应不需要加热,则仪器a中的固体反应物是__ (填化学式)。
(2)把氯气干燥后通入装有40mL苯(密度0.88g/mL)的反应器d中(内有铁屑作催化剂),维持反应温度在50~60℃,回流40分钟。对仪器d加热的方法是__ 。
(3)仪器c的名称是___ ,仪器c出口的气体成分有HCl、Cl2和__ 。
(4)将d中的液体倒入分液漏斗中,分别用蒸馏水和NaOH溶液洗涤,分离出的产物干燥后,进行蒸馏纯化,得到24g纯净的氯苯。
①碱洗之前要进行水洗,其目的是__ 。
②用10%NaOH溶液碱洗时发生氧化还原反应的化学方程式为__ 。
③该实验所得氯苯的产率为__ (保留小数点后一位),该产率低于理论产率的原因___ (填写两条)。
 C6H5Cl+HCl
C6H5Cl+HCl某实验室制取氯苯的装置如图所示(加热和夹持装置已略去)。

请回答下列问题:
(1)仪器a、b组合成制取氯气的装置,反应不需要加热,则仪器a中的固体反应物是
(2)把氯气干燥后通入装有40mL苯(密度0.88g/mL)的反应器d中(内有铁屑作催化剂),维持反应温度在50~60℃,回流40分钟。对仪器d加热的方法是
(3)仪器c的名称是
(4)将d中的液体倒入分液漏斗中,分别用蒸馏水和NaOH溶液洗涤,分离出的产物干燥后,进行蒸馏纯化,得到24g纯净的氯苯。
①碱洗之前要进行水洗,其目的是
②用10%NaOH溶液碱洗时发生氧化还原反应的化学方程式为
③该实验所得氯苯的产率为
您最近一年使用:0次




