利用图装置,可以模拟铁的电化学防护。

若X为铜,为减缓铁的腐蚀,开关K应置于__ 处;若X为锌棒,开关K置于M处,该电化学防护法称为__ 。

若X为铜,为减缓铁的腐蚀,开关K应置于
19-20高二·全国·单元测试 查看更多[2]
更新时间:2020-02-11 18:02:26
|
相似题推荐
填空题
|
容易
(0.94)
【推荐1】对金属制品进行防腐蚀处理,可延长其使用寿命。
(1)以下为铝材表面处理的一种方法:
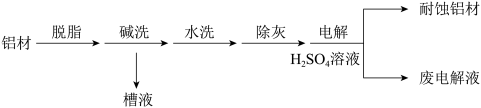
①碱洗的目的是除去铝材表面的自然氧化膜,碱洗时候常有气泡冒出,原因是:________ (用离子方程式表示)。为将碱洗槽液中的铝以沉淀形式回收,最好向槽液中加入下列试剂中的__________ 。
a.NH3b.CO2c.NaOH d.HNO3
②以铝材为阳极,在H2SO4溶液中电解,铝村表面形成氧化膜,阳极电极反应式为:_____ 。
取少量废电解液,加入NaHCO3溶液后产生气泡和白色沉淀,产生沉淀的原因是_________ 。
(2)镀铜可防止铁制品腐蚀,电镀时用铜而不用石墨做阳极的原因是___________ 。
(3)利用下图装置,可以模拟铁的电化学防护。
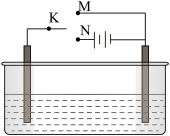
若X为碳棒,为减缓铁的腐蚀,开关K应该置于_______________ 处。
若X为锌,开关K置于M处,该电化学防护法称为_______________ 。
(1)以下为铝材表面处理的一种方法:

①碱洗的目的是除去铝材表面的自然氧化膜,碱洗时候常有气泡冒出,原因是:
a.NH3b.CO2c.NaOH d.HNO3
②以铝材为阳极,在H2SO4溶液中电解,铝村表面形成氧化膜,阳极电极反应式为:
取少量废电解液,加入NaHCO3溶液后产生气泡和白色沉淀,产生沉淀的原因是
(2)镀铜可防止铁制品腐蚀,电镀时用铜而不用石墨做阳极的原因是
(3)利用下图装置,可以模拟铁的电化学防护。

若X为碳棒,为减缓铁的腐蚀,开关K应该置于
若X为锌,开关K置于M处,该电化学防护法称为
您最近一年使用:0次
填空题
|
容易
(0.94)
解题方法
【推荐2】Ⅰ.化学电源在生产生活中有着广泛的应用。
(1)下列化学方程式表示的化学反应能够设计成原电池的是___________
(2)为了探究化学反应中的能量变化,某同学用相同的 棒和相同浓度、相同体积的稀
棒和相同浓度、相同体积的稀 溶液,设计了两个实验(如下图)。有关实验现象,下列说法正确的是___________
溶液,设计了两个实验(如下图)。有关实验现象,下列说法正确的是___________

Ⅱ.以氨气替代氢气研发氨燃料电池是当前科研的一个热点。
(3)氨燃料电池使用的电解质溶液是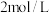 的
的 溶液,电池反应为:
溶液,电池反应为: ,该电池负极的电极反应为:
,该电池负极的电极反应为:___________ ,当反应消耗 时,从理论上计算,外电路中通过电子的电量为
时,从理论上计算,外电路中通过电子的电量为___________ (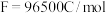 )。
)。
(4)用上述氨燃料电池接如图A、B两极(C、D、E、F都是惰性电极)。电源接通后,F电极附近溶液呈红色。
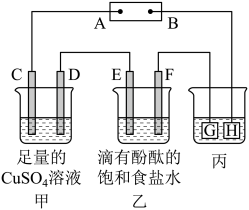
①甲池中C电极为___________ 极,乙池中发生的离子反应方程式为___________ 。
②丙装置是验证外加电流法对钢铁设备的保护(电解液为盐酸酸化的氯化钠溶液),钢铁应该接在___________ 处(填G或H)。为了证明铁能否被保护,可先取少量电解后的溶液于试管中,再向试管中加入___________ (填化学式)溶液,观察是否产生特征蓝色沉淀。
(1)下列化学方程式表示的化学反应能够设计成原电池的是___________
A.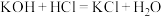 | B. |
C.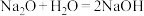 | D. |
(2)为了探究化学反应中的能量变化,某同学用相同的
 棒和相同浓度、相同体积的稀
棒和相同浓度、相同体积的稀 溶液,设计了两个实验(如下图)。有关实验现象,下列说法正确的是___________
溶液,设计了两个实验(如下图)。有关实验现象,下列说法正确的是___________
| A.消耗相同质量的Zn,图Ⅰ中产生的热能大于图Ⅱ |
| B.消耗相同质量的Zn,图Ⅰ中产生的热能等于图Ⅱ |
| C.图Ⅰ和图Ⅱ的锌棒表面均有大量气泡产生 |
| D.图Ⅱ中产生气体的速率比Ⅰ慢 |
Ⅱ.以氨气替代氢气研发氨燃料电池是当前科研的一个热点。
(3)氨燃料电池使用的电解质溶液是
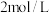 的
的 溶液,电池反应为:
溶液,电池反应为: ,该电池负极的电极反应为:
,该电池负极的电极反应为: 时,从理论上计算,外电路中通过电子的电量为
时,从理论上计算,外电路中通过电子的电量为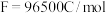 )。
)。(4)用上述氨燃料电池接如图A、B两极(C、D、E、F都是惰性电极)。电源接通后,F电极附近溶液呈红色。

①甲池中C电极为
②丙装置是验证外加电流法对钢铁设备的保护(电解液为盐酸酸化的氯化钠溶液),钢铁应该接在
您最近一年使用:0次
填空题
|
容易
(0.94)
解题方法
【推荐3】如何防止铁的锈蚀是工业上研究的重点内容。为研究铁的锈蚀,某同学做了探究实验,如下图所示,铁处于①、②、③三种不同的环境中。请回答:
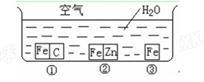
(1)铁被腐蚀的速率由快到慢的顺序是_____________________________ (填序号)。
(2)铁处于①环境时,正极反应式___________________________
(3)请你为以下钢铁制品选择适当的防锈方法。
①自行车的链条、齿轮___________________
②海水中的轮船___________________________

(1)铁被腐蚀的速率由快到慢的顺序是
(2)铁处于①环境时,正极反应式
(3)请你为以下钢铁制品选择适当的防锈方法。
①自行车的链条、齿轮
②海水中的轮船
您最近一年使用:0次
填空题
|
容易
(0.94)
名校
【推荐1】从海水中可以获得淡水、食盐,并可提取镁和溴等物质。
(1)从海水中提取镁的流程如图所示:
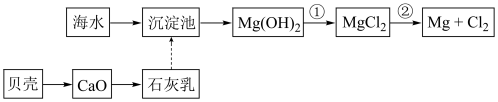
反应①的离子方程式为__ ;
反应②的化学方程式为__ ;
(2)海水提取溴流程:
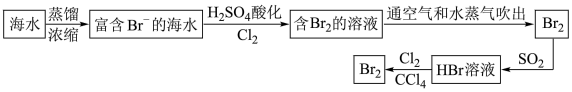
①该流程中涉及发生反应的离子方程式:__ ; ___ ;
②该流程中溴元素被氧化又被还原又被氧化的目的是:___ ;
③从最终溴的四氯化碳溶液中得到液溴,应采取的操作是__ 。
(1)从海水中提取镁的流程如图所示:

反应①的离子方程式为
反应②的化学方程式为
(2)海水提取溴流程:
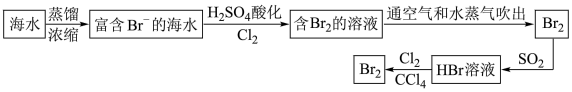
①该流程中涉及发生反应的离子方程式:
②该流程中溴元素被氧化又被还原又被氧化的目的是:
③从最终溴的四氯化碳溶液中得到液溴,应采取的操作是
您最近一年使用:0次
填空题
|
容易
(0.94)
解题方法
【推荐2】次磷酸钠(NaH2PO2)可用于化学镀镍。
(1)NaH2PO2中P元素的化合价为_____ 。
(2)化学镀镍的溶液中含有Ni2+和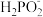 ,在酸性等条件下发生下述反应:
,在酸性等条件下发生下述反应:
(a)Ni2+ +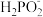 +→Ni +
+→Ni +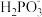 +
+
(b)6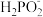 +2H+ = 2P+4
+2H+ = 2P+4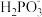 +3H2↑
+3H2↑
请写出并配平反应式(a)________ 。
(3)利用②中反应可在塑料镀件表面沉积镍—磷合金,从而达到化学镀镍的目的,这是一种常见的化学镀。请从以下方面比较化学镀与电镀。方法上的不同点:____________ ;原理上的不同点:__________ ;化学镀的优点:_______ 。
(1)NaH2PO2中P元素的化合价为
(2)化学镀镍的溶液中含有Ni2+和
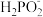 ,在酸性等条件下发生下述反应:
,在酸性等条件下发生下述反应: (a)Ni2+ +
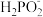 +→Ni +
+→Ni +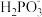 +
+ (b)6
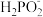 +2H+ = 2P+4
+2H+ = 2P+4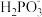 +3H2↑
+3H2↑请写出并配平反应式(a)
(3)利用②中反应可在塑料镀件表面沉积镍—磷合金,从而达到化学镀镍的目的,这是一种常见的化学镀。请从以下方面比较化学镀与电镀。方法上的不同点:
您最近一年使用:0次
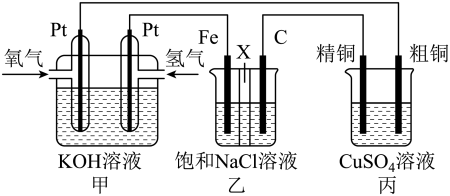
【推荐1】某同学设计一个燃料电池(如图所示),目的是探究氯碱工业原理和粗铜的精炼原理,其中乙装置中X为阳离子交换膜。根据要求回答相关问题:_______ (填“阳极”或“阴极”),反应一段时间后,在乙装置中滴入酚酞溶液,_______ (填“铁极”或“石墨极”)区的溶液先变红。乙池中电解总反应化学方程式_______ 。
(2)如果粗铜中含有锌、银等杂质,丙装置中反应一段时间,溶液中硫酸铜浓度将_______ (填“增大”“减小”或“不变”)。精铜电极上的电极反应式为_______ 。
(3)若在标准状况下,有224mL氧气参加反应,则乙装置中铁电极上生成的气体在标准状况下体积为_______ mL;丙装置中阴极析出铜的质量为_______ g。
(2)如果粗铜中含有锌、银等杂质,丙装置中反应一段时间,溶液中硫酸铜浓度将
(3)若在标准状况下,有224mL氧气参加反应,则乙装置中铁电极上生成的气体在标准状况下体积为
您最近一年使用:0次
填空题
|
容易
(0.94)
名校
【推荐2】如图装置所示,C、D、E、F、X、Y都是惰性电极,甲、乙中溶液的体积和浓度都相同(假设通电前后溶液体积不变),A、B为外接直流电源的两极.将直流电源接通后,F极附近呈红色.
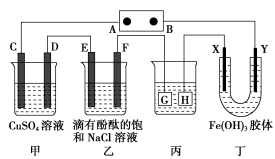
请回答:
(1)B极是电源的_______ ,一段时间后,甲中溶液颜色_______ ,丁中X极附近的颜色
逐渐变浅,Y极附近的颜色逐渐变深,这表明_______ ,在电场作用下向
Y极移动.
(2)现用丙装置给铜件镀银,则H应该是_______ (填“镀层金属”或“镀件”),电镀液
是_______ 溶液.当乙中溶液的pH是13时(此时乙溶液体积为500mL),甲中溶液的pH_______ (填“变大”、“变小”或“不变”),丙中镀件上析出银的质量为_______ .
(3)若甲、乙装置中的C、D、E、F电极均只有一种单质生成时,对应单质的物质的量之比为_______ .
(4)若将C电极换为铁,其他装置都不变,则甲中发生总反应的离子方程式是_______
(5)用甲装置电解100毫升0.2molAgNO3、0.4molCu(NO3)2、0.6molKCl的混合液,若在一极析出19.2gCu,在另一极产生的气体在标况下的体积为_______ L.

请回答:
(1)B极是电源的
逐渐变浅,Y极附近的颜色逐渐变深,这表明
Y极移动.
(2)现用丙装置给铜件镀银,则H应该是
是
(3)若甲、乙装置中的C、D、E、F电极均只有一种单质生成时,对应单质的物质的量之比为
(4)若将C电极换为铁,其他装置都不变,则甲中发生总反应的离子方程式是
(5)用甲装置电解100毫升0.2molAgNO3、0.4molCu(NO3)2、0.6molKCl的混合液,若在一极析出19.2gCu,在另一极产生的气体在标况下的体积为
您最近一年使用:0次
【推荐1】回答下列问题:
(1)以下合成材料制品中,属于塑料制品的是_______ ;属于橡胶制品的是_______ ;属于纤维制品的是_______ ;属于复合材料制品的是_______ 。
A.聚乙烯制品 B.汽车轮胎 C.玻璃钢 D.涤纶
(2)金属腐蚀的本质是金属原子失去电子_______ (填“被氧化”或“被还原”),生成阳离子的过程;在海水中为防止钢铁巨轮被腐蚀,常在轮船水面下的船体上焊上_______ (填“锌块”或“铜块”)。
(1)以下合成材料制品中,属于塑料制品的是
A.聚乙烯制品 B.汽车轮胎 C.玻璃钢 D.涤纶
(2)金属腐蚀的本质是金属原子失去电子
您最近一年使用:0次
填空题
|
容易
(0.94)
解题方法
【推荐2】钢铁是目前应用最广泛的金属材料,了解钢铁腐蚀的原因与防护方法具有重要意义,对钢铁制品进行抗腐蚀处理,可适当延长其使用寿命。
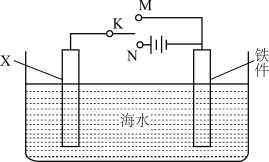
利用如图装置,可以模拟铁的电化学防护。
①若X为碳棒,为减缓铁件的腐蚀,开关K应置于________ 处。
②若X为锌,开关K置于M处,该电化学防护法称为_______ 。

利用如图装置,可以模拟铁的电化学防护。
①若X为碳棒,为减缓铁件的腐蚀,开关K应置于
②若X为锌,开关K置于M处,该电化学防护法称为
您最近一年使用:0次
填空题
|
容易
(0.94)
名校
【推荐3】依据《第四章化学反应与电能》所学知识填空。
(1)把___________ 的装置叫做电解池。
(2)金属冶炼就是使矿石中的金属离子___________ 的过程。
(3)金属与其表面接触的一些物质(如O2、Cl2、SO2等)___________ 而引起的腐蚀,叫做化学腐蚀。当___________ 时会发生原电池反应,比较活泼的金属发生氧化反应而被腐蚀,这种腐蚀叫做电化学腐蚀。
(4)由于条件不同,钢铁腐蚀可分为___________ 和___________ 。金属的防护措施包括改变金属材料的组成、___________ 、电化学保护法,其中电化学保护法包括___________ 和___________ 。
(1)把
(2)金属冶炼就是使矿石中的金属离子
(3)金属与其表面接触的一些物质(如O2、Cl2、SO2等)
(4)由于条件不同,钢铁腐蚀可分为
您最近一年使用:0次




