某天然碱可以看作是CO2 和 NaOH 反应后的产物组成的一种物质。为了研究该物质的组成,进行如下实验:
ⅰ称取 3.98 g 天然碱样品,加入 50mL 稀盐酸(足量),产生 CO2 896mL(标准状况)。
ⅱ称取 3.98g 天然碱样品,加热至分解完全,产生 CO2 224mL(标准状况)和 0.36g 水。
①该稀盐酸的物质的量浓度最小是_____________ 。
②天然碱的化学式是_____________ 。
ⅰ称取 3.98 g 天然碱样品,加入 50mL 稀盐酸(足量),产生 CO2 896mL(标准状况)。
ⅱ称取 3.98g 天然碱样品,加热至分解完全,产生 CO2 224mL(标准状况)和 0.36g 水。
①该稀盐酸的物质的量浓度最小是
②天然碱的化学式是
更新时间:2020-02-17 18:19:57
|
相似题推荐
计算题
|
适中
(0.65)
解题方法
【推荐1】在Na2CO3和NaHCO3混合溶液中缓慢滴加一定浓度的盐酸,测得溶液中 物质的量与所加盐酸体积之间的关系如图所示。
物质的量与所加盐酸体积之间的关系如图所示。
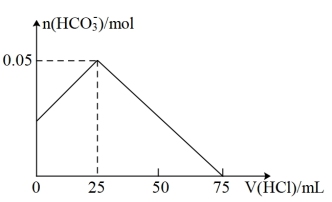
请回答下列问题:
(1)盐酸物质的量浓度为___________ mol/L。
(2)当滴入的盐酸体积为12.5 mL时,溶液中n( ):n(
):n( )为
)为___________ 。
 物质的量与所加盐酸体积之间的关系如图所示。
物质的量与所加盐酸体积之间的关系如图所示。
请回答下列问题:
(1)盐酸物质的量浓度为
(2)当滴入的盐酸体积为12.5 mL时,溶液中n(
 ):n(
):n( )为
)为
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】将一定质量Na2CO3和NaHCO3的均匀混合物分成等量的两份。将其中的一份直接加热至恒重,质量减轻了1.24 g;另一份加入一定量某浓度的盐酸至恰好反应完全,收集到标准状况下2.24 L 气体,消耗盐酸40.0 mL。试计算:
⑴原均匀混合物中NaHCO3的物质的量n(NaHCO3)=____ mol;
⑵盐酸的浓度c(HCl)=_____ mol·L-1。
⑴原均匀混合物中NaHCO3的物质的量n(NaHCO3)=
⑵盐酸的浓度c(HCl)=
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】天然碱是一种重要的矿物质,盛产于我国的青海湖地区。某天然碱样品的成分可以看成是碳酸钠、碳酸氢钠和水按物质的量之比1:1:2形成的结晶水合物。请回答下列问题:
(1)这种天然碱中碳酸钠、碳酸氢钠和水三者的质量比为___________ 。
(2)45.2 g此天然碱与100 mL密度为1.1 g/cm3的中等浓度盐酸恰好完全反应,产生a mol CO2,则a=_______ ,盐酸中溶质的质量分数ω(HCl)=_______ %。
(3)用一个化学方程式表示该天然碱与盐酸的反应:
___________________________ 。
(1)这种天然碱中碳酸钠、碳酸氢钠和水三者的质量比为
(2)45.2 g此天然碱与100 mL密度为1.1 g/cm3的中等浓度盐酸恰好完全反应,产生a mol CO2,则a=
(3)用一个化学方程式表示该天然碱与盐酸的反应:
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】称取铁粉和氧化铜的混合物6.40g,进行如下实验:
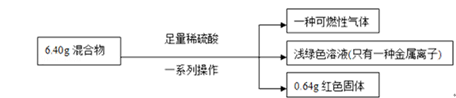
根据实验所得数据,完成下列填空:
(1)原混合物中氧化铜的质量能否确定?____________ (填“能”或“不能”),若能确定,则氧化铜的质量为_________ ;
(2)上述过程中生成气体的名称为_________ ;(折算为标准状况下)的体积为__________ ;
(3)实验中参加反应的硫酸的物质的量为____________ ;
(4)原混合物中铁的质量分数为________ 。

根据实验所得数据,完成下列填空:
(1)原混合物中氧化铜的质量能否确定?
(2)上述过程中生成气体的名称为
(3)实验中参加反应的硫酸的物质的量为
(4)原混合物中铁的质量分数为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐3】某学生在实验室里分析一瓶部分变质的氢氧化钠样品的组成。他先称取mg此样品倒入某容器,然后加入245g10%的稀硫酸,结果恰好完全反应,收集到8.8g气体;再取相同质量的该样品配成405.2g溶液,加入一定质量的熟石灰后也恰好完全反应。求:
(1)该样品的组成情况和m的值_______ ;
(2)405.2g该样品溶液与熟石灰反应后所得溶液的溶质质量分数_______ 。
(1)该样品的组成情况和m的值
(2)405.2g该样品溶液与熟石灰反应后所得溶液的溶质质量分数
您最近一年使用:0次



