高碘酸钠(NaIO4)是一种常用氧化剂。IO4-被I-还原为I2或IO3-的转化率与溶液pH的关系如图所示。
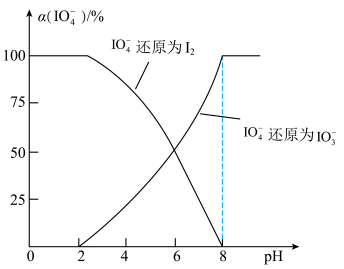
(1)写出pH≤2时,IO4-被I-还原的离子方程式:__ 。
(2)测定溶液中NaIO4浓度的实验步骤如下:准确量取25.00mL待测液,加入NaHCO3溶液调节pH至大于8,加入足量KI晶体,以淀粉作指示剂,用0.0500mol•L-1Na3AsO3溶液滴定至终点,消耗溶液体积12.50mL。
已知:AsO33-+I2+OH--AsO43-+I-+H2O(未配平)
①滴定终点的现象为___ 。
②若调节溶液pH<8,则会导致测得的IO4-的浓度__ (填“偏低”或“偏高”或“不变”)。
③计算溶液中NaIO4的物质的量浓度___ (写出计算过程)。

(1)写出pH≤2时,IO4-被I-还原的离子方程式:
(2)测定溶液中NaIO4浓度的实验步骤如下:准确量取25.00mL待测液,加入NaHCO3溶液调节pH至大于8,加入足量KI晶体,以淀粉作指示剂,用0.0500mol•L-1Na3AsO3溶液滴定至终点,消耗溶液体积12.50mL。
已知:AsO33-+I2+OH--AsO43-+I-+H2O(未配平)
①滴定终点的现象为
②若调节溶液pH<8,则会导致测得的IO4-的浓度
③计算溶液中NaIO4的物质的量浓度
更新时间:2020-02-27 12:53:44
|
【知识点】 探究物质组成或测量物质的含量解读
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】某同学为了测定某生铁(仅含C、Fe)中铁的质量分数,设计了如图所示的实验装置(夹持仪器已省略)和实验方案进行实验探究。
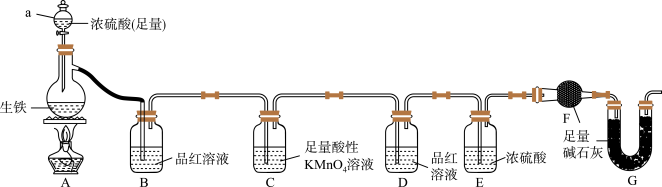
回答下列问题:
(1)仪器a的名称为_______ 。
(2)装置A中铁与浓硫酸发生反应的化学方程式为_______ 。
(3)装置B中产生的实验现象为_______ ,装置D的作用为_______ 。
(4)装置C用于吸收SO2,SO2转化为 ,MnO
,MnO 转化为Mn2+,写出该反应的离子方程式:
转化为Mn2+,写出该反应的离子方程式:_______ 。
(5)若无装置E,装置F吸收的物质为_______ (填化学式)。
(6)待mg生铁完全溶解后,停止加热,拆下装置F并称重。若装置F增重bg,则生铁中铁的质量分数为_______ (用含m、b的表达式表示)。

回答下列问题:
(1)仪器a的名称为
(2)装置A中铁与浓硫酸发生反应的化学方程式为
(3)装置B中产生的实验现象为
(4)装置C用于吸收SO2,SO2转化为
 ,MnO
,MnO 转化为Mn2+,写出该反应的离子方程式:
转化为Mn2+,写出该反应的离子方程式:(5)若无装置E,装置F吸收的物质为
(6)待mg生铁完全溶解后,停止加热,拆下装置F并称重。若装置F增重bg,则生铁中铁的质量分数为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】由硫铁矿烧渣(主要成分: 、
、 、
、 和
和 )得到绿矾
)得到绿矾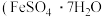 )的流程如图:
)的流程如图:

已知:① 难溶于水。且能还原
难溶于水。且能还原 ,硫元素被氧化成
,硫元素被氧化成 。
。
②金属离子生成氢氧化物沉淀的 见表:
见表:
(1)操作Ⅰ需要使用的玻璃仪器有_______ 。
(2)写出“还原”步骤中涉及的离子反应方程式_______ 。
(3)“除铝”与“还原”两步骤_______ (填“能”或“不能”)颠倒,原因是_______ 。
(4)试剂a最好选用下列试剂中的_______ (填字母代号),原因是_______ 。
A.热水 B.氯水 C.乙醇 D.饱和食盐水
(5)操作Ⅲ包含3个基本的实验操作,依次是_______ 。制得的绿矾需要减压烘干的原因是_______ 。
(6)测定所得绿矾晶体中铁元素的含量:称取样品mg于锥形瓶中,加水溶解后加稀硫酸酸化,用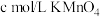 ,溶液滴定至终点,消耗
,溶液滴定至终点,消耗 溶液
溶液 。该晶体中铁的质量分数为
。该晶体中铁的质量分数为_______ 。
 、
、 、
、 和
和 )得到绿矾
)得到绿矾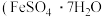 )的流程如图:
)的流程如图:
已知:①
 难溶于水。且能还原
难溶于水。且能还原 ,硫元素被氧化成
,硫元素被氧化成 。
。②金属离子生成氢氧化物沉淀的
 见表:
见表:| 金属离子 | 开始沉淀的pH | 沉淀完全的pH |
| Fe3+ | 1.1 | 3.2 |
| Al3+ | 3.0 | 5.0 |
| Fe2+ | 5.8 | 8.8 |
(2)写出“还原”步骤中涉及的离子反应方程式
(3)“除铝”与“还原”两步骤
(4)试剂a最好选用下列试剂中的
A.热水 B.氯水 C.乙醇 D.饱和食盐水
(5)操作Ⅲ包含3个基本的实验操作,依次是
(6)测定所得绿矾晶体中铁元素的含量:称取样品mg于锥形瓶中,加水溶解后加稀硫酸酸化,用
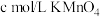 ,溶液滴定至终点,消耗
,溶液滴定至终点,消耗 溶液
溶液 。该晶体中铁的质量分数为
。该晶体中铁的质量分数为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】某研究小组模拟工业上以黄铁矿为原料制备硫酸的第一步反应如下:4FeS2+11O2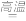 2Fe2O3+8SO2进行以下实验,并测定该样品中FeS2样品的纯度(假设其它杂质不参与反应)。
2Fe2O3+8SO2进行以下实验,并测定该样品中FeS2样品的纯度(假设其它杂质不参与反应)。
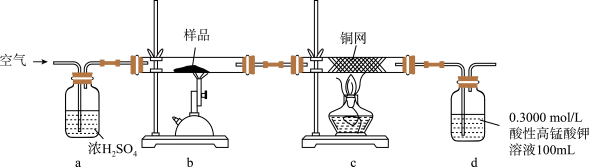
实验步骤:称取研细的样品4.000g放入上图b装置中,然后在空气中进行煅烧。为测定未反应高锰酸钾的量(假设其溶液体积保持不变),实验完成后取出d中溶液10mL置于锥形瓶里,用0.1000mol/L草酸(H2C2O4)标准溶液进行滴定。(已知:5SO2 + 2KMnO4 + 2H2O = K2SO4 + 2MnSO4 + 2H2SO4 )请回答下列问题:
(1)称量样品质量能否用托盘天平_______ (填“能”或“不能”),取出d中溶液10mL需要用______ 准确量取(填序号)
A.容量瓶 B.量筒 C.碱式滴定管 D.酸式滴定管
(2)上述反应结束后,仍需通一段时间的空气,其目的是__________
(3)已知草酸与高锰酸钾酸性溶液作用有CO2和Mn2+等物质生成,则滴定时发生反应的离子方程式为_______________ ﹔判断滴定到达终点的方法是___________ 。
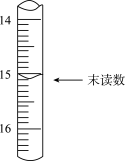
(4)已知滴定管初读数为0.10mL,末读数如图所示,消耗草酸溶液的体积为___________ mL。
下列操作会导致该样品中FeS2的纯度测定结果偏高的是_________ (填序号)
A.盛标准溶液的滴定管用蒸馏水洗涤后未用标准液润洗就装液滴定
B.锥形瓶用蒸馏水洗涤后未用待测液润洗
C.读取标准液读数时,滴定前平视,滴定到终点后俯视
D.滴定前滴定管尖嘴处有气泡未排除,滴定后气泡消失
(5)该样品中FeS2的纯度为__________________
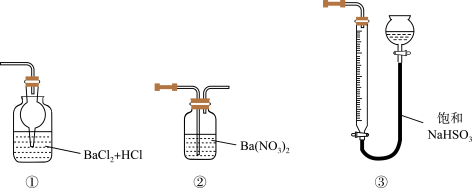
(6)若用下图装置替代上述实验装置d,同样可以达到实验目的的是_______ (填编号)。
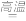 2Fe2O3+8SO2进行以下实验,并测定该样品中FeS2样品的纯度(假设其它杂质不参与反应)。
2Fe2O3+8SO2进行以下实验,并测定该样品中FeS2样品的纯度(假设其它杂质不参与反应)。
实验步骤:称取研细的样品4.000g放入上图b装置中,然后在空气中进行煅烧。为测定未反应高锰酸钾的量(假设其溶液体积保持不变),实验完成后取出d中溶液10mL置于锥形瓶里,用0.1000mol/L草酸(H2C2O4)标准溶液进行滴定。(已知:5SO2 + 2KMnO4 + 2H2O = K2SO4 + 2MnSO4 + 2H2SO4 )请回答下列问题:
(1)称量样品质量能否用托盘天平
A.容量瓶 B.量筒 C.碱式滴定管 D.酸式滴定管
(2)上述反应结束后,仍需通一段时间的空气,其目的是
(3)已知草酸与高锰酸钾酸性溶液作用有CO2和Mn2+等物质生成,则滴定时发生反应的离子方程式为
(4)已知滴定管初读数为0.10mL,末读数如图所示,消耗草酸溶液的体积为

下列操作会导致该样品中FeS2的纯度测定结果偏高的是
A.盛标准溶液的滴定管用蒸馏水洗涤后未用标准液润洗就装液滴定
B.锥形瓶用蒸馏水洗涤后未用待测液润洗
C.读取标准液读数时,滴定前平视,滴定到终点后俯视
D.滴定前滴定管尖嘴处有气泡未排除,滴定后气泡消失
(5)该样品中FeS2的纯度为
(6)若用下图装置替代上述实验装置d,同样可以达到实验目的的是

您最近一年使用:0次



