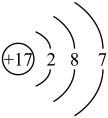
有几种元素的微粒的电子层结构为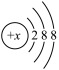 ,试回答下列问题:
,试回答下列问题:
(1)若该微粒代表一种原子,则这种微粒的符号是______ ;
(2)向该微粒(带负电荷)的盐溶液中加入 溶液时会出现白色沉淀,则这种微粒的符号是
溶液时会出现白色沉淀,则这种微粒的符号是______ ;
(3)某原子失去一个电子形成该微粒,则这种微粒的符号是______ ;
(4)某原子得到两个电子形成该微粒,则这种微粒的符号是______ 。
 ,试回答下列问题:
,试回答下列问题:(1)若该微粒代表一种原子,则这种微粒的符号是
(2)向该微粒(带负电荷)的盐溶液中加入
 溶液时会出现白色沉淀,则这种微粒的符号是
溶液时会出现白色沉淀,则这种微粒的符号是(3)某原子失去一个电子形成该微粒,则这种微粒的符号是
(4)某原子得到两个电子形成该微粒,则这种微粒的符号是
19-20高一·全国·课后作业 查看更多[4]
(已下线)【定心卷】4.1.1 原子结构随堂练习-人教版2023-2024学年必修第一册新疆哈密市第八中学2022-2023学年高一上学期期末考试化学试题鲁科版(2019)必修第二册第一章第1节 易错疑难集训第1章原子结构与元素周期律第1节易错疑难集训(一)
更新时间:2020-03-02 14:34:56
|
相似题推荐
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】为纪念元素周期表诞生150周年,IUPAC等向世界介绍118位优秀青年化学家,并形成一张“青年化学家元素周期类”。中国学者雷晓光、姜雪峰、刘庄分别成为“N、S、Hg”元素的代言人。回答下列问题:
(1)请补全汞的原子结构示意图___________ 。
(2)自然界的水银内含7种核素: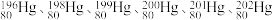 和
和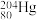 ,其中,
,其中,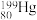 和
和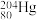 的中子数之比为
的中子数之比为___________ 。
(3)硫磺可用于制作黑火药,爆炸时的反应为: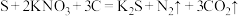 。
。
①上述反应所涉及元素中,某元素原子得到两个电子即可形成2、8的电子层结构,该元素的名称是___________ ,它与氢形成的10电子微粒有___________ 种;某元素的 层电子数是其电子总数的
层电子数是其电子总数的 ,则其简单离子的电子式为
,则其简单离子的电子式为___________ 。
②已知一般情况下原子核外最外层电子数相等的元素具有相似的化学性质。下列原子中与钾元素原子的化学性质相似的是___________ 。
(4)高纯度陶瓷氮化硅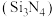 可由石英与焦炭在高温的氮气流中通过所给反应得到:
可由石英与焦炭在高温的氮气流中通过所给反应得到:
①反应后恢复至室温,得到混合气体的平均相对分子质量为___________ 。
②若反应生成 气体(标准状况),则生成的
气体(标准状况),则生成的 质量为
质量为___________ (保留两位小数)。
(1)请补全汞的原子结构示意图

(2)自然界的水银内含7种核素:
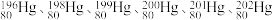 和
和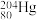 ,其中,
,其中,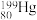 和
和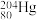 的中子数之比为
的中子数之比为(3)硫磺可用于制作黑火药,爆炸时的反应为:
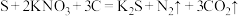 。
。①上述反应所涉及元素中,某元素原子得到两个电子即可形成2、8的电子层结构,该元素的名称是
 层电子数是其电子总数的
层电子数是其电子总数的 ,则其简单离子的电子式为
,则其简单离子的电子式为②已知一般情况下原子核外最外层电子数相等的元素具有相似的化学性质。下列原子中与钾元素原子的化学性质相似的是
 |  | 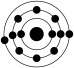 | 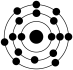 |
| A. | B. | C. | D. |
(4)高纯度陶瓷氮化硅
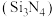 可由石英与焦炭在高温的氮气流中通过所给反应得到:
可由石英与焦炭在高温的氮气流中通过所给反应得到:
①反应后恢复至室温,得到混合气体的平均相对分子质量为
②若反应生成
 气体(标准状况),则生成的
气体(标准状况),则生成的 质量为
质量为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】原子序数为11~17的元素符号和原子结构示意图如下。
 Na
Na  Mg
Mg  Al
Al  Si
Si P
P  S
S  Cl
Cl
(1)原子序数为15的原子质子数为____ ,最外层有____ 个电子。
(2)结合上图用符号表示下列内容:
①原子序数为13的原子形成的简单离子符号为____ 。
②一个单质分子中含有两个原子的物质的化学式为____ 。
③原子序数为12、17的元素组成化合物的化学式为____ 。
(3)原子序数为11~17的元素,随着原子序数的增加,其原子结构或元素的性质呈现出的变化规律是_____________________ 。(任写一条)
 Na
Na  Mg
Mg  Al
Al  Si
Si P
P  S
S  Cl
Cl(1)原子序数为15的原子质子数为
(2)结合上图用符号表示下列内容:
①原子序数为13的原子形成的简单离子符号为
②一个单质分子中含有两个原子的物质的化学式为
③原子序数为12、17的元素组成化合物的化学式为
(3)原子序数为11~17的元素,随着原子序数的增加,其原子结构或元素的性质呈现出的变化规律是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】硅是地壳中含量第二大的元素,其单质是一种重要的半导体材料。
(1) 是硅的一种同位素,该
是硅的一种同位素,该 原子的中子数为
原子的中子数为_______ 。
(2)硅元素在自然界中通常以石英石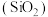 和硅酸盐的形式存在。已知
和硅酸盐的形式存在。已知 是一种酸性氧化物,请写出其与氢氧化钠溶液反应的离子方程式
是一种酸性氧化物,请写出其与氢氧化钠溶液反应的离子方程式_______ 。
(3)关于硅及其相关化合物的叙述正确的是_______(填字母)。
(4)高纯硅单质可由石英砂(主要成分是 )制得,制备高纯硅的主要工艺流程如图所示:
)制得,制备高纯硅的主要工艺流程如图所示:_______ ;
ⅱ.流程④的化学反应为置换反应,写出其化学方程式:_______ 。
(1)
 是硅的一种同位素,该
是硅的一种同位素,该 原子的中子数为
原子的中子数为(2)硅元素在自然界中通常以石英石
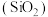 和硅酸盐的形式存在。已知
和硅酸盐的形式存在。已知 是一种酸性氧化物,请写出其与氢氧化钠溶液反应的离子方程式
是一种酸性氧化物,请写出其与氢氧化钠溶液反应的离子方程式(3)关于硅及其相关化合物的叙述正确的是_______(填字母)。
| A.自然界中存在天然游离的硅单质 |
B.已知C与 的最高正价都是正四价,由于 的最高正价都是正四价,由于 ,用类比法得知, ,用类比法得知,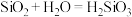 |
C.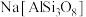 用氧化物形式表示为 用氧化物形式表示为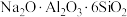 |
D. 既能和 既能和 溶液反应,又能和氢氟酸反应,所以是两性氧化物 溶液反应,又能和氢氟酸反应,所以是两性氧化物 |
 )制得,制备高纯硅的主要工艺流程如图所示:
)制得,制备高纯硅的主要工艺流程如图所示:
ⅱ.流程④的化学反应为置换反应,写出其化学方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】科学家们用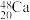 原子轰击某种铬原子,得到了
原子轰击某种铬原子,得到了 原子。
原子。
(1)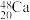 原子的核外电子数是
原子的核外电子数是_______ ,中子数是_______ 。
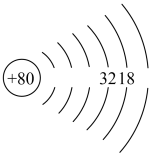
(2) 的原子结构示意图是
的原子结构示意图是 ,其中的x=
,其中的x=_______ ,y=_______ 。 位于元素周期表的第
位于元素周期表的第_______ 周期,第_______ 族,与它属于同族的一种元素是_______ 。
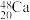 原子轰击某种铬原子,得到了
原子轰击某种铬原子,得到了 原子。
原子。(1)
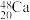 原子的核外电子数是
原子的核外电子数是(2)
 的原子结构示意图是
的原子结构示意图是 ,其中的x=
,其中的x= 位于元素周期表的第
位于元素周期表的第
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】用A+、B-、C2-、D、E、F、G和H分别表示含有18个电子的八种微粒(离子或分子),请回答下列问题:
(1)A元素是_______ 、B元素是_______ 、C元素是_______ (用元素符号表示)。
(2)D是由两种元素组成的双原子分子,其分子式是_______ 。
(3)E是所有含18个电子的微粒中氧化能力最强的分子,其分子式是_______ 。
(4)F是由两种元素组成的三原子分子,其分子式是_______ 。
(5)G分子中含有4个原子,其分子式是_______ 。
(6)H分子中含有8个原子,其分子式是_______ 。
(1)A元素是
(2)D是由两种元素组成的双原子分子,其分子式是
(3)E是所有含18个电子的微粒中氧化能力最强的分子,其分子式是
(4)F是由两种元素组成的三原子分子,其分子式是
(5)G分子中含有4个原子,其分子式是
(6)H分子中含有8个原子,其分子式是
您最近一年使用:0次
【推荐2】画出下列各微粒的结构示意图:
(1)与氖原子电子层结构相同的-2价阴离子:_____________ 。
(2)最外层电子数为次外层电子数2倍的原子:________________ 。
(3)第2层电子数为第1层、第3层电子数之和的原子:________ 。
(4)观察下列A、B、C、D、E五种粒子(原子或离子)的结构示意图,回答有关问题:

①属于离子结构示意图的是_____ (填编号)。
②属于金属元素的是___ (填编号)
③性质最稳定的原子是(填写编号,下同)______ ,最容易失去电子的原子是____ ,最容易得到电子的原子是________ 。
④A在周期表中的位置_____ 周期______ 族。
(1)与氖原子电子层结构相同的-2价阴离子:
(2)最外层电子数为次外层电子数2倍的原子:
(3)第2层电子数为第1层、第3层电子数之和的原子:
(4)观察下列A、B、C、D、E五种粒子(原子或离子)的结构示意图,回答有关问题:

①属于离子结构示意图的是
②属于金属元素的是
③性质最稳定的原子是(填写编号,下同)
④A在周期表中的位置
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】全氮类物质因具有超高能量而成为超高含能材料的典型代表。我国科学家成功合成了全氮阴离子盐——(N5)6(H3O)3(NH4)4Cl,是该领域的重大突破。
(1)氮的原子结构示意图为________ 。
(2)构成该全氮阴离子盐的离子是Cl-、H3O+、NH4+和________ 。
(3)氯与氢之间的作用对全氮阴离子盐的稳定性起着至关重要的作用。结合原子结构解释氯元素非金属性强的原因:________ 。
(1)氮的原子结构示意图为
(2)构成该全氮阴离子盐的离子是Cl-、H3O+、NH4+和
(3)氯与氢之间的作用对全氮阴离子盐的稳定性起着至关重要的作用。结合原子结构解释氯元素非金属性强的原因:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】下列各项决定于原子结构的哪一部分:①质子数,②中子数,③原子的最外层电子数。(以下各项选择序号填空)
(1)元素的种类取决于____________ ;
(2)原子的质量数主要由______________ 决定;
(3)元素的化学性质主要由____________ 决定。
(1)元素的种类取决于
(2)原子的质量数主要由
(3)元素的化学性质主要由
您最近一年使用:0次

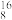 O2、
O2、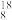 O2、
O2、 H、
H、 C、
C、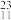 Na、
Na、 N、
N、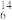 C、
C、 Mg。
Mg。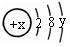 试回答:
试回答: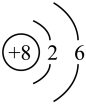 B.
B. C.
C.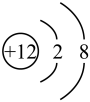 D.
D.