31.2g镁与碳粉的混合物在一定条件下恰好完全反应,再加入足量水,得到40.6g白色沉淀,同时产生密度为1.4107g/L(标准状况)的丙二烯和不饱和烃X的混合气体。
(1)镁与碳粉的反应产物的化学式为___________________ 。
(2)原混合物中碳粉的物质的量分数为___________ 。(用小数表示,保留2位小数)
(1)镁与碳粉的反应产物的化学式为
(2)原混合物中碳粉的物质的量分数为
2014·上海·零模 查看更多[1]
(已下线)上海市十三校2014届高三3月第二次联考化学试题
更新时间:2020-03-24 11:13:18
|
相似题推荐
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】(1)2.8g铁在足量的Cl2中燃烧转移的电子的物质的量为____________ 。
(2)1.7gNH3与____________ gNa+含有相同数目的电子。
(3)当0.1mol钠与足量的水反应时生成的H2的质量为____________ g。
(4)设阿伏加德罗常数为NA,标准状况下mg某气体A含有b个分子,则ng该混合气体的物质的量为____________ mol。
(5)假定把12C的相对原子质量定为24,把24克12C所含的原子数定为阿伏加德罗常数,而摩尔的定义不变,则下列推断不正确的是____________
A.此时氧O的相对原子质量为32,
B.44g二氧化碳的物质的量为0.5mol
C.NA个氧分子与NA个氢分子质量之比为16∶1
D.CO的摩尔质量为56g·mol-1
E.0.5molO2的质量为16克
(2)1.7gNH3与
(3)当0.1mol钠与足量的水反应时生成的H2的质量为
(4)设阿伏加德罗常数为NA,标准状况下mg某气体A含有b个分子,则ng该混合气体的物质的量为
(5)假定把12C的相对原子质量定为24,把24克12C所含的原子数定为阿伏加德罗常数,而摩尔的定义不变,则下列推断不正确的是
A.此时氧O的相对原子质量为32,
B.44g二氧化碳的物质的量为0.5mol
C.NA个氧分子与NA个氢分子质量之比为16∶1
D.CO的摩尔质量为56g·mol-1
E.0.5molO2的质量为16克
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】某校在国际禁毒日的宣传板报上有这样一则内容:

“摇头丸”是一种人工合成毒品,具有兴奋和致幻作用,会严重破坏人体的中枢神经,具有很强的精神依赖性,上瘾后难以戒断。合成“摇头丸”的一种重要物质为苯丙胺。
(1)苯丙胺的摩尔质量为多少______ ?
(2)0.5mol苯丙胺分子中含有多少个氢原子______ ?
(3)270g苯丙胺的物质的量是多少______ ?其中含有碳元素的质量是多少______ ?

“摇头丸”是一种人工合成毒品,具有兴奋和致幻作用,会严重破坏人体的中枢神经,具有很强的精神依赖性,上瘾后难以戒断。合成“摇头丸”的一种重要物质为苯丙胺。
(1)苯丙胺的摩尔质量为多少
(2)0.5mol苯丙胺分子中含有多少个氢原子
(3)270g苯丙胺的物质的量是多少
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】为测定CuSO4溶液的浓度,甲、乙两同学设计了两个方案。回答下列问题:
(1)甲方案
实验原理:CuSO4+BaCl2=BaSO4↓+CuCl2
实验步骤:__________________ mol·L-1。
(2)乙方案,实验装置如图:________ mol·L-1(列出计算表达式)。
(1)甲方案
实验原理:CuSO4+BaCl2=BaSO4↓+CuCl2
实验步骤:
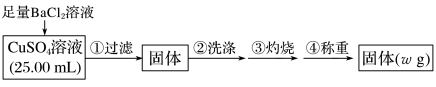
(2)乙方案,实验装置如图:

您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐2】铁的某种氯化物FeClx质量为1.625 g溶于水后,加入足量的AgNO3溶液,产生的沉淀经洗涤干燥后称得质量为4.305 g。求x的值和铁的氯化物的化学式______ 、_______ 。
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐3】现有等物质的量的NaHCO3和KHCO3的混合物ag与100mL盐酸反应,题中设计的气体体积均以标准状况计,填空时可以用带字母的公式表示。
(1)该混合物中NaHCO3和KHCO3的质量比为:____ 。
(2)如碳酸氢盐与盐酸恰好完全反应则盐酸的浓度为:____ 。
(3)如盐酸过量,生成CO2的体积为:____ 。
(4)如果反应后碳酸氢盐有剩余,盐酸不足量要计算生成的CO2的体积,还需知道:____ 。
(5)若NaHCO3和KHCO3不是以等物质的量混合,则ag固体混合物与足量的盐酸完全反应时生成CO2的体积范围是:____ 。
(1)该混合物中NaHCO3和KHCO3的质量比为:
(2)如碳酸氢盐与盐酸恰好完全反应则盐酸的浓度为:
(3)如盐酸过量,生成CO2的体积为:
(4)如果反应后碳酸氢盐有剩余,盐酸不足量要计算生成的CO2的体积,还需知道:
(5)若NaHCO3和KHCO3不是以等物质的量混合,则ag固体混合物与足量的盐酸完全反应时生成CO2的体积范围是:
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】将一定质量 和
和 的均匀混合物分成等量的两份,将其中的一份直接加热至恒重,质量减轻了1.24g:另一份加入一定量某浓度的盐酸至恰好反应完全,收集到标准状况下2.241L气体,消耗盐酸40.0mL,试计算:
的均匀混合物分成等量的两份,将其中的一份直接加热至恒重,质量减轻了1.24g:另一份加入一定量某浓度的盐酸至恰好反应完全,收集到标准状况下2.241L气体,消耗盐酸40.0mL,试计算:
(1)原均匀混合物中 的物质的量
的物质的量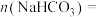
_____  。
。
(2)盐酸的浓度
_____  。
。
 和
和 的均匀混合物分成等量的两份,将其中的一份直接加热至恒重,质量减轻了1.24g:另一份加入一定量某浓度的盐酸至恰好反应完全,收集到标准状况下2.241L气体,消耗盐酸40.0mL,试计算:
的均匀混合物分成等量的两份,将其中的一份直接加热至恒重,质量减轻了1.24g:另一份加入一定量某浓度的盐酸至恰好反应完全,收集到标准状况下2.241L气体,消耗盐酸40.0mL,试计算:(1)原均匀混合物中
 的物质的量
的物质的量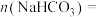
 。
。(2)盐酸的浓度

 。
。
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】一定量的Na2CO3和NaHCO3的均匀混合物分成质量不等的三份,分别与50mL相同浓度的盐酸反应,得到气体的质量与固体混合物的质量关系如下表所示:
(1)上表中_______ 组数据表明盐酸参加反应后有剩余,理由是______________ 。
(2)上表中第2组数据中盐酸____________ (填“过量”、“适量”、“不足量”)。
(3)通过计算求Na2CO3和NaHCO3的质量分数各为_________ 、____________ 。
| 组 别 | 1 | 2 | 3 |
| 固体质量/g | 3.80 | 6.20 | 7.20 |
| 气体质量/g | 1.76 | 2.64 | 2.64 |
(1)上表中
(2)上表中第2组数据中盐酸
(3)通过计算求Na2CO3和NaHCO3的质量分数各为
您最近一年使用:0次
【推荐3】回答下列问题:
(1)在一定条件下,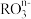 和氟气可发生如下反应
和氟气可发生如下反应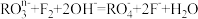 从而可知在
从而可知在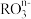 中,元素R的化合价为
中,元素R的化合价为_______ 。
(2)若在标准状况下,将VLHCl气体溶于1L水中,所得溶液密度为dg/L,则此溶液的物质的量浓度为_______ mol/L。(用含V,d字母的算式表示)
(3)某学生用 和
和 组成的均匀混合物进行以下实验。(气体体积已折算成标准状况下的体积,不考虑
组成的均匀混合物进行以下实验。(气体体积已折算成标准状况下的体积,不考虑 在水中的溶解,不考虑HCl的挥发)
在水中的溶解,不考虑HCl的挥发)
实验1:取2.96g固体混合物加入质量分数为12.0%,密度为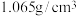 的盐酸40mL共产生672mL气体。
的盐酸40mL共产生672mL气体。
实验2:取8.88g该固体混合物逐滴加入40mL该盐酸,则产生amL的气体。
①盐酸的物质的量浓度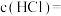
_______ (保留两位小数)。
②样品中物质的量之比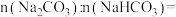
_______ 。
③a=_______ mL。
(1)在一定条件下,
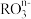 和氟气可发生如下反应
和氟气可发生如下反应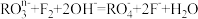 从而可知在
从而可知在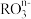 中,元素R的化合价为
中,元素R的化合价为(2)若在标准状况下,将VLHCl气体溶于1L水中,所得溶液密度为dg/L,则此溶液的物质的量浓度为
(3)某学生用
 和
和 组成的均匀混合物进行以下实验。(气体体积已折算成标准状况下的体积,不考虑
组成的均匀混合物进行以下实验。(气体体积已折算成标准状况下的体积,不考虑 在水中的溶解,不考虑HCl的挥发)
在水中的溶解,不考虑HCl的挥发)实验1:取2.96g固体混合物加入质量分数为12.0%,密度为
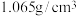 的盐酸40mL共产生672mL气体。
的盐酸40mL共产生672mL气体。实验2:取8.88g该固体混合物逐滴加入40mL该盐酸,则产生amL的气体。
①盐酸的物质的量浓度
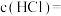
②样品中物质的量之比
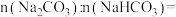
③a=
您最近一年使用:0次
计算题
|
适中
(0.65)
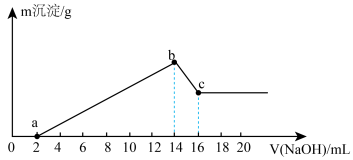
【推荐1】将一定质量的镁铝合金投入100 mL一定物质的量浓度的盐酸中,合金全部溶解,向所得溶液中滴加5 mol/L的NaOH溶液至过量,生成沉淀的质量与加入的氢氧化钠溶液的体积关系如图所示。回答下列问题:

(1)当沉淀量达到最大值时,Al(OH)3的物质的量为________ 。
(2)原合金中Mg的质量为________ 。
(3)盐酸的物质的量浓度为________ 。

(1)当沉淀量达到最大值时,Al(OH)3的物质的量为
(2)原合金中Mg的质量为
(3)盐酸的物质的量浓度为
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】金属及其化合物变化多,用途广。请完成下列计算:
(1)等物质的量的镁在氧气中充分灼烧,产物质量为a g,比它在空气中灼烧所得产物增重b g。它在空气中灼烧后的产物中Mg3N2的质量分数是________________ (用a、b表示,只考虑空气中氮气、氧气参与反应)。
(2)硬铝(因其主要成分,在此仅看作Al-Cu合金)常用于建筑装潢。1.18g某种硬铝恰好与10mL某浓度的硝酸完全反应,生成的混合气体(其中NO2与NO的体积比为2:1)再与448mL氧气(标准状况)混合,恰好能被水完全吸收。
①计算该硝酸的物质的量浓度__________ 。
②计算并确定此种硬铝的化学式__________ 。
(3)取5.1g Al-Mg合金与200mL 1mol·L-1的NaOH(aq)充分反应,产生气体a L。过滤,向滤液中通入V L CO2后开始出现沉淀,继续通入CO2使沉淀完全。过滤、洗涤、干燥、灼烧,得到固体5.1 g。则a =_______ ,V =________ 。(气体体积均为标准状况)
(4)向Cu、Cu2O和CuO的混合粉末中加入500mL 0.6 mol·L-1HNO3(aq),恰好完全溶解,同时收集到1120 mL NO(标准状况)。通过计算推断混合粉末中Cu的物质的量_____ 。
(1)等物质的量的镁在氧气中充分灼烧,产物质量为a g,比它在空气中灼烧所得产物增重b g。它在空气中灼烧后的产物中Mg3N2的质量分数是
(2)硬铝(因其主要成分,在此仅看作Al-Cu合金)常用于建筑装潢。1.18g某种硬铝恰好与10mL某浓度的硝酸完全反应,生成的混合气体(其中NO2与NO的体积比为2:1)再与448mL氧气(标准状况)混合,恰好能被水完全吸收。
①计算该硝酸的物质的量浓度
②计算并确定此种硬铝的化学式
(3)取5.1g Al-Mg合金与200mL 1mol·L-1的NaOH(aq)充分反应,产生气体a L。过滤,向滤液中通入V L CO2后开始出现沉淀,继续通入CO2使沉淀完全。过滤、洗涤、干燥、灼烧,得到固体5.1 g。则a =
(4)向Cu、Cu2O和CuO的混合粉末中加入500mL 0.6 mol·L-1HNO3(aq),恰好完全溶解,同时收集到1120 mL NO(标准状况)。通过计算推断混合粉末中Cu的物质的量
您最近一年使用:0次

 的物质的量是
的物质的量是