实验室利用铜屑、硝酸和硫酸的混酸为原料制备硫酸铜晶体。结合具体操作过程回答下列问题。
(1)配制混酸:将3 mol/L的硫酸(密度1.180g/cm3)与15mol/L的浓硝酸(密度1.400 g/cm3)按体积比5:1混合后冷却。
①计算混酸中硫酸的质量分数为__________ ;
②取1g混酸,用水稀释至20.00mL,用0.5mol/L烧碱进行滴定,消耗标准烧碱溶液的体积为__________ mL。
(2)灼烧废铜屑:称量一定质量表面含油污的纯铜屑(铜含量为99.84%),置于坩埚中灼烧,将油污充分氧化后除去,直至铜屑表面均呈黑色。冷却后称量,固体质量比灼烧前增加了3.2 %,
①固体中氧元素的质量分数为__________ (保留3位小数);
②固体中铜与氧化铜的物质的量之比为___________ 。
(3)溶解:称取2.064g固体,慢慢分批加入一定质量的混酸,恰好完全反应。列式计算产生NO气体体积在标准状况下的体积(设硝酸的还原产物只有NO)。______________
(4)结晶:将反应后的溶液水浴加热浓缩后冷却结晶,析出胆矾晶体。
①计算反应后溶液中CuSO4的物质的量是__________ ;
②若最终得到胆矾晶体质量为6.400g,胆矾的产率为_________ 。(精确到1%)
(1)配制混酸:将3 mol/L的硫酸(密度1.180g/cm3)与15mol/L的浓硝酸(密度1.400 g/cm3)按体积比5:1混合后冷却。
①计算混酸中硫酸的质量分数为
②取1g混酸,用水稀释至20.00mL,用0.5mol/L烧碱进行滴定,消耗标准烧碱溶液的体积为
(2)灼烧废铜屑:称量一定质量表面含油污的纯铜屑(铜含量为99.84%),置于坩埚中灼烧,将油污充分氧化后除去,直至铜屑表面均呈黑色。冷却后称量,固体质量比灼烧前增加了3.2 %,
①固体中氧元素的质量分数为
②固体中铜与氧化铜的物质的量之比为
(3)溶解:称取2.064g固体,慢慢分批加入一定质量的混酸,恰好完全反应。列式计算产生NO气体体积在标准状况下的体积(设硝酸的还原产物只有NO)。
(4)结晶:将反应后的溶液水浴加热浓缩后冷却结晶,析出胆矾晶体。
①计算反应后溶液中CuSO4的物质的量是
②若最终得到胆矾晶体质量为6.400g,胆矾的产率为
2013·上海·零模 查看更多[2]
更新时间:2020-03-30 21:43:10
|
相似题推荐
计算题
|
困难
(0.15)
解题方法
【推荐1】化学正在走向精准。当代化学的三大支柱是:理论、实验和计算。
Ⅰ.某溶液为硫酸和硝酸混合后的稀溶液,取200.00mL,该溶液加入过量锌粉充分反应。反应后溶液中只含有一种溶质,其浓度为 (溶液体积不变),收集到无色气体6.72L(标准状况),请列式计算溶液中硫酸和硝酸的浓度比,及产生的氢气的体积(标准状况)。
(溶液体积不变),收集到无色气体6.72L(标准状况),请列式计算溶液中硫酸和硝酸的浓度比,及产生的氢气的体积(标准状况)。______
Ⅱ.某硫铜矿的主要成分为 ,可用于冶炼金属铜,为测定矿石中
,可用于冶炼金属铜,为测定矿石中 的质量分数,进行如下实验(杂质不参加反应):
的质量分数,进行如下实验(杂质不参加反应):
步骤1:在1.00g试样中加入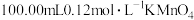 的酸性溶液,加热,硫元素全部转化为
的酸性溶液,加热,硫元素全部转化为 ,铜元素全部转化为
,铜元素全部转化为 ,滤去不溶性杂质。
,滤去不溶性杂质。
步骤2:收集步骤1所得滤液至250mL容量瓶中,定容。取25.00mL溶液,用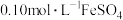 溶液与剩余
溶液与剩余 恰好反应,消耗10.00mL。列式计算
恰好反应,消耗10.00mL。列式计算 的质量分数
的质量分数______ 。
Ⅰ.某溶液为硫酸和硝酸混合后的稀溶液,取200.00mL,该溶液加入过量锌粉充分反应。反应后溶液中只含有一种溶质,其浓度为
 (溶液体积不变),收集到无色气体6.72L(标准状况),请列式计算溶液中硫酸和硝酸的浓度比,及产生的氢气的体积(标准状况)。
(溶液体积不变),收集到无色气体6.72L(标准状况),请列式计算溶液中硫酸和硝酸的浓度比,及产生的氢气的体积(标准状况)。Ⅱ.某硫铜矿的主要成分为
 ,可用于冶炼金属铜,为测定矿石中
,可用于冶炼金属铜,为测定矿石中 的质量分数,进行如下实验(杂质不参加反应):
的质量分数,进行如下实验(杂质不参加反应):步骤1:在1.00g试样中加入
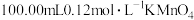 的酸性溶液,加热,硫元素全部转化为
的酸性溶液,加热,硫元素全部转化为 ,铜元素全部转化为
,铜元素全部转化为 ,滤去不溶性杂质。
,滤去不溶性杂质。步骤2:收集步骤1所得滤液至250mL容量瓶中,定容。取25.00mL溶液,用
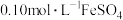 溶液与剩余
溶液与剩余 恰好反应,消耗10.00mL。列式计算
恰好反应,消耗10.00mL。列式计算 的质量分数
的质量分数
您最近一年使用:0次
【推荐2】钾元素可以与氧元素在不同条件下生成K2O2、KO2和KO3,如: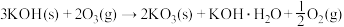
(1)KOH与O3反应,反应前后气体体积减小67.2L(S.T.P.),则生成KO3__________ g。
(2)将上述生成的混和物用液氨冷却结晶,可得到KO3晶体。它会缓慢分解为KO2和O2; .已知分解后残留固体中含氧的质量分数为0.5063,则KO3的分解百分率为
.已知分解后残留固体中含氧的质量分数为0.5063,则KO3的分解百分率为_____ 。(保留两位小数)
(3)已知某样品中含有K2O2、KO2和KO3中的两种,把71.1g该样品加入过量的Al2(SO4)3溶液中,产生白色沉淀23.4g。
①该样品中钾原子与氧原子个数的最简整数比为_______ 。(写出计算过程)
②写出可能存在的组合中两种化合物的物质的量之比_________ 。
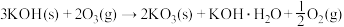
(1)KOH与O3反应,反应前后气体体积减小67.2L(S.T.P.),则生成KO3
(2)将上述生成的混和物用液氨冷却结晶,可得到KO3晶体。它会缓慢分解为KO2和O2;
 .已知分解后残留固体中含氧的质量分数为0.5063,则KO3的分解百分率为
.已知分解后残留固体中含氧的质量分数为0.5063,则KO3的分解百分率为(3)已知某样品中含有K2O2、KO2和KO3中的两种,把71.1g该样品加入过量的Al2(SO4)3溶液中,产生白色沉淀23.4g。
①该样品中钾原子与氧原子个数的最简整数比为
②写出可能存在的组合中两种化合物的物质的量之比
您最近一年使用:0次
计算题
|
困难
(0.15)
解题方法
【推荐3】将20g某铁矿石(设只含铁的氧化物和杂质SiO2)溶于过量的稀盐酸,过滤后得5.6g不溶物和滤液;然后在滤液中加入足量的NaOH溶液,过滤后将沉淀灼烧,得16g红棕色固体。
(1)红棕色固体的化学式是____________________ ,其中的n(Fe)=____________________ mol。
(2)请计算(写出计算过程):
①该矿石中铁氧化物的化学式____________________ 。
②若加入的稀盐酸为4.0mol·L -1200mL,反应前后体积变化忽略不计,则滤液中剩余H+的物质的量浓度是多少?____________________
(1)红棕色固体的化学式是
(2)请计算(写出计算过程):
①该矿石中铁氧化物的化学式
②若加入的稀盐酸为4.0mol·L -1200mL,反应前后体积变化忽略不计,则滤液中剩余H+的物质的量浓度是多少?
您最近一年使用:0次




