某溶液A中可能含有NO3-、CO32-、SO32-、SO42-、NH4+、Fe2+、Al3+、Fe3+中的几种离子,且溶液中各离子的物质的量浓度均为0.1 mol/L。现取100 mL该溶液A进行如下实验:
实验1:向该溶液中逐滴滴入过量的(NH4)2CO3溶液,产生白色沉淀B,并有无色气泡产生。
实验2:静置后,再向溶液中加入过量Ba(OH)2溶液,加热,仍然存在白色沉淀C,并有无色气泡产生。
实验3:静置后,继续向溶液中加入Cu片和过量的盐酸,仍然存在白色沉淀D,溶液变蓝色,并有气泡E产生。
(1)白色沉淀C的成分为________ (填化学式);气体E的成分为______ (写名称)。
(2)实验1中发生反应的离子方程式为______________ 。
(3)实验3中发生所有反应的离子方程式为__________ 。
(4)溶液A中__________ (填“一定”“可能”或“一定不”)存在NH4+,理由是_________ 。
实验1:向该溶液中逐滴滴入过量的(NH4)2CO3溶液,产生白色沉淀B,并有无色气泡产生。
实验2:静置后,再向溶液中加入过量Ba(OH)2溶液,加热,仍然存在白色沉淀C,并有无色气泡产生。
实验3:静置后,继续向溶液中加入Cu片和过量的盐酸,仍然存在白色沉淀D,溶液变蓝色,并有气泡E产生。
(1)白色沉淀C的成分为
(2)实验1中发生反应的离子方程式为
(3)实验3中发生所有反应的离子方程式为
(4)溶液A中
更新时间:2020-04-03 10:14:06
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】A、B、C、D四种可溶性盐,它们的阳离子可能是Ba2+、Ag+、Na+、Cu2+中的某一种,阴离子可能是 、
、 、Cl-、
、Cl-、 的某一种(每种离子只能使用一次);
的某一种(每种离子只能使用一次);
①若把四种盐分别溶解于盛有蒸馏水的四支试管中,只有C盐的溶液呈蓝色;
②若向四支试管中分别加足量盐酸,B溶液有沉淀产生,D溶液有无色无味气体逸出。
根据①②实验事实可推断它们的化学式为:
(1)A、___________ ;B、___________ ;C、____________ ;D、___________ ;
(2)写出②中D与盐酸反应的离子方程式:______________________________ 。
(3)某溶液中含有少量的CaCl2,某学生用过量的D使Ca2+离子转化为沉淀而除去,确认D已过量的实验操作是_______________________ 。
 、
、 、Cl-、
、Cl-、 的某一种(每种离子只能使用一次);
的某一种(每种离子只能使用一次);①若把四种盐分别溶解于盛有蒸馏水的四支试管中,只有C盐的溶液呈蓝色;
②若向四支试管中分别加足量盐酸,B溶液有沉淀产生,D溶液有无色无味气体逸出。
根据①②实验事实可推断它们的化学式为:
(1)A、
(2)写出②中D与盐酸反应的离子方程式:
(3)某溶液中含有少量的CaCl2,某学生用过量的D使Ca2+离子转化为沉淀而除去,确认D已过量的实验操作是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】某无色透明溶液中可能大量存在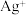 、
、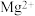 、
、 、
、 、
、 、
、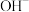 、
、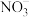 、
、 中的几种。请填写下列空白:
中的几种。请填写下列空白:
(1)不做任何实验就可以肯定原溶液中不存在的离子是___________ 。
(2)取少量原溶液,加入过量稀盐酸,有白色沉淀生成;再加入过量的稀硝酸,沉淀不消失。说明原溶液中肯定存在的离子是___________ ,有关的离子方程式为___________ 。
(3)取(2)中的滤液,加入过量的氢氧化钠溶液,出现白色沉淀,说明原溶液中肯定有___________ ,此过程中涉及到的离子方程式有___________ 。
(4)通过以上叙述可知溶液中肯定不存在的离子是可能存在的离子是___________ 。
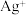 、
、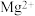 、
、 、
、 、
、 、
、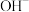 、
、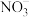 、
、 中的几种。请填写下列空白:
中的几种。请填写下列空白:(1)不做任何实验就可以肯定原溶液中不存在的离子是
(2)取少量原溶液,加入过量稀盐酸,有白色沉淀生成;再加入过量的稀硝酸,沉淀不消失。说明原溶液中肯定存在的离子是
(3)取(2)中的滤液,加入过量的氢氧化钠溶液,出现白色沉淀,说明原溶液中肯定有
(4)通过以上叙述可知溶液中肯定不存在的离子是可能存在的离子是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】有一包白色固体粉末,已知除了含有 KNO3 以外,其中可能还含有 KCl、Ba(NO3)2、CuSO4、K2CO3、Na2SO4 中的一种或几种,现通过以下实验来确定该样品的组成:
①将部分粉末加入水中,振荡,有白色沉淀生成,过滤,溶液呈无色;
②向①的沉淀物中加入足量稀硝酸,固体完全溶解,并有气泡产生;
③取少量②的溶液,滴入稀硫酸,有白色沉淀产生;
④另取①中过滤后的溶液加入足量 AgNO3 溶液,产生白色沉淀; 根据上述实验事实,回答下列问题:
(1)原白色粉末中除 KNO3 以外一定还含有的物质是_________ ,一定不含有的物质 是_____ ,可能存在的物质是_____ (填化学式);
(2)请写出第②步变化中所涉及的化学反应方程式:_____ ;
(3)A 同学为了确认该固体粉末中“可能存在的物质”是否存在, 他重新取了少量该样品于试管中加适量的蒸馏水溶解,请根据该同学设计的方案填空:

加入的试剂①_________ 试剂②_____ (填化学式);当加入试剂②时,实验现 象为_____ 就可以确认该物质一定存在。
(4)B 同学为了进一步确定该样品的成分,他称取了 10.0 g 该固体,按如下方案进行实验: 说明:实验中产生的气体已经换算成标准状况下的体积。
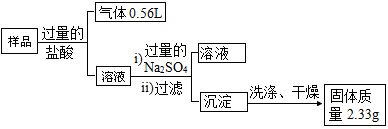
①请简述在实验室进行上述实验过程时如何洗涤沉淀_____ 。
②若按照 B 同学以上实验方案,还需对“溶液 2”中的溶质进一步分析,通过已有的实验数据分析,若该 样品中含 KNO3 的质量分数为_____ 时,可以确认样品中一定不含有“可能存在的物质”。
①将部分粉末加入水中,振荡,有白色沉淀生成,过滤,溶液呈无色;
②向①的沉淀物中加入足量稀硝酸,固体完全溶解,并有气泡产生;
③取少量②的溶液,滴入稀硫酸,有白色沉淀产生;
④另取①中过滤后的溶液加入足量 AgNO3 溶液,产生白色沉淀; 根据上述实验事实,回答下列问题:
(1)原白色粉末中除 KNO3 以外一定还含有的物质是
(2)请写出第②步变化中所涉及的化学反应方程式:
(3)A 同学为了确认该固体粉末中“可能存在的物质”是否存在, 他重新取了少量该样品于试管中加适量的蒸馏水溶解,请根据该同学设计的方案填空:

加入的试剂①
(4)B 同学为了进一步确定该样品的成分,他称取了 10.0 g 该固体,按如下方案进行实验: 说明:实验中产生的气体已经换算成标准状况下的体积。

①请简述在实验室进行上述实验过程时如何洗涤沉淀
②若按照 B 同学以上实验方案,还需对“溶液 2”中的溶质进一步分析,通过已有的实验数据分析,若该 样品中含 KNO3 的质量分数为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐1】以含钴废催化剂(主要成分为Co、Fe、SiO2)为原料制取复合氧化钴的流程如下:
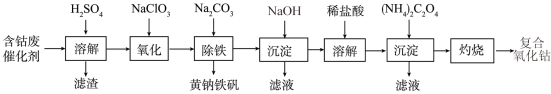
(1)用H2SO4溶解后过滤,得到的滤渣是____ (填化学式)。将滤渣洗涤2~3次,再将洗液与滤液合并的目的是_________________________________ 。
(2)在加热搅拌条件下加入NaClO3,将Fe2+氧化成Fe3+,反应的离子方程式是__________ 。
(3)已知:铁氰化钾的化学式为K3[Fe(CN)6];亚铁氰化钾的化学式为K4[Fe(CN)6]。
3Fe2++2[Fe(CN)6]3− =Fe3[Fe(CN)6]2↓(蓝色沉淀)
4Fe3++3[Fe(CN)6]4− = Fe4[Fe(CN)6]3↓(蓝色沉淀)
确定Fe2+是否氧化完全的方法是_________________________________ 。(仅供选择的试剂:铁氰化钾溶液、亚铁氰化钾溶液、铁粉、KSCN溶液)
(4)已知CoCl2的溶解度曲线如图所示。
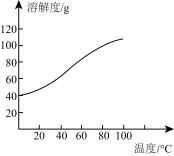
向碱式碳酸钴沉淀中加入足量稀盐酸边加热边搅拌至完全溶解后,需趁热过滤的原因是_________________ 。

(1)用H2SO4溶解后过滤,得到的滤渣是
(2)在加热搅拌条件下加入NaClO3,将Fe2+氧化成Fe3+,反应的离子方程式是
(3)已知:铁氰化钾的化学式为K3[Fe(CN)6];亚铁氰化钾的化学式为K4[Fe(CN)6]。
3Fe2++2[Fe(CN)6]3− =Fe3[Fe(CN)6]2↓(蓝色沉淀)
4Fe3++3[Fe(CN)6]4− = Fe4[Fe(CN)6]3↓(蓝色沉淀)
确定Fe2+是否氧化完全的方法是
(4)已知CoCl2的溶解度曲线如图所示。

向碱式碳酸钴沉淀中加入足量稀盐酸边加热边搅拌至完全溶解后,需趁热过滤的原因是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】有一包白色粉末,可能含有 Na2SO4、CaCO3、KCl、BaCl2、CuSO4 中的一种或几种,按以下步骤进行实验:
①将此粉末溶于水,得到无色溶液和白色沉淀;
②将足量稀盐酸加入白色沉淀中,沉淀部分溶解,并有气泡产生。
(1)根据上述实验现象,判断此粉末中一定含有的物质是______ 、________ _________ ,一定没有的物质是__________ ,可能含有的物质是____________ (均填写化学式)。
(2)上述实验中反应的离子方程式是__________________________________________ 。
①将此粉末溶于水,得到无色溶液和白色沉淀;
②将足量稀盐酸加入白色沉淀中,沉淀部分溶解,并有气泡产生。
(1)根据上述实验现象,判断此粉末中一定含有的物质是
(2)上述实验中反应的离子方程式是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】水污染是常见的环境问题,每一个人都应该自觉地保护水资源,防止污染物随意排放到水体中。化学实验中产生的重金属盐离子如Ag+、Ba2+、Cu2+、Pb2+等能使蛋白质丧失生理功能,使生物体中毒,需要集中处理后才能排放。某次化学实验后,回收的废液中可能存在Ag+、Ba2+、Cu2+。
(1)确定废液中存在Ag+的操作:______________________ 。
(2)若废液中存在Ag+、Ba2+、Cu2+,某同学欲对这三种离子逐一沉淀分离,加入试剂的顺序为_____ 。
A. HCl、H2SO4、NaOH B. H2SO4、NaOH、HCl
C. NaOH、H2SO4、HCl D. H2SO4、HCl、NaOH
(3)若废液中存在Ag+、Ba2+、Cu2+,某同学欲从废液中除去这些离子且对铜、银两种金属分别回收,设计如下处理方案:
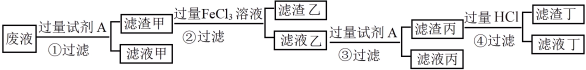
已知:a:氧化性Ag+>Fe3+>Cu2+>Fe2+,Cu+2Fe3+=Cu2++2Fe2+。
b:向滤液丙和丁中通入氯气,可重新获得FeCl3溶液,用于循环利用。
①滤液甲应该加入___________ 试剂处理后才能够倒掉。
②步骤①相关的离子反应方程式:___________ ,___________ 。
③滤渣乙的成分___________ 。
(1)确定废液中存在Ag+的操作:
(2)若废液中存在Ag+、Ba2+、Cu2+,某同学欲对这三种离子逐一沉淀分离,加入试剂的顺序为
A. HCl、H2SO4、NaOH B. H2SO4、NaOH、HCl
C. NaOH、H2SO4、HCl D. H2SO4、HCl、NaOH
(3)若废液中存在Ag+、Ba2+、Cu2+,某同学欲从废液中除去这些离子且对铜、银两种金属分别回收,设计如下处理方案:

已知:a:氧化性Ag+>Fe3+>Cu2+>Fe2+,Cu+2Fe3+=Cu2++2Fe2+。
b:向滤液丙和丁中通入氯气,可重新获得FeCl3溶液,用于循环利用。
①滤液甲应该加入
②步骤①相关的离子反应方程式:
③滤渣乙的成分
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】四溴化碳是一种灰白色粉末,熔点为94~95℃,广泛用于有机化合物的溴代、农药的制备等。某合作学习小组的同学拟用丙酮和液溴制备四溴化碳,其原理为CH3COCH3+4Br2+5NaOH→CBr4+CH3COONa+4NaBr+4H2O。回答下列问题:
Ⅰ.制取Br2
(1)甲组同学拟用溴化钠、二氧化锰及浓硫酸制备液溴,其实验装置如图1所示:

①该装置不用橡皮塞及橡皮管,其原因是___________________ ;
②冰水的作用是__________________________ 。
Ⅱ.制取CBr4
(2)乙组同学拟利用甲组同学制得的液溴与CH3COCH3(沸点56.5℃)等试剂制取四溴化碳。实验步骤如下:
步骤1:向图2中三颈烧瓶中加入11.4 g NaOH和46 mL水,搅拌。
步骤2:冰水浴冷却至2℃时,开始不断滴加液溴20 g,滴加完毕后在5℃下保持20 min。
步骤3:加入少量相转移试剂,在不断搅拌下滴入1.6 g丙酮,维持温度在5~10℃,连续搅拌4 h。
步骤4:过滤、冷水洗涤、减压烘干,得产品8.3 g。
①步骤2滴入Br2之前,冷却至2℃的目的是__________________________
②步骤4洗涤时,如何证明已洗涤干净:___________________________ 。
③本次实验中产品的产率为______________ 。
Ⅰ.制取Br2
(1)甲组同学拟用溴化钠、二氧化锰及浓硫酸制备液溴,其实验装置如图1所示:

①该装置不用橡皮塞及橡皮管,其原因是
②冰水的作用是
Ⅱ.制取CBr4
(2)乙组同学拟利用甲组同学制得的液溴与CH3COCH3(沸点56.5℃)等试剂制取四溴化碳。实验步骤如下:
步骤1:向图2中三颈烧瓶中加入11.4 g NaOH和46 mL水,搅拌。
步骤2:冰水浴冷却至2℃时,开始不断滴加液溴20 g,滴加完毕后在5℃下保持20 min。
步骤3:加入少量相转移试剂,在不断搅拌下滴入1.6 g丙酮,维持温度在5~10℃,连续搅拌4 h。
步骤4:过滤、冷水洗涤、减压烘干,得产品8.3 g。
①步骤2滴入Br2之前,冷却至2℃的目的是
②步骤4洗涤时,如何证明已洗涤干净:
③本次实验中产品的产率为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】有一瓶无色透明溶液,其中可能含有Na+、Mg2+、Ba2+、Al3+、Fe3+、SO42-、CO32-、I-。取该溶液进行以下实验:
①用pH试纸测得该溶液显酸性;
②取部分溶液,加入数滴新制氯水及少量CCl4,经振荡、静置后,CCl4层呈紫红色;
③另取部分溶液,逐滴加入稀NaOH溶液,使溶液从酸性逐渐变至碱性,在整个滴加过程中无沉淀生成;
④取部分③得到的碱性溶液,加入Na2CO3溶液,有白色沉淀生成;
(1)该溶液为无色透明溶液,可确定其中一定不含___________ ;(填离子符号,下同)
(2)由步骤①中测量溶液pH的方法_____________________________________________ ,通过测量结果可知,溶液中一定不存在____________ ;
(3)由步骤②可知,溶液中含有____________ ;
(4)由步骤③可排除_____________ 、____________ 的存在;
(5)由步骤④可知,溶液中含有_________ ,由此可排除_________ 的存在;
(6)通过实验不能确定___________ 是否存在。
①用pH试纸测得该溶液显酸性;
②取部分溶液,加入数滴新制氯水及少量CCl4,经振荡、静置后,CCl4层呈紫红色;
③另取部分溶液,逐滴加入稀NaOH溶液,使溶液从酸性逐渐变至碱性,在整个滴加过程中无沉淀生成;
④取部分③得到的碱性溶液,加入Na2CO3溶液,有白色沉淀生成;
(1)该溶液为无色透明溶液,可确定其中一定不含
(2)由步骤①中测量溶液pH的方法
(3)由步骤②可知,溶液中含有
(4)由步骤③可排除
(5)由步骤④可知,溶液中含有
(6)通过实验不能确定
您最近一年使用:0次
【推荐3】某化学小组同学探究在实验室中 检验的干扰因素。
检验的干扰因素。
(1)检验溶液中是否含有 时先用过量盐酸将溶液酸化,其目的是排除
时先用过量盐酸将溶液酸化,其目的是排除_______________ 、 、Ag+等离子可能造成的干扰。
、Ag+等离子可能造成的干扰。
(2)为了验证盐酸能否排除 的干扰,该小组同学进行了如下实验:
的干扰,该小组同学进行了如下实验:
Ⅰ.量取一定体积的浓盐酸(盛放浓盐酸试剂瓶的标签中部分信息如下图),稀释,配制成 5 mol/L 的稀盐酸。

Ⅱ.甲同学取 0.3 g 未变质的 Na2SO3 固体,向其中加入上述 5mol/L 稀盐酸至过量,产生大量气泡。充分振荡后滴加 4 滴BaCl2溶液,迅速产生白色浑浊,产生白色浑浊的原因可能是:
①______________ 。
②盐酸中含有 Fe3+,实验证实含有 Fe3+的方案是:___________________ ,用离子方程式解释由 Fe3+产生白色浑浊的原因:__________ 。
(3)乙同学提出,检验 时能否用硝酸酸化来排除
时能否用硝酸酸化来排除 的干扰,丙同学认为不可行,理由是(用离子方程式表示)
的干扰,丙同学认为不可行,理由是(用离子方程式表示)____________________________ ,继续实验:称取 5 份 0.3 g 未变质的Na2SO3固体,分别向其中加入 10 mL 不同浓度的硝酸, 振荡;再滴加 4 滴BaCl2 溶液,观察并记录实验现象如下表。
依据上述实验得出的结论是:________________ 。
(4)丙同学查阅资料后提出:Cl-的存在也会对 的检验产生干扰。在 Cl-催化作用下,稀硝酸可将
的检验产生干扰。在 Cl-催化作用下,稀硝酸可将 氧化为
氧化为  。为证明上述观点,设计如下实验,请将实验ⅱ的操作补充完整。
。为证明上述观点,设计如下实验,请将实验ⅱ的操作补充完整。
 检验的干扰因素。
检验的干扰因素。(1)检验溶液中是否含有
 时先用过量盐酸将溶液酸化,其目的是排除
时先用过量盐酸将溶液酸化,其目的是排除 、Ag+等离子可能造成的干扰。
、Ag+等离子可能造成的干扰。(2)为了验证盐酸能否排除
 的干扰,该小组同学进行了如下实验:
的干扰,该小组同学进行了如下实验:Ⅰ.量取一定体积的浓盐酸(盛放浓盐酸试剂瓶的标签中部分信息如下图),稀释,配制成 5 mol/L 的稀盐酸。

Ⅱ.甲同学取 0.3 g 未变质的 Na2SO3 固体,向其中加入上述 5mol/L 稀盐酸至过量,产生大量气泡。充分振荡后滴加 4 滴BaCl2溶液,迅速产生白色浑浊,产生白色浑浊的原因可能是:
①
②盐酸中含有 Fe3+,实验证实含有 Fe3+的方案是:
(3)乙同学提出,检验
 时能否用硝酸酸化来排除
时能否用硝酸酸化来排除 的干扰,丙同学认为不可行,理由是(用离子方程式表示)
的干扰,丙同学认为不可行,理由是(用离子方程式表示)| 硝酸浓度(mol/L) | 滴加氯化钡溶液之前现象 | 滴加氯化钡溶液之后现象 |
| 15.0(浓硝酸) | 产生大量红棕色气体,溶液呈黄色 | 立即产生大量白色沉淀 |
| 7.5 | 产生大量红棕色气体,溶液呈淡黄色 | 立即产生大量白色沉淀 |
| 4.8 | 产生少量无色、刺激性气味气体,溶液无色 | 开始无现象,约 60 min 后溶液开始变浑浊 |
| 2.0 | 产生少量无色、刺激性气味气体,溶液无色 | 开始无现象,约 70 min 后溶液开始变浑浊 |
| 0.5 | 产生少量无色、刺激性气味气体,溶液无色 | 开始无现象,约 120 min 后溶液开始变浑浊 |
(4)丙同学查阅资料后提出:Cl-的存在也会对
 的检验产生干扰。在 Cl-催化作用下,稀硝酸可将
的检验产生干扰。在 Cl-催化作用下,稀硝酸可将 氧化为
氧化为  。为证明上述观点,设计如下实验,请将实验ⅱ的操作补充完整。
。为证明上述观点,设计如下实验,请将实验ⅱ的操作补充完整。| 实验 | 实验操作 | 实验现象 |
| ⅰ | 将 0.3 g Na2SO3和 0.3 g NaCl 固体混合,加入 10 mL 2.0mol/L 的稀硝酸,振荡后,再滴加 4 滴 BaCl2溶液。 | 立即产生大量白色沉淀。 |
| ⅱ | 放置两小时后溶液未变浑浊。 |
您最近一年使用:0次



