某小组在Fe2+检验实验中观察到异常现象,为探究“红色褪去”的原因,进行如下实验:
分析上述三个实验,下列叙述不正确的是
| 编号 | 实验I | 实验II | 实验III |
| 实验步骤 | 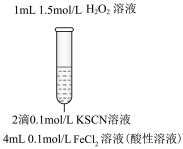 | 将实验I褪色后的溶液分三份分别进行实验 | 进一步探究“红色褪去”的原因,又进行以下实验 ①  ②取反应后的溶液,滴加盐酸和BaCl2溶液 |
| 现象 | 溶液先变红,片刻后红色褪去,有气体生成(经检验为O2) | ①无明显现象 ②溶液变红 ③产生白色沉淀 | ①溶液变红,一段时间后不褪色。 ②无白色沉淀产生 |
分析上述三个实验,下列叙述不正确的是
| A.在此实验条件下H2O2氧化Fe2+的速率比氧化SCN-的速率快 |
| B.通过实验Ⅱ推出实验Ⅰ中红色褪去的原因是由于SCN-被氧化 |
| C.通过实验Ⅰ和实验Ⅲ对比推出红色褪去只与H2O2的氧化性有关 |
| D.综上所述,实验Ⅰ中红色褪去的原因与化学平衡移动原理无关 |
更新时间:2020-04-02 08:59:05
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】有 、
、 、
、 、
、 、
、 五种溶液,用一种试剂就可把它们鉴别开来,这种试剂是
五种溶液,用一种试剂就可把它们鉴别开来,这种试剂是
 、
、 、
、 、
、 、
、 五种溶液,用一种试剂就可把它们鉴别开来,这种试剂是
五种溶液,用一种试剂就可把它们鉴别开来,这种试剂是A. 溶液 溶液 | B.烧碱溶液 | C.氨水 | D. 溶液 溶液 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】以硫铁矿烧渣(主要成分为 、
、 、
、 和
和 )为原料生产聚合硫酸铁
)为原料生产聚合硫酸铁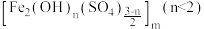 的流程如下:
的流程如下:
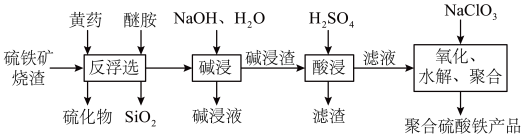
下列说法正确的是
 、
、 、
、 和
和 )为原料生产聚合硫酸铁
)为原料生产聚合硫酸铁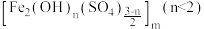 的流程如下:
的流程如下:
下列说法正确的是
| A.“碱浸”的目的是除去铝元素 |
B.检验“酸浸”后滤液中是否含有 ,选用试剂为KSCN溶液和氯水 ,选用试剂为KSCN溶液和氯水 |
C.可用 代替“氧化、水解、聚合”中的 代替“氧化、水解、聚合”中的 |
| D.为加快反应速率,“氧化、水解、聚合”应在较高温度下进行 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】室温下进行下列实验,实验操作、现象及结论都正确的是
| 选项 | 实验操作和现象 | 结论 |
| A | 向浓硝酸中插入红热的木炭,产生红棕色气体 | NO2一定是由木炭和浓硝酸反应生成 |
| B | 将NaOH浓溶液滴入某溶液中加热放出的气体能使湿润的蓝色石蕊试纸变红 | 某溶液中有 |
| C | 把SO2和气体X一起通入到BaCl2溶液中,有白色沉淀产生 | X气体可能具有强氧化性 |
| D | 将 样品溶于稀硫酸后,滴加KSCN溶液,溶液变红 样品溶于稀硫酸后,滴加KSCN溶液,溶液变红 |  样品已变质 样品已变质 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】某未知溶液可能含Cl-、 、Na+、
、Na+、 、H+,将溶液滴在蓝色石蕊试纸上,试纸变红。取少量试液,滴加硝酸酸化的氯化钡溶液,有白色沉淀生成,静置后向上层清液中滴加硝酸银溶液,产生白色沉淀。下列判断合理的是
、H+,将溶液滴在蓝色石蕊试纸上,试纸变红。取少量试液,滴加硝酸酸化的氯化钡溶液,有白色沉淀生成,静置后向上层清液中滴加硝酸银溶液,产生白色沉淀。下列判断合理的是
 、Na+、
、Na+、 、H+,将溶液滴在蓝色石蕊试纸上,试纸变红。取少量试液,滴加硝酸酸化的氯化钡溶液,有白色沉淀生成,静置后向上层清液中滴加硝酸银溶液,产生白色沉淀。下列判断合理的是
、H+,将溶液滴在蓝色石蕊试纸上,试纸变红。取少量试液,滴加硝酸酸化的氯化钡溶液,有白色沉淀生成,静置后向上层清液中滴加硝酸银溶液,产生白色沉淀。下列判断合理的是| A.一定有Cl- | B.不一定有 |
C.一定没有 | D.一定没有Na+ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列依据相关实验得出的结论正确的是( )
| A.向某溶液中加入稀盐酸,产生的气体通入澄清石灰水,石灰水变浑浊,该溶液一定是碳酸盐溶液 |
B.已知I3- I2+I-,向盛有KI3溶液的试管中加入适量CCl4,振荡静置后CCl4层显紫色,说明KI3在CCl4中的溶解度比在水中的大 I2+I-,向盛有KI3溶液的试管中加入适量CCl4,振荡静置后CCl4层显紫色,说明KI3在CCl4中的溶解度比在水中的大 |
| C.将某气体通入溴水中,溴水颜色褪去,该气体一定是乙烯 |
| D.向含有少量FeCl3的MgCl2溶液中加入足量Mg(OH)2粉末,搅拌一段时间后过滤,可除去氯化镁溶液中少量氯化铁 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】实验室探究 与
与 溶液反应的原理,装置如图,实验中Y装置中产生白色沉淀.下列说法错误的是
溶液反应的原理,装置如图,实验中Y装置中产生白色沉淀.下列说法错误的是

 与
与 溶液反应的原理,装置如图,实验中Y装置中产生白色沉淀.下列说法错误的是
溶液反应的原理,装置如图,实验中Y装置中产生白色沉淀.下列说法错误的是
A.实验前先打开弹簧夹,通入一段时间 |
B.Y中产生的白色沉淀是 |
| C.浓硫酸可以改为浓硝酸 |
D.将 换成氨水,Y中也产生白色沉淀 换成氨水,Y中也产生白色沉淀 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】根据下列实验操作和现象得出的结论正确的是
| 选项 | 实验 | 现象 | 结论 |
| A | 甲烷与氯气在光照下反应,将反应后的气体通入紫色石蕊试液中 | 紫色石蕊试液变红 | 反应后的气体是HCl |
| B | 向正己烷中加入催化剂,高温使其热裂解,将产生的气体通入溴水中 | 溴水褪色 | 裂解产生的气体是乙烯 |
| C | 向FeCl3溶液中滴入几滴30%的H2O2溶液 | 有气体产生,一段时间后,FeCl3溶液颜色加深 | Fe3+能催化H2O2分解,该分解反应为放热反应 |
| D | 向某溶液中滴加氢氧化钠稀溶液后,将红色石蕊试纸置于试管口 | 试纸不变蓝 | 该溶液无 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次

 ,下列方案中正确的是
,下列方案中正确的是

