浙教版科学 九年级上册 物质及其变化 (1.4--1.6)
浙江
九年级
单元测试
2019-09-12
303次
整体难度:
适中
考查范围:
常见的物质、物质的结构、物质的运动与相互作用、增进对科学探究的理解和提高探究的能力
一、选择题 添加题型下试题
| A.无色酚酞试液 | B.FeCl3 溶液 | C.BaCl2 溶液 | D.pH试纸 |
【知识点】 中和反应及其应用 酸碱指示剂及其性质 溶液的酸碱性与pH值的关系
A. 在部分变质的NaOH溶液中滴加稀盐酸 在部分变质的NaOH溶液中滴加稀盐酸 |
B. O2的溶解度受温度影响的变化曲线 O2的溶解度受温度影响的变化曲线 |
C. 等质量的Mg粉和Fe粉与足量同浓度的稀盐酸反应 等质量的Mg粉和Fe粉与足量同浓度的稀盐酸反应 |
D. 浓盐酸稀释过程中pH的变化曲线 浓盐酸稀释过程中pH的变化曲线 |
| A.常见的酸溶液:H2O、HCl、H2SO4 | B.常见的黑色固体:CuO、MnO2、Fe3O4 |
| C.常见的有还原性的物质:C、CO、O2 | D.常见的氧化物:MgO KMnO4 H2O |
【知识点】 物质分类的方法 常见物质的分类 氧化物、酸、碱和盐的概念
①用氢氧化钠溶液洗涤石油产品中的残余硫酸②用碳酸氢钠治疗胃酸过多
③用熟石灰改良酸性土壤 ④用稀氨水涂抹在蚊子叮咬处(分泌出蚁酸)止痒。
| A.①② | B.②③④ | C.②③ | D.①③④ |
【知识点】 中和反应及其应用
A.一定是稀硫酸 | B.一定是硝酸银溶液 | C.一定是可溶性硫酸盐溶液 | D.难以确定 |
【知识点】 常见离子的检验方法及现象
序号 | 甲 | 乙 |
A | Fe粉、Cu粉 | 稀盐酸 |
B | CuCl2、HCl溶液 | KOH溶液 |
C | CaCl2、HCl溶液 | Na2CO3固体 |
D | Ba(OH)2溶液、BaCO3固体 | H2SO4 |
| A.A | B.B | C.C | D.D |
| A.浓硫酸、生石灰可用作干燥剂,均是利用了它们的化学性质 |
| B.氢氧化钠、碳酸钠的水溶液都呈碱性,是因为它们在水中都能电离出OH- |
| C.盐酸、硫酸具有相似的化学性质,是由于它们都具有氢元素 |
| D.熟石灰、硫酸铜可用于配制波尔多液,这利用了碱能和某些盐发生反应的化学性质 |
| A.水烧开后易把壶盖冲起﹣﹣说明温度升高分子会变大 |
| B.冬天用煤炉取暖,为防热量散失关紧门窗,O2不足煤不完全燃烧易起CO中毒 |
| C.酸碱中和反应都能生成水﹣﹣实质是H+与OH﹣结合生成了H2O |
| D.铝制品有抗腐蚀性能﹣﹣实质是表面生成了致密氧化膜起保护作用 |
A.Na+ 、H+ 、SO42-  | B.Ca2+、 OH- 、Na+ |
C.H+ 、 SO42- 、 Cl- | D.K+ 、 CO32- 、 NO3- |
【知识点】 氧化物、酸、碱和盐的概念
A.K2CO3、HCl、CaCl2、KNO3 | B.(NH4)2SO4、NaNO3、NaOH、KCl |
| C.NaCl、Na2SO4、H2SO4、Ba(NO3)2 | D.CuSO4、NaOH、NaNO3、NaCl |
选项 | 实验目的 | 所用试剂或方法 |
A | 实验室制取CO2 | 块状大理石与稀硫酸 |
B | 鉴别硬水和软水 | 观察液体是否浑浊 |
C | 鉴别H2O、KCl溶液 | AgNO3溶液 |
D | 除去CO2中少量的CO | 通入O2 ,点燃 |
A.A  | B.B  | C.C  | D.D |
二、填空题 添加题型下试题
①硝酸钾②小苏打③熟石灰④聚乙烯⑤生石灰⑥氯化钙⑦碳酸钙.
试按下列要求用序号填空:
(1)常用作干燥剂得到是
(2)常用作发酵粉主要成分的是
(3)可以制作食品包装袋的是
(4)常用作改良酸性土壤的碱是
【知识点】 盐的性质及用途 酸碱性对生命活动和农作物生长的影响
三、探究题 添加题型下试题
小明同学联想到再做“固体碘溶解在酒精中”的实验时,酒精作为溶剂,能溶解固体碘.酒精能否溶解氢氧化钠和碳酸钠呢?小明查阅资料并通过实验获知:氢氧化钠不与酒精发生化学反应,但能溶解在酒精中形成无色、透明的溶液。氢氧化钠的酒精溶液与氢氧化钠的水溶液化学性质相似。碳酸钠不与酒精反应也不溶于酒精。
至此,小明同学对自己提出的问题有了清晰的解决方案。
(1)小明同学的解决方案是
(3)写出解决方案中涉及到的化学方程式:
【知识点】 制定探究方案 二氧化碳的化学性质 碱的化学性质 书写化学方程式、文字表达式
四、填空题 添加题型下试题
①取一定量的白色粉末加入足量的水,振荡,静置,得白色沉淀,上层清液为无色.
②过滤,在白色沉淀中加入足量稀盐酸,白色沉淀全部溶解,且有气泡产生.
据此推断,该白色粉末中一定含有
【知识点】 中和反应及其应用 酸碱指示剂及其性质 溶液的酸碱性与pH值的关系
(1)取少量白色粉末,向其中加入足量的水,充分搅拌后过滤,得到白色沉淀和无色滤液,由此可推断混合物中一定没有
(2)取实验(1)滤出的白色沉淀,向其中加入足量的盐酸,沉淀全部溶解,并产生无色气体。根据上述实验可推断:原白色粉末中一定有
【知识点】 盐的性质及用途 酸、碱、盐的鉴别 常见离子的检验方法及现象
(1)氯化铵(NH4Cl)各组成元素中对植物生长最有效的元素是
(2)小宇同学在氯化铵中加了熟石灰,结果闻到了一股刺激性气味,说:“怎么像厕所里的气味?”这是因为
【知识点】 碱的化学性质 盐与化肥 常见离子的检验方法及现象
五、探究题 添加题型下试题

【提出问题】这瓶溶液是什么溶液?
【获得信息】酸、碱、盐的性质实验中用到含有钠元素的物质是氯化钠、氢氧化钠、碳酸钠.
【提出猜想】猜想一:氯化钠溶液; 猜想二:氢氧化钠溶液; 猜想三:碳酸钠溶液.
(1)【实验推断】 ①小丽取样滴加无色酚酞试液,溶液呈红色.
②小刚另取样品滴加稀盐酸有
③小青认为小刚的结论不完全正确,理由是
(2)小组同学讨论后一致认为还需要进行如下实验:
【继续探究】另取样品加入过量的CaCl2溶液,观察到有白色沉淀产生;静置后,取上层清液,滴入酚酞试液,溶液呈红色,其中加入过量的CaCl2溶液的目的是
 【提出问题】这瓶溶液是什么溶液?
【提出问题】这瓶溶液是什么溶液?【获得信息】酸、碱、盐的性质实验中用到含有钠元素的物质是氯化钠、氢氧化钠、碳酸钠。
【提出猜想】这瓶溶液是:猜想一:氯化钠溶液;猜想二:氢氧化钠溶液;猜想三:碳酸钠溶液。
(1)【实验推断】
①小丽取样滴加无色酚酞试液,溶液呈红色,得出结论:该溶液不可能是氯化钠溶液;
②小刚另取样滴加稀盐酸有气泡产生,小刚得出结论:该溶液是碳酸钠溶液;
③小青认为小刚的结论不完全正确,理由是
(2)【继续探究】另取样加入过量的
(3)【实验结论】这瓶溶液标签上显示的是
(1)其他条件相同,同种金属与不同质量分数的盐酸反应,反应的快慢不同。取质量相等的铝片,分别放入5%、20%的足量稀盐酸中。实验表明盐酸浓度越大,反应进行越快。如图Ⅰ、Ⅱ、Ⅲ是三位同学记录实验生成氢气的质量(m)与反应时间(t)的关系曲线,其中正确的是

(2)其他条件相同,不同金属与相同质量分数的盐酸反应,反应的快慢不同。取质量相等的镁片、锌片、铁片中的两种金属,分别放入溶质质量分数相同的足量稀盐酸中,生成氢气的质量(m)与反应时间(t)的关系曲线如图甲所示。则曲线A对应的金属与稀盐酸反应后生成的盐的名称是
(3)其他条件相同,颗粒大小不同的同种金属与相同质量分数的盐酸反应,反应的快慢不同。取质量相等的锌粉和锌片,分别放入溶质质量分数相同的足量稀盐酸中,锌粉与盐酸反应生成氢气的质量(m)与反应时间(t)的关系曲线如图乙所示,请在答题卡的该图上用实线“───”补画出锌片与盐酸反应生成氢气的质量(m)与反应时间(t)的关系曲线

(4)请你再提出一个影响金属与盐酸反应快慢的合理因素
【知识点】 金属的化学性质
六、解答题 添加题型下试题

(1)写出PM段发生的化学方程式
(2)P点溶液中的溶质是
(3)试通过计算确定m1的值
(4)M点溶液的溶质质量分数是多少?
【知识点】 酸的化学性质 盐的性质及用途 根据化学反应方程式的计算
七、填空题 添加题型下试题



(1)图1所示实验中发生的化学反应方程式是:
(2)图1所示反应恰好完成时的现象是
小明认为图2、3中的
(3)根据图1反应历程图4、5中能正确反应盐酸和氢氧化钠溶液发生反应过程中溶液的pH的变化曲线是:
(4)用溶质的质量分数为36.5%的盐酸40g与足量氢氧化钠溶液恰好完全反应,需要溶质的质量分数为20%的氢氧化钠溶液
八、解答题 添加题型下试题

(1)传统水泥和绿色水泥的生产过程分别涉及以下反应:
CaCO3
 CaO+ CO2↑ Mg3Si2O5(OH)4
CaO+ CO2↑ Mg3Si2O5(OH)4 3MgO + 2SiO2 + 2H2O↑
3MgO + 2SiO2 + 2H2O↑以上两个反应都属于
(2)与传统水泥相比,每生产和使用1吨绿色水泥能够减少排放
(3)传统水泥生产中,高温煅烧某种石灰石50吨,可产生二氧化碳多少吨?
九、填空题 添加题型下试题

(1)在实验过程中,可以先后看到的明显实验现象是
(2)最终所得溶液的pH
(3)求原溶液中BaCl2的质量分数为多少?
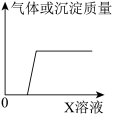
(4)当滴入Na2CO3溶液至图中B点时,通过计算求所得不饱和溶液中溶质质量分数为多少?(计算结果精确到0.1%)

(1)废液恰好处理完毕时,溶液的pH为
(2)图中m=
(3)废液恰好处理完毕时,回收所得溶液的溶质质量分数是多少(提示:硫酸恰好全部转化为硫酸钠,即H2SO4~Na2SO4)
【知识点】 酸的化学性质 碱的化学性质 盐的性质及用途 根据化学反应方程式的计算
十、探究题 添加题型下试题
(1)取2.5g水垢按图甲中A装置高温加热充分反应(已知CaCO3
 CaO+CO2↑),产生的气体依次通过B、C装置,实验后发现C装置中氢氧化钠溶液增加了0.88g。
CaO+CO2↑),产生的气体依次通过B、C装置,实验后发现C装置中氢氧化钠溶液增加了0.88g。
①写出C装置中发生化学反应方程式
②B装置中的浓硫酸是用来吸收反应中产生的水蒸气,这是利用了浓硫酸的
③该水垢所含碳酸钙的质量分数为
(2)按图乙所示的方法来实验,结果发现澄清石灰水没有变浑浊,原因是
【知识点】 盐的性质及用途 浓硫酸的性质及浓硫酸的稀释 根据化学反应方程式的计算
试卷分析
试卷题型(共 30题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、选择题 | |||
| 1 | 0.4 | 二氧化碳的化学性质 盐的性质及用途 物质除杂或净化 | |
| 2 | 0.94 | 碱的物理性质及用途 碱的化学性质 物质除杂或净化 | |
| 3 | 0.65 | 中和反应及其应用 酸碱指示剂及其性质 溶液的酸碱性与pH值的关系 | |
| 4 | 0.65 | 氧气的物理性质 金属活动性顺序及其应用 碱的化学性质 溶液的酸碱性与pH值的关系 | |
| 5 | 0.65 | 物质分类的方法 常见物质的分类 氧化物、酸、碱和盐的概念 | |
| 6 | 0.65 | 中和反应及其应用 | |
| 7 | 0.65 | 常见离子的检验方法及现象 | |
| 8 | 0.65 | 金属的化学性质 酸的化学性质 盐的性质及用途 | |
| 9 | 0.65 | 酸的化学性质 碱的化学性质 盐的性质及用途 | |
| 10 | 0.85 | 金属资源的保护 中和反应及其应用 分子的热运动 | |
| 11 | 0.65 | 酸、碱、盐的鉴别 酸碱指示剂及其性质 复分解反应及其应用 | |
| 12 | 0.85 | 氧化物、酸、碱和盐的概念 | |
| 13 | 0.4 | 盐的性质及用途 酸、碱、盐的鉴别 | |
| 14 | 0.85 | 酸的化学性质 酸、碱、盐的鉴别 | |
| 15 | 0.65 | 水的净化 盐的性质及用途 物质除杂或净化 | |
| 二、填空题 | |||
| 16 | 0.65 | 盐的性质及用途 酸碱性对生命活动和农作物生长的影响 | |
| 18 | 0.4 | 盐的性质及用途 酸、碱、盐的鉴别 物质的推断 | |
| 19 | 0.85 | 中和反应及其应用 酸碱指示剂及其性质 溶液的酸碱性与pH值的关系 | |
| 20 | 0.4 | 盐的性质及用途 酸、碱、盐的鉴别 常见离子的检验方法及现象 | |
| 21 | 0.85 | 碱的化学性质 盐与化肥 常见离子的检验方法及现象 | |
| 26 | 0.4 | 溶质质量分数的简单计算 中和反应及其应用 酸碱指示剂及其性质 溶液的酸碱性与pH值的关系 | |
| 28 | 0.4 | 溶质质量分数的简单计算 溶液的酸碱性与pH值的关系 根据化学反应方程式的计算 | |
| 29 | 0.4 | 酸的化学性质 碱的化学性质 盐的性质及用途 根据化学反应方程式的计算 | |
| 三、探究题 | |||
| 17 | 0.4 | 制定探究方案 二氧化碳的化学性质 碱的化学性质 书写化学方程式、文字表达式 | |
| 22 | 0.4 | 酸的化学性质 碱的化学性质 盐的性质及用途 酸碱指示剂及其性质 | |
| 23 | 0.4 | 酸的化学性质 碱的化学性质 盐的性质及用途 酸碱指示剂及其性质 | |
| 24 | 0.65 | 金属的化学性质 | |
| 30 | 0.65 | 盐的性质及用途 浓硫酸的性质及浓硫酸的稀释 根据化学反应方程式的计算 | |
| 四、解答题 | |||
| 25 | 0.65 | 酸的化学性质 盐的性质及用途 根据化学反应方程式的计算 | |
| 27 | 0.65 | 质量守恒定律及其应用 书写化学方程式、文字表达式 根据化学反应方程式的计算 分解反应及其应用 | |








