浙江省杭州市余杭区星桥中学2019-2020学年九年级第一次月考科学试题
浙江
九年级
阶段练习
2019-10-24
218次
整体难度:
适中
考查范围:
常见的物质、物质的运动与相互作用、物质的结构
一、选择题 添加题型下试题
| A.生产红糖时蒸发甘蔗汁液 | B.配制红曲酒时发酵糯米 |
| C.制作火腿时将成品切块包装 | D.制作蜜枣时晒干水 |
【知识点】 化学变化和物理变化的判别
| A.浓硫酸 |
| B.浓盐酸 |
| C.浓硝酸 |
| D.石灰乳 |
【知识点】 酸的物理性质及用途 碱的化学性质 浓硫酸的性质及浓硫酸的稀释
| A.AgNO3溶液 | B.NaOH溶液 | C.稀醋酸 | D.KNO3溶液 |
【知识点】 酸的化学性质
| A.加入硝酸银溶液后再加入稀硝酸 |
| B.滴加氯化钡溶液后再加入稀硝酸 |
| C.加入紫色石蕊试液后再加入硝酸银溶液和稀硝酸 |
| D.加入紫色石蕊试液后再加入碳酸钠溶液 |
【知识点】 酸的化学性质 常见离子的检验方法及现象 常见物质的鉴定 酸碱指示剂及其性质
| A.都能用作建筑材料 |
| B.都能用作某些气体的干燥剂 |
| C.它们的溶液都能用于检验二氧化碳气体 |
| D.农业上常用熟石灰来改良酸性土壤 |
| A.实验室需要用到的玻璃仪器有量筒、玻璃棒和胶头滴管 |
| B.配制该稀硫酸需要加水400mL |
| C.配制时应将浓硫酸小心的加入水中 |
| D.该稀硫酸中溶液质量:溶剂质量=5:4 |
【知识点】 溶液的组成 一定溶质质量分数的溶液的配制
| 试管内物质 | 胶头滴管内物质 | |
| A | 氢氧化钠固体 | 水 |
| B | 氧化铁 | 稀盐酸 |
| C | 氯化钡溶液 | 稀硫酸 |
| D | 二氧化碳 | 氢氧化钠溶液 |
| A.A | B.B | C.C | D.D |
【知识点】 溶解时的吸热或放热现象 酸的化学性质 碱的化学性质
| A.取样,在溶液中加过量的稀盐酸,如果有气泡产生,则可证明该溶液已完全变质 |
| B.取样,在溶液中滴加酚酞,如酚酞呈无色,则溶液已完全变质 |
| C.取样,在溶液中加入过量滴有酚酞的氯化钡溶液,如产生白色沉淀,且上层清液呈红色,则溶液未完全变质 |
| D.取样,在溶液中加入过量稀盐酸,则可除去氢氧化钠溶液中产生的杂质 |
| 选项 | 物质 | 所含杂质 | 所选试剂即用量 |
| A | 碳酸钠 | 氯化钾 | 适量的水 |
| B | 盐酸 | 硫酸 | 适量的氯化钡 |
| C | 氯化钙 | 稀盐酸 | 过量碳酸钙 |
| D | 氯化钾 | 稀盐酸 | 适量碳酸钾溶液 |
| A.A | B.B | C.C | D.D |
【知识点】 盐的性质及用途
| A. La(OH)3和HCl |
| B.La2O3和HCl |
| C.La和HCl |
| D.FeCl3和La(OH)3 |

由此得出的结论正确的是( )
| A.一定含有CaCO3和Ca(OH)2 |
| B.一定含有Ca(OH)2,可能含有CaCO3 |
| C.一定没有CaCO3和Ca(OH)2 |
| D.一定含有CaCO3,可能含有Ca(OH)2 |
| A.大于7 |
| B.小于7 |
| C.等于7 |
| D.等于0 |

| A.盐酸 |
| B.碳酸钠 |
| C.硫酸 |
| D.氯化钠 |
A. |
B. |
C. |
D. |
【知识点】 溶质质量分数的简单计算 二氧化碳的实验室制法
| A.Cu2+和SO42− |
| B.Cu2+和Cl− |
| C.Na+和SO42− |
| D.Ag+和NO3− |
【知识点】 离子或物质的共存问题 常见离子的检验方法及现象 常见物质的鉴定

| A.OE发生化学反应:Na2CO3+2HCl=2NaCl+CO2↑+H2O |
| B.PF有沉淀生成 |
| C.G点溶液的pH>7 |
| D.反应有先后顺序,Na2CO3先和CaCl2反应 |
二、填空题 添加题型下试题
(1)用小木棍蘸取浓硫酸少许,一段时间后,小木棍上出现的实验现象是
(2)在蔗糖(C12H22O11)分子中,氢、氧原子个数比是
(1)浓硫酸在实验室常用作干燥剂,因为浓硫酸有
(2)写出稀硫酸与下列物质反应的化学方程式:
①与铁粉反应:
②与碳酸钠溶液反应:
③与氯化钡溶液反应:
上述反应中,属于酸的共同性质的是
(3)盐酸的下列用途中,不能用硫酸代替盐酸的是
①金属表面除锈 ②制造药物氯化锌 ③除去NaCl中的少量NaOH
【知识点】 酸的化学性质 浓硫酸的性质及浓硫酸的稀释

(1)已知X是金属单质,则X可以是
(2)Y这种物质需要带何种离子才符合要求
(3)请写出稀硫酸与Y反应的一个化学方程式
【知识点】 酸的化学性质
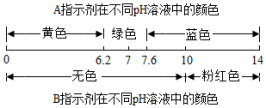
(1)在A处溶液中加入石蕊试液,溶液呈
(2)AB两点间的溶液的溶质是
(3)B到C的过程中溶液的pH逐渐
(4)在C点溶液中加入碳酸钙,现象为
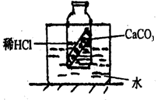
【知识点】 二氧化碳的实验室制法 影响液体压强大小的因素 物体的浮沉条件及其应用

(1)若混合后溶液质量减小,可能的组合是:
(2)混合后两物质发生反应,但溶液质量不变的组合是:
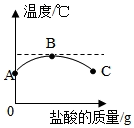
(3)混合后溶液质量不变,但滴入稀硫酸后产生气体的质量与加入稀硫酸的质量如图所示,则组合为:
(1)氯化铵(NH4Cl)各组成元素中对植物生长最有效的元素是
(2)小宇同学在氯化铵中加了熟石灰,结果闻到了一股刺激性气味,说:“怎么像厕所里的气味?”这是因为
【知识点】 碱的化学性质 盐与化肥 常见离子的检验方法及现象
三、探究题 添加题型下试题

(1)A实验最终能观察到的现象是
(2)B实验能体现出稀硫酸具有的化学性质是
(3)C实验中发生反应的化学方程式为
(4)将上述实验后所得溶液在烧杯中混合,观察到烧杯底部有沉淀,上层为有色溶液,此时,利用烧杯中的沉淀,再选择适当的试剂,即可证明C实验中所加BaCl2溶液过量,实验的操作及现象是
小金带着这个疑问进一步进行了接下来的实验,请你帮助他完成以下探究实验:
【提出问题】镁是否能与水反应?
【实验探究】在两个烧杯中,分别加入等量的冷水和镁条,用酚酞作指示剂,实验过程和现象如图:

【反思与总结】
(1)小金得出的实验结论是
(2)小金发现B试管放置在空气中一会儿,溶液的红色会褪色,这说明溶液的碱性减弱了,于是他大胆作出了一个猜想并设计了验证方案:
| 猜想 | 验证方案 |
| 可能是氢氧化镁的溶解度受温度的影响,温度降低,溶解度变小,从而导致溶液碱性减弱 | 将褪色后的溶液 |
小金通过实验证明了自己的猜想是正确的.
(3)一段时间后,小明观察到镁条在热水中无现象,但当他想到实验室制取二氧化碳不能用稀硫酸与大理石反应时,便有了解释,他的解释是
【提出猜想】猜想①:可能是H2O;猜想②:可能是Na+;猜想③:可能是OH—.
【实验验证】
实验操作 | 实验现象 | 结论 |
| ①用试管取少量蒸馏水,滴入1~2滴无色酚酞试液,振荡 | 试管内溶液仍为无色 | 水分子不能使无色酚酞试液变红色 |
| ②用试管取少量氯化钠溶液,滴入1~2滴无色酚酞试液,振荡 | ||
| ③用试管取少量氢氧化钠溶液,滴入1~2滴无色酚酞试液,振荡 |
【讨论反思】有同学认为猜想①不需要实验验证就可以排除,你认为该同学的理由是
四、填空题 添加题型下试题
甲组同学利用紫色石蕊试液进行鉴别.
实验步骤 | 现象与结论 |
(1)用4支试管,分别取少量的不同溶液,各滴加紫色石蕊试液. | 1支试管中出现红色,则原溶液是(1) |
(2)另用3支试管,分别取少量未确定的溶液,各滴加步骤(1)检验出的溶液 | 1支试管中有气泡产生,则原溶液是Na2CO3溶液. |
(3)另用2支试管,分别取少量未确定的溶液,(2) | 1支试管中有白色沉淀析出,则原溶液是Ca(OH)2溶液.1支试管中无现象,则原溶液是NaOH溶液. |
乙组同学不用其他试剂进行鉴别:
同学 | 实验操作 | 现象 | 结论 |
小敏 | 取3支试管,分别取少量不同的溶液,各滴加剩余的另一种溶液. | 1支试管中有气泡产生,其余2支试管中无现象 | 所滴加的溶液是(3) |
小红 | 1支试管中有白色沉淀析出,其余2支试管(4) | 所滴加的溶液是Na2CO3 | |
小刚 | …… | …… |
乙组同学经过交流后发现如果小刚所滴加的是NaOH溶液,则他的实验现象是
【知识点】 酸、碱、盐的鉴别
五、探究题 添加题型下试题

(1)小刚用A装置未看到明显的现象,他认为CO2与NaOH不发生反应;
(2)小丽用B装置进行实验,看到气球变鼓,认为CO2与NaOH发生反应.
老师指出:CO2与水接触也能看到上述现象,因此上述实验不足以证明CO2与NaOH发生了反应,两位同学经过认真思考,决定从分液漏斗再向B烧瓶中加入足量的稀盐酸,又看到气球变瘪,从而确定CO2与NaOH发生了反应.解释气球变鼓的原因:
(3)证明C中的CO2与NaOH溶液发生反应,两位同学认为利用该装置做个对比实验,补做实验的实验操作:
六、解答题 添加题型下试题

由图可知,HCl与NaOH的反应实质是H+和OH-之间的反应,此反应可表示为:H++OH-=H2O.像这种用实际参与反应的离子来表示反应的式子称为离子方程式.任何复分解反应都可用离子方程式来表示.
【练习】按照书写化学方程式的要求写出下列反应的离子方程式:
HCl溶液与AgNO3溶液反应:
HNO3溶液与Na2CO3溶液反应:
【归纳】复分解反应的实质是:阴阳离子结合生成
【知识点】 书写化学方程式、文字表达式 复分解反应及其应用
七、填空题 添加题型下试题

(1)根据实验现象,白色粉末中一定有
(2)实验中不能用BaCl2溶液代替Ba(NO3)2溶液的理由是:
(3)请写出该实验涉及的所有化学反应方程式:
【知识点】 盐的性质及用途

(1)a点溶液中含有的离子有
(2)当pH=7时,消耗NaOH溶液中的NaOH的质量为
(3)计算稀H2SO4的溶质质量分数.
【知识点】 溶质质量分数的简单计算 中和反应及其应用 溶液的酸碱性与pH值的关系
| 第一次 | 第二次 | 第三次 | 第四次 | 第五次 | 第六次 | |
| 加入稀硫酸的质量(g) | 10 | 10 | 10 | 10 | 10 | 10 |
| 剩余固体的质量(g) | 9.35 | 8.7 | 8.05 | 7.4 | 6.75 | 6.75 |
(提示:铜不与稀硫酸反应)
(1)黄铜样品中锌的质量分数为多少?
(2)所用稀硫酸的质量分数为多少?
【知识点】 溶质质量分数的简单计算 金属的化学性质 根据化学反应方程式的计算
①取10克样品于烧杯中,加入蒸馏水充分溶解,配制成60克溶液;
②在配制的溶液中,加入一定量的硝酸银溶液,恰好完全反应;
⑧将上述混合液过滤,沉淀经洗涤、干燥后,称得质量为14.35克.
(1)在过滤操作中使用的玻璃仪器有:烧杯、
(2)样品中氯化钾的质量分数为多少?
(3)完全反应后,混合液中的硝酸钾质量是多少克?
(4)为了回收硝酸钾,小明对滤液进行蒸发、结晶、称量,发现所得的晶体质量小于计算得出的理论值.造成这种结果的原因可能是
A.晶体没有干燥 B.蒸发时液体飞溅 C.硝酸钾残留在玻璃棒上
【知识点】 溶质质量分数的简单计算 盐的性质及用途 根据化学反应方程式的计算
试卷分析
试卷题型(共 37题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、选择题 | |||
| 1 | 0.65 | 物质的酸碱性 | |
| 2 | 0.85 | 化学变化和物理变化的判别 | |
| 3 | 0.85 | 碱的物理性质及用途 盐的性质及用途 常见物质的俗称 | |
| 4 | 0.85 | 酸的物理性质及用途 碱的化学性质 浓硫酸的性质及浓硫酸的稀释 | |
| 5 | 0.85 | 酸的化学性质 | |
| 6 | 0.85 | 酸的化学性质 常见离子的检验方法及现象 常见物质的鉴定 酸碱指示剂及其性质 | |
| 7 | 0.65 | 碱的物理性质及用途 碱的化学性质 | |
| 8 | 0.94 | 酸的化学性质 复分解反应及其应用 | |
| 9 | 0.85 | 溶液的组成 一定溶质质量分数的溶液的配制 | |
| 10 | 0.65 | 溶解时的吸热或放热现象 酸的化学性质 碱的化学性质 | |
| 11 | 0.85 | 碱的化学性质 盐的性质及用途 酸、碱、盐的贮存 酸碱指示剂及其性质 | |
| 12 | 0.65 | 盐的性质及用途 | |
| 13 | 0.85 | 酸的化学性质 碱的化学性质 盐的性质及用途 | |
| 14 | 0.85 | 碱的化学性质 盐的性质及用途 | |
| 15 | 0.65 | 中和反应及其应用 溶液的酸碱性与pH值的关系 根据化学反应方程式的计算 | |
| 16 | 0.85 | 中和反应及其应用 盐的性质及用途 常见物质的鉴定 | |
| 17 | 0.65 | 盐的性质及用途 酸碱指示剂及其性质 | |
| 18 | 0.4 | 溶质质量分数的简单计算 二氧化碳的实验室制法 | |
| 19 | 0.65 | 离子或物质的共存问题 常见离子的检验方法及现象 常见物质的鉴定 | |
| 20 | 0.65 | 酸的化学性质 盐的性质及用途 | |
| 二、填空题 | |||
| 21 | 0.65 | 浓硫酸的性质及浓硫酸的稀释 有关化学式的计算和推断 质量守恒定律及其应用 | |
| 22 | 0.65 | 酸的化学性质 浓硫酸的性质及浓硫酸的稀释 | |
| 23 | 0.4 | 酸的化学性质 | |
| 24 | 0.65 | 中和反应及其应用 盐的性质及用途 pH值的变化 | |
| 25 | 0.65 | 二氧化碳的实验室制法 影响液体压强大小的因素 物体的浮沉条件及其应用 | |
| 26 | 0.65 | 酸的化学性质 碱的化学性质 盐的性质及用途 | |
| 27 | 0.85 | 碱的化学性质 盐与化肥 常见离子的检验方法及现象 | |
| 31 | 0.4 | 酸、碱、盐的鉴别 | |
| 34 | 0.4 | 盐的性质及用途 | |
| 35 | 0.65 | 溶质质量分数的简单计算 中和反应及其应用 溶液的酸碱性与pH值的关系 | |
| 36 | 0.4 | 溶质质量分数的简单计算 金属的化学性质 根据化学反应方程式的计算 | |
| 37 | 0.4 | 溶质质量分数的简单计算 盐的性质及用途 根据化学反应方程式的计算 | |
| 三、探究题 | |||
| 28 | 0.65 | 酸的化学性质 碱的化学性质 盐的性质及用途 酸碱指示剂及其性质 | |
| 29 | 0.65 | 金属的化学性质 酸碱指示剂及其性质 | |
| 30 | 0.85 | 碱的化学性质 酸碱指示剂及其性质 | |
| 32 | 0.85 | 二氧化碳的化学性质 碱的化学性质 | |
| 四、解答题 | |||
| 33 | 0.65 | 书写化学方程式、文字表达式 复分解反应及其应用 | |