浙江省绍兴市新昌县2020-2021学年九年级上学期期中科学试题(到第2章结束)
浙江
九年级
期中
2021-01-25
366次
整体难度:
容易
考查范围:
常见的物质、物质的运动与相互作用、物质的结构
一、选择题 添加题型下试题
| A.酒精灯:“帽子哪里去了?我的燃料越来越少了。” |
| B.胶头滴管:“谁做的?我的嘴怎么碰碎到试管里去了?” |
| C.锥形瓶:“同学们不爱惜我,我被摔碎了。” |
| D.铁架台:“好难受啊!我在潮湿的空气中生锈了。” |
【知识点】 化学变化和物理变化的判别
| A.pH是反映物质酸碱性强弱的指标,它的范围通常在0-14之间 |
| B.如果我们的环境没有任何污染,那么雨水的pH应该是7 |
| C.浓硫酸的稀释实验中,不把水倒入浓硫酸的的原因之一是浓硫酸溶于水会放出大量热 |
| D.向氢氧化钠溶液中边滴加盐酸边振荡,目的是为了使两者充分反应。 |
【知识点】 碱的化学性质 酸、碱的使用注意事项 溶液的酸碱性与pH值的关系
液体 | 胃液 | 胰液 | 胆汁 | 血浆 |
PH | 0.9-1.5 | 7.5-8.0 | 7.1-7.3 | 7.35-7.45 |
| A.胰液 | B.胃液 |
| C.胆汁 | D.血浆 |
【知识点】 pH值的变化
选项 | A | B | C | D |
物质 | 氯化钠 | 二氧化碳 | 浓硫酸 | 氢气 |
用途 | 除铁锈 | 作气体肥料 | 作干燥剂 | 作燃料 |
A.A  | B.B  | C.C  | D.D |
| A.铁锈与稀盐酸反应溶液变成浅绿色 |
| B.氢氧化钠溶液中加入硫酸铜溶液,产生蓝色沉淀 |
| C.打开盛有浓盐酸的试剂瓶的瓶盖,瓶口出现白烟 |
| D.将氧化铜加入稀硫酸中,产生气泡同时溶液变蓝色 |

A. 紫色石蕊试液“警察” 紫色石蕊试液“警察” | B. 稀盐酸“警察” 稀盐酸“警察” |
C. 无色酚酞试液“警察” 无色酚酞试液“警察” | D. 纯碱溶液“警察” 纯碱溶液“警察” |
【知识点】 常见物质的鉴定

| A.熟石灰 | B.硫酸铜 | C.稀盐酸 | D.氯化钠 |
| A.食盐NaCl | B.苛性钠NaHCO3 | C.纯碱Ba(OH)2 | D.熟石灰CaCO3 |
 性质的描述中,不属于酸的通性的是( )
性质的描述中,不属于酸的通性的是( )| A.使紫色石蕊试液变红 | B.与 发生中和反应 发生中和反应 |
| C.浓硫酸滴到白纸上使纸变黑 | D.与 反应放出氢气 反应放出氢气 |
【知识点】 酸的化学性质
| A.2H2+O2 = 2H2O |
| B.NaOH+HCl=NaCl+H2O |
| C.2H2O2=2H2O+O2↑ |
| D.Fe+CuCl2=Cu+FeCl2 |
【知识点】 置换反应及其应用 识别化学反应基本类型
| A.只含有Mg2+、SO42- |
| B.一定含有Cl-、K+,可能含有Mg2+、SO42- |
| C.一定含有Mg2+、SO42-,可能含有Cl-、K+ |
| D.一定含有K+、Mg2+、Cl-、SO42- |
【知识点】 常见离子的检验方法及现象 物质的推断

A.①—Mg | B.②—CuCl2 | C.③—HCl | D.④—Mg(OH)2 |

| A.甲、乙、丙 | B.甲、乙、丁 |
| C.甲、丙、丁 | D.乙、丙、丁 |
【知识点】 分子的热运动
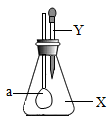
| X | Y | |
| A | CO2 | Ca(OH)2 |
| B | CO | NaOH |
| C | HCl | Ba(OH)2 |
| D | SO2 | NaOH |
| A.A | B.B | C.C | D.D |
二、填空题 添加题型下试题
| 溶液名称 | 白醋 | 稀盐酸 | 氯化钠溶液 | 蒸馏水 | 石灰水 | 氢氧化钾溶液 |
| X汁液 | 红色 | 红色 | 紫色 | 紫色 | 绿色 | 绿色 |
(2)将 X 汁液滴入某溶液中呈绿色,则该溶液 pH
【知识点】 酸碱指示剂及其性质 溶液的酸碱性与pH值的关系
三、探究题 添加题型下试题

(1)物质N属于
(2)若②处有气泡、③处无现象,则可判断锌的金属活动性
(3)若①②④⑤处有明显现象,则M可能为
【知识点】 金属活动性顺序及其应用 酸的化学性质
四、填空题 添加题型下试题
(1)少量存于胃液中帮助消化的是
(2)常用来降低土壤酸性的是
五、解答题 添加题型下试题
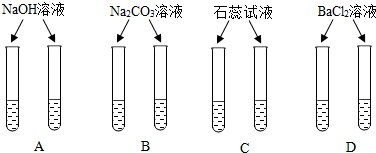
(1)稀盐酸(HCl)和稀硫酸(H2SO4)具有相似的化学性质,原因是它们在电离时都产生了
(2)稀盐酸和稀硫酸都是无色透明的液体,为鉴别它们,小柯设计了如图四种方案(每种方案的两支试管中事先分别加入等量的上述两种酸),其中可行的方案有
六、填空题 添加题型下试题
【知识点】 铁锈的主要成分 金属活动性顺序及其应用 酸的化学性质

(1)二氧化碳应放在
(2)物质②与上下相邻两层物质之间的反应类型都属于
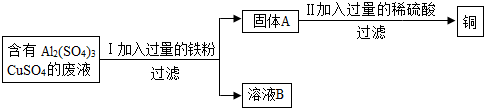
(1)溶液B中所含的溶质是
(2)II中加入过量的稀硫酸的目的是除去铜粉中混有的
【知识点】 金属的化学性质
七、探究题 添加题型下试题
取2毫升该试剂于试管中,滴入无色酚酞试液,发现溶液不变色。则推断该试剂不可能是

再取2毫升该试剂于试管中,滴入A溶液后,根据现象,小明确定该试剂是氯化钠溶液。则A溶液是
八、填空题 添加题型下试题
 中的几种离子,现欲检验两种阴离子是否存在,选用的最佳方案是:先向溶液中滴入足量的
中的几种离子,现欲检验两种阴离子是否存在,选用的最佳方案是:先向溶液中滴入足量的 存在;再取上层清液滴加
存在;再取上层清液滴加【知识点】 盐的性质及用途 常见离子的检验方法及现象

增大压强,HCl由气态变为液态,从微观的角度分析该变化过程中改变的是
A.铁锈 B.水垢 C.硝酸钾 D.苛性钠
在盐酸中加入过量的铁粉充分反应。
①可以看到的现象是
②下图表示该反应前后溶液中存在的主要离子,请写出下列图形代表的离子(填离子符号):

 代表
代表 代表
代表A

(1)如果要还原得到6.4克铜,则理论上需要消耗0.2克氢气,但实际消耗的氢气质量一定大于理论值,造成这一结果最主要的原因是
(2)实验结束后,某同学发现试管中出现的红色物质又变回黑色,其可能的原因是以下的
A.实验开始时先给试管加热,然后通氢气
B.盛放氧化铜的试管口略向上倾斜
C.实验结束时先停止通氢气,再停止加热
D.试管外壁可能还有水
E.加热时氢气本身不纯
【知识点】 金属的冶炼

(2)图乙表示酸碱恰好完全反应的点是
(3)计算稀盐酸中溶质的质量分数。
【知识点】 溶质质量分数的简单计算 pH值的变化
九、解答题 添加题型下试题

(1)稀硫酸反应完时,产生氢气的质量为
(2)该稀硫酸中溶质的质量分数
【知识点】 金属的化学性质 根据化学反应方程式的计算

【知识点】 金属的化学性质
 2Fe+3CO2。计算:
2Fe+3CO2。计算:(1)铁矿石中氧化铁的质量为
(2)这些矿石理论上能炼得铁多少吨?
【知识点】 金属的冶炼 根据化学反应方程式的计算
十、探究题 添加题型下试题
(1)首先对固体的成分进行确定。取少量固体于试管中,加水充分溶解,先加入足量的BaCl2溶液,产生白色沉淀,静置后取上层清液,再加入CuSO4溶液,产生蓝色絮状沉淀。根据实验现象,可确定该固体是 ;
(2)称取10.6g该固体样品于锥形瓶中,加入一定质量分数的稀盐酸,直至过量,得到数据如下表:计算该样品中Na2CO3的质量分数。
| 样品质量 | 反应前总质量 | 反应后总质量 |
| 10.6克 | 148.5克 | 146.3克 |
【知识点】 溶质质量分数的简单计算 酸的化学性质 碱的化学性质 盐的性质及用途
十一、解答题 添加题型下试题
实验次数 | 加入稀盐酸的质量/g | 剩余固体的质量/g |
1 | 10 | 7.5 |
2 | 10 | 5.0 |
3 | 10 | 3.2 |
4 | 10 | a |
根据实验数据计算:
(1)表中a的数值为
(2)求样品中碳酸钙的质量分数
(3)求盐酸中溶质的质量分数
【知识点】 盐的性质及用途 根据化学反应方程式的计算
试卷分析
试卷题型(共 34题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、选择题 | |||
| 1 | 0.85 | 化学变化和物理变化的判别 | |
| 2 | 0.65 | 碱的化学性质 酸、碱的使用注意事项 溶液的酸碱性与pH值的关系 | |
| 3 | 0.65 | pH值的变化 | |
| 4 | 0.85 | 金属的化学性质 酸的化学性质 碱的化学性质 物质除杂或净化 | |
| 5 | 0.85 | 二氧化碳的用途 酸的物理性质及用途 盐的性质及用途 | |
| 6 | 0.94 | 酸的化学性质 盐的性质及用途 | |
| 7 | 0.4 | 常见物质的鉴定 | |
| 8 | 0.85 | 溶液的酸碱性与pH值的关系 酸碱性对生命活动和农作物生长的影响 | |
| 9 | 0.94 | 盐的性质及用途 常见物质的俗称 | |
| 10 | 0.94 | 酸的化学性质 | |
| 11 | 0.94 | 置换反应及其应用 识别化学反应基本类型 | |
| 12 | 0.4 | 常见离子的检验方法及现象 物质的推断 | |
| 13 | 0.65 | 酸的化学性质 盐的性质及用途 | |
| 14 | 0.65 | 分子的热运动 | |
| 15 | 0.65 | 酸的化学性质 碱的化学性质 | |
| 二、填空题 | |||
| 16 | 0.65 | 酸碱指示剂及其性质 溶液的酸碱性与pH值的关系 | |
| 18 | 0.94 | 碱的物理性质及用途 酸的物理性质及用途 | |
| 20 | 0.65 | 铁锈的主要成分 金属活动性顺序及其应用 酸的化学性质 | |
| 21 | 0.65 | 碱的化学性质 盐的性质及用途 复分解反应及其应用 | |
| 22 | 0.85 | 金属的化学性质 | |
| 24 | 0.85 | 盐的性质及用途 常见离子的检验方法及现象 | |
| 25 | 0.4 | 酸的化学性质 碱的化学性质 | |
| 26 | 0.65 | 金属的化学性质 酸的化学性质 | |
| 27 | 0.85 | 盐的性质及用途 物质的推断 | |
| 28 | 0.85 | 金属的冶炼 | |
| 29 | 0.4 | 溶质质量分数的简单计算 pH值的变化 | |
| 三、探究题 | |||
| 17 | 0.85 | 金属活动性顺序及其应用 酸的化学性质 | |
| 23 | 0.85 | 盐的性质及用途 常见物质的鉴定 | |
| 33 | 0.85 | 溶质质量分数的简单计算 酸的化学性质 碱的化学性质 盐的性质及用途 | |
| 四、解答题 | |||
| 19 | 0.65 | 酸的化学性质 中和反应及其应用 盐的性质及用途 酸碱指示剂及其性质 | |
| 30 | 0.65 | 金属的化学性质 根据化学反应方程式的计算 | |
| 31 | 0.85 | 金属的化学性质 | |
| 32 | 0.85 | 金属的冶炼 根据化学反应方程式的计算 | |
| 34 | 0.65 | 盐的性质及用途 根据化学反应方程式的计算 | |



