浙江省宁波市海曙区四校联考2023-2024学年九年级上学期期中科学试题
浙江
九年级
期中
2024-05-21
13次
整体难度:
容易
考查范围:
常见的物质、物质的运动与相互作用、科学探究所需要的基本技能、物质的结构
一、选择题 添加题型下试题
| A.氯化钠、 食盐 、 NaCl | B.氢氧化钙 、熟石灰 、 CaOH |
| C.氢氧化钠 、纯碱 、 NaOH | D.碳酸氢钠 、苏打、  |
【知识点】 常见物质的俗称
| 体液 | 唾液 | 胃液 | 胆汁 | 血液 |
| pH | 6.6~7.1 | 0.9~1.5 | 7.1~7.3 | 7.35~7.45 |
| A.唾液 | B.胃液 | C.胆汁 | D.血液 |
【知识点】 溶液的酸碱性与pH值的关系
A. | B. | C. | D. |
【知识点】 盐与化肥
| A.Li | B.Li2O | C.LiOH | D.Li2CO3 |
【知识点】 质量守恒定律及其应用
A.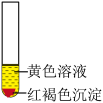 | B.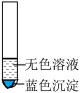 |
C.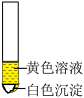 | D.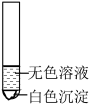 |
【知识点】 盐的性质及用途
| A.甲烷的化学式为C2H4 |
| B.甲烷属于有机物 |
| C.甲烷燃烧只生成水 |
| D.甲烷与空气的混合物遇火一定不会发生爆炸 |
A. 试纸 试纸 | B.酚酞试液 | C.稀硫酸 | D.硝酸钡溶液 |
【知识点】 盐的性质及用途
| A.绿色植物的生长过程,既涉及碳循环,又涉及氧循环 |
| B.碳循环和氧循环过程中均发生了化学变化 |
| C.碳循环和氧循环分别是指二氧化碳和氧气的循环 |
| D.碳循环和氧循环有利于维持大气中氧气和二氧化碳含量的相对稳定 |
A.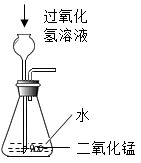 | B. |
C.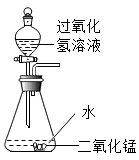 | D. |
【知识点】 常用气体的发生装置和收集装置与选取方法
| 物质 | X | Y | Z | Q |
| 反应前质量/g | 20 | 20 | 20 | 20 |
| 反应后质量/g | a | 16 | 14 | 20 |
| A.a值为30 |
| B.Q可能是催化剂 |
| C.该反应为分解反应 |
| D.参加反应的Y与Z的质量比为2:3 |

下列说法错误的是( )
| A.甲实验不如乙实验环保 |
| B.只根据甲实验“固体消失”这一现象,可验证碳酸氢铵发生了分解 |
| C.乙实验有利于学生分析“固体消失”的原因 |
D.只根据乙实验的现象,可验证:NH4HCO3 NH3↑+CO2↑+H2O NH3↑+CO2↑+H2O |
【知识点】 盐的性质及用途
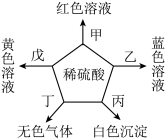
| A.甲可能是无色酚酞试液 | B.乙、戊一定是金属单质 |
| C.稀硫酸与丙生成的白色沉淀不可能属于盐 | D.稀硫酸与丁的反应类型可能是置换反应 |

| A.若丙为单质,则该反应一定是置换反应 |
| B.若丙为碳酸钙,则甲、乙中一定有二氧化碳 |
| C.若丁为氯化铜,则甲、乙中一定有碱 |
| D.甲、乙、丙、丁可能含有同一种元素 |

| A.a点时溶液中的溶质为NaOH、Na2SO4 |
| B.b点时溶液的pH=7 |
| C.原溶液中MgSO4的质量分数为7.5% |
| D.a点时锥形瓶内所得溶液的溶质质量分数约为12.4% |
【知识点】 溶质质量分数的简单计算 盐的性质及用途 根据化学反应方程式的计算
二、填空题 添加题型下试题
(1)制取银朱的反应方程式为:Hg+S=HgS,该反应属于基本反应类型中的
(2)书中记载:十六两汞能制取十七两五钱的硫化汞。增重的“一两五钱”实际上是参加反应的
【知识点】 质量守恒定律及其应用 化合反应及其应用
| 溶液名称 | 白醋 | 稀盐酸 | 氯化钠溶液 | 蒸馏水 | 石灰水 | 氢氧化钾溶液 |
| X汁液 | 红色 | 红色 | 紫色 | 紫色 | 绿色 | 绿色 |
(2)将 X 汁液滴入某溶液中呈绿色,则该溶液 pH
【知识点】 酸碱指示剂及其性质 溶液的酸碱性与pH值的关系
(1)春季:雨水生,万物长。
(2)夏季:小满不满,麦有一险,为促进小麦生长,下列属于复合肥的
a、碳酸氢铵:NH4HCO3
b、磷酸二氢钾:KH2PO4
c、磷矿粉:Ca3(PO4)2
d、磷酸二氢铵:NH4H2PO4
(3)秋季:立秋荞麦白露花,寒露荞麦收到家。秋种时节,为改良酸性土壤
三、探究题 添加题型下试题
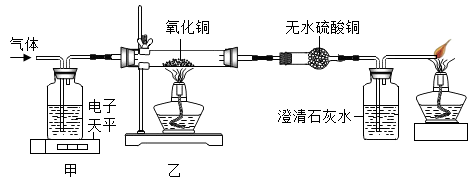
(1)甲装置中盛放的液体是
(2)实验过程中观察到无水硫酸铜不变色,澄清石灰水变浑浊,则原气体中一定含有
【知识点】 常见气体的检验与除杂方法 二氧化碳的检验和验满 金属的冶炼
四、填空题 添加题型下试题

(2)在性质③中,X代表
【知识点】 盐的性质及用途
(1)向A点溶液中滴加紫色石蕊溶液的现象是
(2)曲线上
(3)C点溶液中含有


②若液体B呈无色,且向固体A中加入稀盐酸后产生气泡,则固体A中一定含有的物质有
【知识点】 金属的化学性质
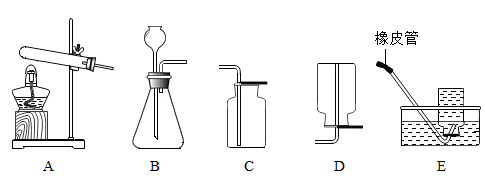
(2)实验室用过氧化氢和二氧化锰制取氧气,反应的化学方程式为
 ,选用BE 装置组合后,采用检验装置气密性的方法如下:将E 处的橡密皮管封,向B 中长颈漏斗中加水,若观察到
,选用BE 装置组合后,采用检验装置气密性的方法如下:将E 处的橡密皮管封,向B 中长颈漏斗中加水,若观察到(1)验证可溶性碱能与酸反应。打开活塞a,向锥形瓶中逐滴滴入稀盐酸。Ba(OH)2溶液与稀盐酸恰好完全反应的实验现象是
(2)验证可溶性碱能与CO2反应。完成(1)后,打开活塞b,向锥形瓶中滴入足量的NaOH溶液后
(3)验证可溶性碱能与盐溶液反应。完成(2)后,装置乙中锥形瓶内的溶液呈红色,取少量该溶液于试管中,滴入足量CuSO4溶液,观察到有蓝色沉淀生成。据上述实验现象能否验证NaOH溶液与CuSO4溶液反应,判断并说明理由

【知识点】 碱的化学性质 盐的性质及用途 常见离子的检验方法及现象 酸碱指示剂及其性质
五、探究题 添加题型下试题
步骤1:连接装置并检查装置气密性。
步骤2:取1克炭粉和10克氧化铜,混合均匀,加入到试管中
步骤3:按图所示固定好试管,连接好装置,用酒精喷灯加热混合固体,并记录实验现象。
(1)步骤3中,加热一段时间后能观察到的实验现象是
(2)实验结束后,小金先将导管从液体中移出,再熄灭酒精喷灯
(3)小金所设计的这个实验要不要进行尾气处理?说说你的理由。

【知识点】 金属的冶炼

(2)实验开始一段时间后,可观察到
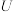 形管中两侧液面高低情况是
形管中两侧液面高低情况是(3)为进一步探究温度对铁生锈快慢的影响。小博将该装置(每组装置内铁丝绒质量均相等且足量)分别置于不同温度下进行实验,4小时后记录每组
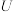 形管两端液面高度差,具体数据如下表:
形管两端液面高度差,具体数据如下表:| 温度/摄氏度 | 10 | 20 | 30 | 40 | 50 | 60 | 70 |
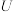 形管两端液面高度差/厘米 形管两端液面高度差/厘米 | 2 | 4 | 6 | 7 | 8 | 8 | 8 |
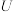 形管两端液面高度差不变。请分析出现该现象的原因:
形管两端液面高度差不变。请分析出现该现象的原因:【知识点】 金属锈蚀的条件及其防护
六、解答题 添加题型下试题
(1)七氟烷由
(2)七氟烷的相对分子质量是
(3)七氟烷中碳元素和氧元素的质量比
【知识点】 化学式 有关化学式的计算和推断
(1)求硫酸铵中氮元素的质量分数。
(2)尿素CO(NH2)2 也是一种常用的氮肥,某市场中硫酸铵和尿素每千克售价分别为1.3元和1.8元,根据它们含氮的质量分数分析肥效,购买哪种化肥更经济?
【知识点】 有关化学式的计算和推断
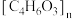 (相对分子质量为
(相对分子质量为 ),一定条件下,反应可表示为:
),一定条件下,反应可表示为: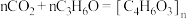 。若制取204吨该塑料,理论上可以少排放多少吨二氧化碳?(写出计算过程)
。若制取204吨该塑料,理论上可以少排放多少吨二氧化碳?(写出计算过程)
【知识点】 根据化学反应方程式的计算
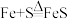 ):
):第一次 | 第二次 | 第三次 | |
硫粉的质量/g | 16 | 32 | 32 |
铁粉的质量/g | 28 | 28 | 56 |
硫化亚铁(FeS)的质量/g | 44 | 44 | 88 |
(2)通过实验说明,参加反应的各物质之间存在着比例关系,从如表可知,参加反应的铁和硫的质量比是
(3)若该同学要进行第四次实验,如果要将48克硫粉完全反应,则需要铁粉多少克?能生成硫化亚铁多少克
【知识点】 根据化学反应方程式的计算
(1)产生CO2的总质量。
(2)石灰石中碳酸钙的质量分数(写出计算过程)。

【知识点】 二氧化碳的实验室制法 质量守恒定律及其应用 根据化学反应方程式的计算
七、填空题 添加题型下试题

(2)图乙表示酸碱恰好完全反应的点是
(3)计算稀盐酸中溶质的质量分数。
【知识点】 溶质质量分数的简单计算 pH值的变化
八、解答题 添加题型下试题

(2)根据实验数据,通过化学方程式计算20mL 过氧化氢溶液中溶质的质量。
(3)已知上述20mL 过氧化氢溶液的成本为0.4元,若在实验室用同样的过氧化氢溶液制取 600L氧气(密度取 1.4g/L),需要的成本是
(4)小科连接图甲和图丙装置,用注射器另取4mL 同样的过氧化氢溶液,通过直接测量氧气的体积来计算成本。若不考虑导管对实验的影响,以下分析正确的是
A.广口瓶中的水面上有少量植物油,能防止氧气溶于水
B.实验前图丙装置中广口瓶内的水量不会影响测量结果
C.读数时量筒中的水面高于广口瓶内的液面导致测得氧气的体积偏小
D.测得氧气的体积等于量筒中增加的水的体积减去加入的过氧化氢溶液的体积
试卷分析
试卷题型(共 33题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、选择题 | |||
| 1 | 0.85 | 常见物质的俗称 | |
| 2 | 0.94 | 溶液的酸碱性与pH值的关系 | |
| 3 | 0.94 | 盐与化肥 | |
| 4 | 0.94 | 质量守恒定律及其应用 | |
| 5 | 0.94 | 盐的性质及用途 | |
| 6 | 0.85 | 甲烷、乙炔等常见有机物的性质和用途 有机物与无机物的区别 质量守恒定律及其应用 | |
| 7 | 0.85 | 盐的性质及用途 | |
| 8 | 0.85 | 自然界中氧循环 自然界中碳循环 | |
| 9 | 0.85 | 常用气体的发生装置和收集装置与选取方法 | |
| 10 | 0.85 | 催化剂在化学反应中的作用 质量守恒定律及其应用 化合反应及其应用 分解反应及其应用 | |
| 11 | 0.85 | 盐的性质及用途 | |
| 12 | 0.65 | 酸的化学性质 盐的性质及用途 | |
| 13 | 0.85 | 金属的化学性质 酸的化学性质 酸碱指示剂及其性质 置换反应及其应用 | |
| 14 | 0.65 | 酸的化学性质 碱的化学性质 盐的性质及用途 置换反应及其应用 | |
| 15 | 0.85 | 溶质质量分数的简单计算 盐的性质及用途 根据化学反应方程式的计算 | |
| 二、填空题 | |||
| 16 | 0.85 | 质量守恒定律及其应用 化合反应及其应用 | |
| 17 | 0.65 | 酸碱指示剂及其性质 溶液的酸碱性与pH值的关系 | |
| 18 | 0.85 | 中和反应及其应用 盐与化肥 | |
| 20 | 0.85 | 盐的性质及用途 | |
| 21 | 0.85 | 中和反应及其应用 酸碱指示剂及其性质 | |
| 22 | 0.85 | 金属的化学性质 | |
| 23 | 0.65 | 常用气体的发生装置和收集装置与选取方法 氧气的制取装置 二氧化碳的实验室制法 二氧化碳的物理性质 | |
| 24 | 0.4 | 碱的化学性质 盐的性质及用途 常见离子的检验方法及现象 酸碱指示剂及其性质 | |
| 32 | 0.4 | 溶质质量分数的简单计算 pH值的变化 | |
| 三、探究题 | |||
| 19 | 0.65 | 常见气体的检验与除杂方法 二氧化碳的检验和验满 金属的冶炼 | |
| 25 | 0.85 | 金属的冶炼 | |
| 26 | 0.65 | 金属锈蚀的条件及其防护 | |
| 四、解答题 | |||
| 27 | 0.85 | 化学式 有关化学式的计算和推断 | |
| 28 | 0.65 | 有关化学式的计算和推断 | |
| 29 | 0.65 | 根据化学反应方程式的计算 | |
| 30 | 0.65 | 根据化学反应方程式的计算 | |
| 31 | 0.85 | 二氧化碳的实验室制法 质量守恒定律及其应用 根据化学反应方程式的计算 | |
| 33 | 0.65 | 氧气的制取装置 实验室制取氧气的反应原理 质量守恒定律及其应用 根据化学反应方程式的计算 | |

 可用于治疗锌缺乏引起的食欲不振、生长发育迟缓等病症。下列选项中的两种物质,
可用于治疗锌缺乏引起的食欲不振、生长发育迟缓等病症。下列选项中的两种物质, 和
和
 和
和 和
和


