小华同学通过阅读课外资料得知,潜水艇中常用过氧化钠(Na2O2)作为供氧剂,有关反应的化学方程式为:2Na2O2+2CO2=== 2Na2CO3+O2,2Na2O2+2H2O=== 4NaOH+O2↑,于是他用如图所示装置来制取CO2并验证其与Na2O2的反应:
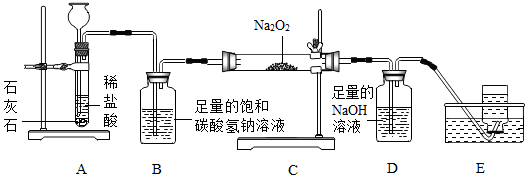
(1)装置B的作用是____________ 。
(2)反应后装置C硬质玻璃管中固体的成分是什么?小华为此又进行了如下探究:
【猜想与假设】猜想一:Na2CO3;猜想二:Na2CO3和Na2O2
猜想三:Na2CO3和NaOH;猜想四:Na2CO3、NaOH、Na2O2
【设计实验】
(3)【反思与评价】反应后装置C硬质玻璃管中的固体含有NaOH,原因可能是__________________________________ 。

(1)装置B的作用是
(2)反应后装置C硬质玻璃管中固体的成分是什么?小华为此又进行了如下探究:
【猜想与假设】猜想一:Na2CO3;猜想二:Na2CO3和Na2O2
猜想三:Na2CO3和NaOH;猜想四:Na2CO3、NaOH、Na2O2
【设计实验】
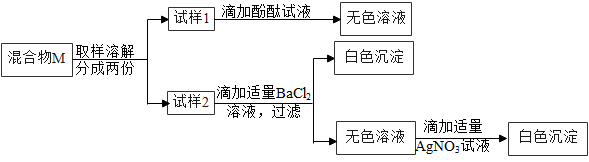
| 实验操作 | 实验现象 | 实验结论 |
| ①取少量样品于试管中,加入足量的水,振荡 | 固体完全溶解, | 样品中一定没有Na2O2 |
| ②取少量实验①所得溶液于另一试管中,加入过量的BaCl2溶液,振荡 | 有白色沉淀产生 | 猜想三正确 |
| ③取少量实验②所得上层清液于另一试管中,加入 | 有白色沉淀产生 |
(3)【反思与评价】反应后装置C硬质玻璃管中的固体含有NaOH,原因可能是
更新时间:2021-06-08 11:34:44
|
相似题推荐
探究题
|
适中
(0.65)
【推荐1】在用氢气还原氧化铜的方法测定某氧化铜样品的纯度(杂质不与氢气反应),同学们设计 了以下实验装置,准确称取20克样品进行实验。
(1)在实验中,乙装置的目的是_______ 。
(2)准确称取完全反应前后装置丙和丁的质量如表。
小明根据装置丙减少的质量就是氧元素质量,求得氧化铜的质量为15.6克,纯度为78%。小红想根据装置丁的质量变化来求出氧化铜样品的纯度,请帮小红写出计算过程。__________ 。
(3)比较两种计算结果,请分析导致这一结果的原因可能是______ 。
A.通入的氢气量不足
B.空气中的水分被丁处浓硫酸吸收
C.氧化铜样品受潮
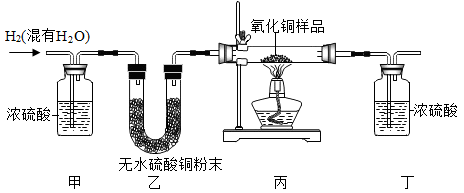
(1)在实验中,乙装置的目的是
(2)准确称取完全反应前后装置丙和丁的质量如表。
| 装置丙质量/克 | 装置丁质量/克 | |
| 反应前 | 48.8 | 161.2 |
| 反应后 | 45.7 | 164.8 |
小明根据装置丙减少的质量就是氧元素质量,求得氧化铜的质量为15.6克,纯度为78%。小红想根据装置丁的质量变化来求出氧化铜样品的纯度,请帮小红写出计算过程。
(3)比较两种计算结果,请分析导致这一结果的原因可能是
A.通入的氢气量不足
B.空气中的水分被丁处浓硫酸吸收
C.氧化铜样品受潮

您最近半年使用:0次
探究题
|
适中
(0.65)
【推荐2】小明家有一包已经打开近一个月的面粉,怀疑不能再食用,可母亲说,面粉还是好的,为什么不能食用呢?小明决定对家中的面粉做一次新鲜度的检验,于是收集有关面粉变质的信息如下:
(1)久置的面粉由于空气中的氧气、水分和各种微生物的作用,会分解成醇和各种有机酸,导致 变质,变质的面粉中有机酸的含量增多。
(2)有机酸和盐酸一样可用NaOH溶液中和,根据面粉中酸的含量可以确定面粉是否新鲜或变质。
(3)如果要测定的面粉消耗的NaOH与同等质量的新鲜面粉消耗的NaOH相仿,说明是新鲜的,如果消耗的氢氧化钠溶液体积是标准液的2.5倍以上,说明面粉已经变质,不能食用,若在2.5倍以下,则面粉不够新鲜,但还能食用。
实验步骤:
步骤一:取甲、乙两只均盛有40mL蒸馏水的锥形瓶,分别加入5克新鲜的面粉和5克待测的面粉,搅拌直至面粉液中不存在任何面团。
步骤二:在配好的面粉液中,分别加入3滴无色酚酞试液,此时,观察到锥形瓶中的液态物质不变色。
步骤三:用滴管向锥形瓶内逐滴加入0.02%的氢氧化钠溶液,边滴边振荡,直到氢氧化钠和有机酸恰好完全反应。分别记下消耗掉的氢氧化钠溶液体积为10毫升和15毫升。
请你帮他解决一些问题:
(1)小明进行上述实验的目的是探究家中面粉的______________ ;
(2)实验中小明根据什么现象来判断氢氧化钠和有机酸恰好完全反应?______________ ;
(3)小明在实验时,自家面粉消耗的NaOH溶液体积是新鲜面粉消耗的1.5倍,他得出的结论是__________________________ 。
(1)久置的面粉由于空气中的氧气、水分和各种微生物的作用,会分解成醇和各种有机酸,导致 变质,变质的面粉中有机酸的含量增多。
(2)有机酸和盐酸一样可用NaOH溶液中和,根据面粉中酸的含量可以确定面粉是否新鲜或变质。
(3)如果要测定的面粉消耗的NaOH与同等质量的新鲜面粉消耗的NaOH相仿,说明是新鲜的,如果消耗的氢氧化钠溶液体积是标准液的2.5倍以上,说明面粉已经变质,不能食用,若在2.5倍以下,则面粉不够新鲜,但还能食用。
实验步骤:
步骤一:取甲、乙两只均盛有40mL蒸馏水的锥形瓶,分别加入5克新鲜的面粉和5克待测的面粉,搅拌直至面粉液中不存在任何面团。
步骤二:在配好的面粉液中,分别加入3滴无色酚酞试液,此时,观察到锥形瓶中的液态物质不变色。
步骤三:用滴管向锥形瓶内逐滴加入0.02%的氢氧化钠溶液,边滴边振荡,直到氢氧化钠和有机酸恰好完全反应。分别记下消耗掉的氢氧化钠溶液体积为10毫升和15毫升。
请你帮他解决一些问题:
(1)小明进行上述实验的目的是探究家中面粉的
(2)实验中小明根据什么现象来判断氢氧化钠和有机酸恰好完全反应?
(3)小明在实验时,自家面粉消耗的NaOH溶液体积是新鲜面粉消耗的1.5倍,他得出的结论是
您最近半年使用:0次
探究题
|
适中
(0.65)
【推荐3】甜叶菊苷是一种新型甜味剂,其甜度为蔗糖的250~450倍,某实验小组欲探究甜叶菊苷的元素组成,进行了如图1进行操作,并分别将干冷的烧杯和蘸有澄清石灰水的烧杯倒置与火焰上方。

(1)小晴认为该实验设计不严谨,原因是________ 。经改进试验后,检验到甜叶菊苷在氧气中充分燃烧的产物只有二氧化碳和水,由此确定甜叶菊苷中一定含有碳、氢元素。
(2)为了进步确定其元素组成,小晴利用如图2装置进行实验。(已知:装置中C中的氧化铜能确保甜叶菊苷中的碳元素完全转化为二氧化碳)
①实验中B装置的作用是什么?________
②4.02g甜叶菊苷在C装置中充分反应后,D装置增重2.7g,E装置增重8.36g。(产物完全被吸收);数据分析:4.02g甜叶菊苷中氧元素的质量为________ g,从而确定甜叶菊苷是由碳、氢、氧元素组成。
③实验前后在装置中通N2都能减小该实验中的误差,但也有同学认为这个实验中其实不通N2也能通过实验操作减小这方面误差,该同学这样说的理由是________ 。

(1)小晴认为该实验设计不严谨,原因是
(2)为了进步确定其元素组成,小晴利用如图2装置进行实验。(已知:装置中C中的氧化铜能确保甜叶菊苷中的碳元素完全转化为二氧化碳)
①实验中B装置的作用是什么?
②4.02g甜叶菊苷在C装置中充分反应后,D装置增重2.7g,E装置增重8.36g。(产物完全被吸收);数据分析:4.02g甜叶菊苷中氧元素的质量为
③实验前后在装置中通N2都能减小该实验中的误差,但也有同学认为这个实验中其实不通N2也能通过实验操作减小这方面误差,该同学这样说的理由是
您最近半年使用:0次
探究题
|
适中
(0.65)
【推荐1】化学小组同学设计了探究二氧化碳与氢氧化钠溶液反应的方案,实验步骤如下:
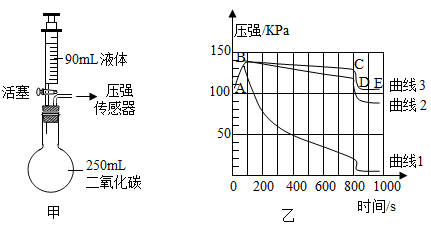
(1)如甲图所示装置的气密性良好,三瓶250mL的烧瓶内收集满CO2气体,三个注射器内各装有90mL的液体(分别是水、40%的氢氧化钠溶液、饱和澄清石灰水)。连接好装置和压强传感器。
(2)三位同学同时迅速将注射器内90mL的液体注入各自烧瓶中,关闭活塞。
(3)一段时间后,同时振荡烧瓶。观察传感器定量实时地传回烧瓶内气压变化形成的图像情况如乙图所示。
试回答下列问题:
(1)曲线1对应反应的化学方程式为_______ ;曲线1与曲线2差异较大的原因是_______ 。
(2)导致曲线3中CD段气压急速减小的操作是_______ 。不改变装置和药品的情况下,进一步降低E点的方法是_______ 。
(3)对比曲线1、2、3,不能得出的结论是_______ (填序号,多选)。
①CO2能与水发生反应
②CO2能与NaOH溶液发生反应
③检验CO2用饱和澄清石灰水较适
④吸收CO2用NaOH溶液较合适

(1)如甲图所示装置的气密性良好,三瓶250mL的烧瓶内收集满CO2气体,三个注射器内各装有90mL的液体(分别是水、40%的氢氧化钠溶液、饱和澄清石灰水)。连接好装置和压强传感器。
(2)三位同学同时迅速将注射器内90mL的液体注入各自烧瓶中,关闭活塞。
(3)一段时间后,同时振荡烧瓶。观察传感器定量实时地传回烧瓶内气压变化形成的图像情况如乙图所示。
试回答下列问题:
(1)曲线1对应反应的化学方程式为
(2)导致曲线3中CD段气压急速减小的操作是
(3)对比曲线1、2、3,不能得出的结论是
①CO2能与水发生反应
②CO2能与NaOH溶液发生反应
③检验CO2用饱和澄清石灰水较适
④吸收CO2用NaOH溶液较合适
您最近半年使用:0次
探究题
|
适中
(0.65)
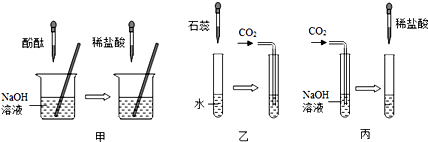
【推荐2】为探究CO2和NaOH是否确实发生了化学反应,某实验小组的同学设计出了上图4种实验装置,请回答下列问题:
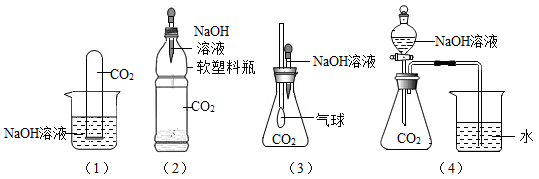
(1)简述(1)出现的实验现象:____________________________________________ 。
(2)某同学认为以上实验仍无法证明CO2和NaOH确实发生了化学反应,该同学质疑的依据是:_____________________ 。

(1)简述(1)出现的实验现象:
(2)某同学认为以上实验仍无法证明CO2和NaOH确实发生了化学反应,该同学质疑的依据是:
您最近半年使用:0次
探究题
|
适中
(0.65)
【推荐1】隔夜菜是否能吃,主要在于烧熟后的隔夜菜中亚硝酸盐含量的变化是否符合食品安全要求。蔬菜中的硝酸盐来自生长过程中所施氮肥。空气中的微生物(如硝酸盐还原菌)进入到蔬菜中,会产生一种还原酶,使蔬菜中的部分硝酸盐还原成亚硝酸盐。烧熟后的菜在食用和保存阶段都会有一些细菌进入;做熟的蔬菜更适合细菌生长。
某研究小组对烧熟的菜中亚硝酸盐含量做了测试,数据如下表:
盖有保鲜膜的菜肴在4℃的冰箱中放置不同时间的亚硝酸盐含量(单位: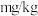 )
)
将一份红烧鲫鱼样本(不盖保鲜膜)在常温下放置4小时,测定其亚硝酸盐含量为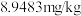 .请根据以上材料,回答下列问题:
.请根据以上材料,回答下列问题:
(1)亚硝酸盐中含有 ,其中氮元素的化合价是
,其中氮元素的化合价是_____ ;
(2)根据表中的数据,菜中的亚硝酸盐含量变化的共同规律是_____ ;
(3)要使烧熟后的隔夜菜中亚硝酸盐含量尽可能低,保存的条件应该是_____ ;
(4)炒菜过程中温度一般在 以上,你认为从生菜炒到熟菜过程中的亚硝酸盐含量是否会持续增加
以上,你认为从生菜炒到熟菜过程中的亚硝酸盐含量是否会持续增加_____ ,原因是_____ 。
某研究小组对烧熟的菜中亚硝酸盐含量做了测试,数据如下表:
盖有保鲜膜的菜肴在4℃的冰箱中放置不同时间的亚硝酸盐含量(单位:
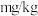 )
)| 菜肴 | 半小时 | 6小时 | 18小时 | 24小时 |
| 炒青菜 | 0.6861 | 0.7982 | 4.3333 | 5.3624 |
| 韭菜炒蛋 | 1.8153 | 1.9249 | 2.8390 | 5.6306 |
| 红烧肉 | 2.4956 | 4.2558 | 4.3668 | 5.5188 |
| 红烧鲫鱼 | —— | 2.0948 | 3.2300 | 7.2397 |
将一份红烧鲫鱼样本(不盖保鲜膜)在常温下放置4小时,测定其亚硝酸盐含量为
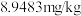 .请根据以上材料,回答下列问题:
.请根据以上材料,回答下列问题:(1)亚硝酸盐中含有
 ,其中氮元素的化合价是
,其中氮元素的化合价是(2)根据表中的数据,菜中的亚硝酸盐含量变化的共同规律是
(3)要使烧熟后的隔夜菜中亚硝酸盐含量尽可能低,保存的条件应该是
(4)炒菜过程中温度一般在
 以上,你认为从生菜炒到熟菜过程中的亚硝酸盐含量是否会持续增加
以上,你认为从生菜炒到熟菜过程中的亚硝酸盐含量是否会持续增加
您最近半年使用:0次
探究题
|
适中
(0.65)
【推荐2】为测定石灰石样品中碳酸钙含量,某小组同学在一定量的样品中加入足量稀盐酸,利用生成CO2的质量来测定(忽略稀盐酸挥发的影响)。

(1)小科用图甲装置实验,通过测定反应前后D装置质量的变化来得到CO2质量。为了避免水蒸气对实验的影响,使测量结果更准确,装置C中应装入______ (填试剂名称)。
(2)小明用图乙装置实验,通过测定反应前后装置总质量的变化来得到CO2质量。他用碱石灰做干燥剂,请判断这种做法是否合理并说出理由。______
(3)实验时,正确选择干燥剂后,两装置均可通过左侧导管鼓入某种气体一段时间,来进一步减小误差。下列操作可行的是______ 。
【实验结论】在原反应结束时,稀盐酸与石灰石没有恰好完全反应,石灰石中碳酸钙有剩余。

(1)小科用图甲装置实验,通过测定反应前后D装置质量的变化来得到CO2质量。为了避免水蒸气对实验的影响,使测量结果更准确,装置C中应装入
(2)小明用图乙装置实验,通过测定反应前后装置总质量的变化来得到CO2质量。他用碱石灰做干燥剂,请判断这种做法是否合理并说出理由。
(3)实验时,正确选择干燥剂后,两装置均可通过左侧导管鼓入某种气体一段时间,来进一步减小误差。下列操作可行的是
| 选项 | 实验装置 | 反应开始前鼓入的气体 | 反应结束后鼓入的气体 |
| A | 甲 | 氮气 | 氮气 |
| B | 甲 | 干燥空气 | 干燥空气 |
| C | 乙 | 氮气 | 氮气 |
| D | 乙 | 干燥空气 | 干燥空气 |
【实验结论】在原反应结束时,稀盐酸与石灰石没有恰好完全反应,石灰石中碳酸钙有剩余。
您最近半年使用:0次