2018学年南武教育集团初三调研测试(六)化学
广东
九年级
一模
2021-09-27
191次
整体难度:
适中
考查范围:
物质的化学变化、身边的化学物质、化学与社会发展、化学实验、物质构成的奥秘
一、选择题 添加题型下试题
| A.石墨作电极 | B.干冰用于人工降雨 |
| C.氢氧化钠去除油污 | D.浓硫酸作干燥剂 |
| A.空气中的氮气因化学性质不活泼,常用作保护气 |
| B.空气中的氧气具有氧化性,是常用的燃料之一 |
| C.空气中的稀有气体无色无味,没有任何用途 |
| D.全球气候变暖、臭氧层破坏和酸雨等与空气污染无关 |
| A.金刚石切割玻璃——硬度大 | B.石墨用作电池电极——导电性良好 |
| C.活性炭除异味——吸附性 | D.干冰用于人工降雨——能与水反应 |
| A.生活中常用的纤维、塑料、合金都属于有机合成材料 |
| B.青少年每日必须摄入足够量的钙,否则会引起发育不良 |
| C.油脂是人体的重要供能物质,油炸食品、肥肉等富含油脂,应多食用 |
| D.可用甲醛水溶液浸泡海鲜,达到保鲜的目的 |
| A.硬水通过煮沸或蒸馏都能转化为纯净水 | B.天然水里多数含有杂质,属于混合物 |
| C.通过过滤的方法可除去水中难溶性杂质 | D.水是一种常用的溶剂 |
【知识点】 常见几种净化水操作的比较解读 纯水、天然水与自来水解读

| A.该反应属于置换反应 | B.能与血红蛋白结合的只有 |
| C.分子总数在反应前后没有变化 | D.反应中 发生还原反应 发生还原反应 |
【知识点】 置换反应解读 质量守恒定律的微观解释解读 微粒图像的分析及应用解读
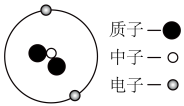
| A.其原子核内中子数和核外电子数相等 | B.该原子的化学性质比较活泼 |
C.该原子的结构示意图为 | D.该原子的质量约为其中子质量的3倍 |
| A.电线一般用铜制,而不用银制,是因为铜的导电性比银好 |
| B.在日常生活中,大量使用的金属材料常常不是纯金属,而是合金 |
| C.“真金不怕火炼”,该俗语说明金的化学性质不活泼 |
| D.废旧金属的回收利用可以减少环境的污染 |
| A.将氯化铵和氯化钾混合可制得复合肥料 |
| B.氯化钾、硫酸钾和氢氧化钾都可用作钾肥 |
| C.尿素和氯化铵可通过加熟石灰研磨的方法区分 |
| D.残留农药可通过农作物转移到人体中 |
【知识点】 常见化肥的种类及性质解读 合理使用化肥和农药解读
 ”表示的微粒是
”表示的微粒是
| A.H+ | B.Cl- | C.Fe2+ | D.Fe3+ |
【知识点】 中和反应的概念及微观本质解读
| A.硫化丙烯的相对分子质量为(12×3+1×6+32)g |
| B.硫化丙烯中硫元素的质量分数最小 |
| C.硫化丙烯分子中碳、氢、硫原子个数比为3:6:1 |
| D.硫化丙烯在空气中燃烧只生成CO2和H2O |
| A.A>B>D | B.D>B>A | C.C>A>B>D | D.A>B>D>C |
【知识点】 金属与盐溶液反应 金属活动顺序理解和判断解读
A. 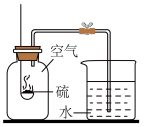 测空气中氧气含量 测空气中氧气含量 | B. 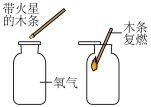 氧气的验满 氧气的验满 |
C. 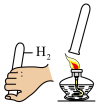 验证氢气的纯度 验证氢气的纯度 | D. 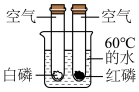 验证燃烧需要氧气 验证燃烧需要氧气 |

| A.10℃时,100g饱和KNO3溶液中含有20.9g KNO3 |
| B.20℃时,NaCl溶液的溶质质量分数最大 |
| C.70℃时接近饱和的MgSO4溶液,通过升温或降温都能转化成饱和溶液 |
| D.将10℃的饱和KNO3溶液升温至50℃,其溶质质量分数增大 |
【知识点】 饱和溶液和不饱和溶液的转换解读 固体溶解度曲线的应用解读
| A.铜和硝酸银溶液 | B.稀硫酸和小苏打溶液 |
| C.稀盐酸和澄清石灰水 | D.烧碱溶液和氯化钾溶液 |
| A.在空气中打开盛浓盐酸的试剂瓶瓶塞,有刺激性气味,冒出白烟 |
| B.木炭在氧气中燃烧,发白光,生成二氧化碳 |
| C.镁条与足量的稀盐酸反应,镁条逐渐消失,产生大量气泡,同时放热 |
| D.硫在空气中燃烧,会发出明亮的蓝紫色火焰,产生有刺激性气味的气体 |
| A.392g水 | B.390g 20%的稀硫酸 |
| C.780g5%的稀硫酸 | D.780g10%的稀硫酸 |
| A.滴加洗涤剂能将餐具上的油污洗掉,因为洗涤剂能溶解油污 |
| B.打开浓盐酸试剂瓶瓶塞,能闻到刺激性气味,是因为分子在不断地运动 |
| C.浓硫酸可用作气体的干燥剂,因为浓硫酸具有吸水性 |
| D.吃松花蛋时可加入少量食醋,因为食醋能消除蛋中所含碱性物质的涩味 |
【知识点】 浓硫酸的物理、化学性质解读 中和反应的实际应用解读
| 选项 | 物质 | 杂质 | 试剂 | 操作 |
| A | CaO | CaCO3 | 稀盐酸 | 过滤,洗涤,干燥 |
| B | MnO2 | KCl | 水 | 过滤,洗涤,干燥 |
| C | KNO3溶液 | AgNO3 | NaCl溶液 | 过滤 |
| D | CO2 | HCl | NaOH溶液 | 洗气 |
| A.A | B.B | C.C | D.D |
二、填空与简答 添加题型下试题
(1)①人在高原地区容易因缺氧等因素引起高原反应。这里的“氧”指的是
A分子 B原子 C离子 D元素
②为缓解高原反应的症状,进藏时最好随身携带高原便携氧气瓶。从微观角度看,100L的氧气压缩到0.8L的氧气瓶,该过程中
(2)载人航天器工作舱中的空气要与地球上的空气基本一致。已知在同温同压下,气体的体积之比等于分子个数之比。
①用微观示意图表示工作舱中空气的主要成分,下图中最合理的是

②宇航员呼出的CO2用氢氧化锂(LiOH)吸收,生成一种溶液X,该反应的化学方程式为
③航天器返回地面后,可将溶液X与适量
| 物质 | 硫酸亚铊 (Tl2SO4) | 氢氧化亚铊 (TlOH) | 氧化亚铊 (Tl2O) | 氯化亚铊 (TlCl) |
| 颜色 | 溶液呈无色 | 溶液呈黄色 | 黑色固体 | 白色固体 |
| 溶解性 | 易溶 | 易溶 | 难溶 |
(2)取少量Tl2SO4溶液于试管中,滴加过量Ba(OH)2溶液,振荡,观察到的实验现象是
(3)下列反应一定不能发生的有
A Tl2SO4 + HCl B Tl2O + H2SO4 C TlCl + Na2SO4 D TlOH + SO3

(1)25℃时,将20g甲固体加入到50g水中,充分溶解并恢复到原温度后,得到溶液的质量为
(2)要使35℃时接近饱和的丙溶液变成该温度下的饱和溶液,可采用的一种方法是
(3)现有操作步骤:A.溶解B.过滤C.降温结晶D.加热浓缩。若甲固体中含有少量乙,则提纯甲的操作步骤的顺序是
(4)若将35℃时甲的饱和溶液降温到25℃,则其溶液的溶质质量分数会
【知识点】 固体溶解度曲线的应用解读
第一步:将钛铁矿粉与炭粉混合,发生反应:2FeTiO3 + C
 2Fe + 2X + CO2↑
2Fe + 2X + CO2↑第二步:将第一步得到的X与炭粉混合,高温条件下通入Cl2,生成TiCl4和一种可燃性气体。
第三步:高温下,生成的TiCl4与Mg发生置换反应,得到金属钛。
(1)FeTiO3读作钛酸亚铁,其中钛元素的化合价为
A金属氧化物 B酸 C盐 D化合物
(2)第一步反应的化学方程式中,X的化学式为
(3)第二步反应中,参加反应的炭粉与Cl2的质量比为
(4)钛铁矿中钛酸亚铁的含量为b%,若要制得质量为a g的钛金属,理论上最少需要钛铁矿石的质量为
【知识点】 保护和利用金属资源的有效途径解读 金属冶炼的计算解读

相关物质的溶解度(20℃时)如下表:
| 物质 | KMnO4 | K2CO3 | K2SO4 |
| 溶解度/g | 6.34 | 111 | 11.1 |
(2)“浓缩结晶”后得到的母液中,溶质是
(3)“干燥”过程中温度不宜过高的原因
(4)本流程中可循环利用的物质(水除外)是
(5)“通CO2酸化”,化学方程式为:3K2MnO4+2CO2═2KMnO4+MnO2↓+2K2CO3;若用稀H2SO4酸化,化学方程式为:3K2MnO4+2H2SO4═2KMnO4+MnO2↓+2K2SO4+2H2O;工业上不采用稀H2SO4酸化的原因是
三、实验题 添加题型下试题
步骤Ⅰ:取一定量的白色粉末加入足量的水,振荡,静置,得白色沉淀,上层清液为无色。
步骤Ⅱ:过滤,在白色沉淀中加入足量稀盐酸,沉淀全部溶解,且有气泡产生。
(1)步骤Ⅰ中得到的白色沉淀是
(2)根据上述实验,暂不能推断混合物中是否含有的成分是
(3)设计实验进一步确定混合物组成,依次用到的试剂是

(1)操作A中,如果粗盐和5g砝码位置颠倒,称量出的粗盐质量
(2)操作B中还需用到的仪器是
(3)操作C中,滤纸边缘要低于漏斗边缘是为了防止
(4)操作D中盛放滤液的仪器a是
【知识点】 固体配制一定质量分数溶液解读 粗盐提纯解读

(1)若实验室要用同一装置制取O2和CO2,最好选择发生装置是
(2)将红热的铁丝伸入(2)中收集满氧气的集气瓶(如图所示)内,没有看到铁丝火星四射的现象,可能的原因是

A没有擦除细铁丝表面的铁锈和油污
B水槽中导管有气泡冒出时马上收集气体
C点燃火柴后立即伸入集气瓶中
(3)实验室用锌和稀硫酸反应来制取氢气并测定氢气的体积,请从上图中选择最佳的装置进行组合,整套装置的导管口连接顺序是
A a→d B b→f C b→h→g→i D b→g→h→i
(4)实验室常用C装置来制备氯气(Cl2),推测其反应物可能是
A水和木炭 B氯化钠固体和二氧化锰C浓盐酸和二氧化锰
(5)氯气(Cl2)是有强烈刺激性气味的剧毒气体,能溶于水,与水反应生成

| 实验 编号 | 电压(V) | 温度(℃) | NaOH溶液浓度 | H2体积(mL) | O2体积(mL) | 时间(s) |
| a | 6 | 15 | 2% | 20 | 9.8 | 54.0 |
| b | 6 | 15 | 5% | 20 | 9.8 | 36.2 |
| c | 6 | 30 | 2% | 20 | 9.6 | 46.2 |
| d | 6 | 30 | 5% | 20 | 9.7 | t |
(1)本实验研究影响电解水速率的因素是
(2)比较实验a、c可得出结论:
(3)根据对实验a、b、c数据的分析,实验d的时间t最有可能是
A35.4 B37.8 C50.2 D55.6
(4)本实验通过比较
(5)电解水时H2与O2的体积比理论值为2:1,实验测得H2与O2的体积比大于理论值,请根据氢气、氧气的物理性质猜想原因可能是
四、科学探究题 添加题型下试题
(1)酸雨的pH
(2)常用脱硫方法减少废气中的SO2:以生石灰为脱硫剂,高温下与废气中的SO2和O2化合生成CaSO4,化学方程式为
(3)实验室常用亚硫酸盐与稀盐酸或稀硫酸制备SO2,Na2SO3与盐酸反应的化学方程式为
(4)小明同学利用中和反应的原理,在空气中放置一段时间的酸雨(pH约为3)中加入足量的KOH溶液,并就反应混合液中的盐的成分进行分析。
猜想1:
限选试剂:稀硫酸、稀盐酸、稀硝酸、氯化钡溶液、澄清石灰水、品红溶液、紫色石蕊溶液
| 实验操作 | 预期现象与结论 |
| 1. 各取2ml反应后混合溶液于A、B两支试管中 | |
| 2. 向A试管中加入足量稀硫酸,加入几滴品红溶液,振荡 | |
| 3. 向B试管加入 | 先有白色沉淀生成,后 |
试卷分析
试卷题型(共 30题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、选择题 | |||
| 1 | 0.85 | 化学性质和物理性质 二氧化碳的用途 浓硫酸做干燥剂 几种常见碱的物理性质及用途 | 单选题 |
| 2 | 0.65 | 空气中各成分的用途 空气的污染与防治 | 单选题 |
| 3 | 0.65 | 金刚石的相关知识 石墨的相关知识 二氧化碳的用途 | 单选题 |
| 4 | 0.85 | 对人体健康危害的物质 油脂作用 某些元素的缺乏症 | 单选题 |
| 5 | 0.85 | 常见几种净化水操作的比较 纯水、天然水与自来水 | 单选题 |
| 6 | 0.65 | 浓硫酸的稀释 仪器连接 气密性检测 | 单选题 |
| 7 | 0.65 | 置换反应 质量守恒定律的微观解释 微粒图像的分析及应用 | 单选题 |
| 8 | 0.65 | 原子结构 原子中各类微粒的数值关系 原子结构相关信息分析及应用 | 单选题 |
| 9 | 0.85 | 金属的物理通性与用途 合金的认识 应用金属活动性解释相关现象 废弃金属对环境的影响及回收 | 单选题 |
| 10 | 0.65 | 常见化肥的种类及性质 合理使用化肥和农药 | 单选题 |
| 11 | 0.85 | 中和反应的概念及微观本质 | 单选题 |
| 12 | 0.65 | 化学式、分子式及涵义 根据化学式计算元素质量比 根据化学式计算元素质量分数 | 单选题 |
| 13 | 0.65 | 金属与盐溶液反应 金属活动顺序理解和判断 | 单选题 |
| 14 | 0.65 | 测定空气中氧气的含量实验的过程 氢气的检验和验纯 实验探究燃烧条件 | 单选题 |
| 15 | 0.65 | 饱和溶液和不饱和溶液的转换 固体溶解度曲线的应用 | 单选题 |
| 16 | 0.65 | 复分解反应发生的条件 酸的通性 盐类参与的反应 | 单选题 |
| 17 | 0.65 | 硫在氧气中燃烧及其实验 木炭在氧气中燃烧及其实验 金属与酸反应原理 浓酸敞口放置的变化和现象 | 单选题 |
| 18 | 0.65 | 浓溶液稀释配制一定质量分数溶液 有关溶液浓缩、稀释的计算 | 单选题 |
| 19 | 0.65 | 浓硫酸的物理、化学性质 中和反应的实际应用 | 单选题 |
| 20 | 0.4 | 常见酸碱盐的溶解性 除杂 气体净化、干燥 | 单选题 |
| 二、填空与简答 | |||
| 21 | 0.65 | 化学方程式的书写 微粒的观点解释现象 空气中各成分的用途 | 简答题 |
| 22 | 0.4 | 复分解反应发生的条件 常用化合价规律 常见物质的溶解性 | 简答题 |
| 23 | 0.65 | 固体溶解度曲线的应用 | 填空题 |
| 24 | 0.4 | 保护和利用金属资源的有效途径 金属冶炼的计算 | 流程题 |
| 25 | 0.65 | 结晶分离混合物 盐类参与的反应 过滤 | 流程题 |
| 三、实验题 | |||
| 26 | 0.4 | 盐类参与的反应 碳酸根离子的验证 设计实验探究物质的成分 | |
| 27 | 0.65 | 固体配制一定质量分数溶液 粗盐提纯 | |
| 28 | 0.4 | 铁在氧气中燃烧及其实验 制取二氧化碳的装置 氢气的制备及应用 气体发生、收集装置 | |
| 29 | 0.85 | 电解水原理 对比实验 | |
| 四、科学探究题 | |||
| 30 | 0.4 | 溶液酸碱性及pH相关关系 酸碱性对生命活动和农作物生长的影响 设计实验探究物质的成分 | |

 加热液体
加热液体 塞紧胶塞
塞紧胶塞 气密性良好
气密性良好 稀释浓硫酸
稀释浓硫酸

