2022年江苏省镇江市区中考二模化学试题
江苏
九年级
二模
2022-07-03
297次
整体难度:
适中
考查范围:
物质构成的奥秘、身边的化学物质、化学与社会发展、化学实验、物质的化学变化
2022年江苏省镇江市区中考二模化学试题
江苏
九年级
二模
2022-07-03
297次
整体难度:
适中
考查范围:
物质构成的奥秘、身边的化学物质、化学与社会发展、化学实验、物质的化学变化
一、选择题 添加题型下试题
选择题-单选题
|
适中(0.65)
解题方法
1. 下列属于纯净物的是
| A.赤铁矿 | B.矿泉水 | C.石灰石 | D.液态氧 |
您最近一年使用:0次
2022-06-14更新
|
65次组卷
|
3卷引用:2022年江苏省镇江市市区中考二模化学试题
选择题-单选题
|
容易(0.94)
解题方法
2. 下列物质的用途主要与其化学性质有关的是
| A.干冰用作人工降雨 | B.液氮可用于医疗手术 |
| C.铁粉用作食品保鲜 | D.铜丝用作制导线 |
您最近一年使用:0次
2022-06-15更新
|
83次组卷
|
3卷引用:2022年江苏省镇江市市区中考二模化学试题
选择题-单选题
|
容易(0.94)
解题方法
3. 下列符合“安全、健康、绿色、舒适”的生产生活理念的是
| A.煤气泄漏,点火查看 | B.垃圾分类回收,集中处理 |
| C.农村田地上的秸秆焚烧处理 | D.用甲醛溶液浸泡海鲜 |
您最近一年使用:0次
2022-06-15更新
|
83次组卷
|
3卷引用:2022年江苏省镇江市市区中考二模化学试题
选择题-单选题
|
适中(0.65)
解题方法
4. 下列归类说法不正确的
| 选项 | 归类 | 内容 |
| A | 常见的碱 | 氨水、纯碱、苛性钠 |
| B | 营养物质 | 淀粉、维生素、蛋白质 |
| C | 氧化物 | 冰、生石灰、氧化铜 |
| D | 人体微量元素 | 铁、碘、锌 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-06-15更新
|
98次组卷
|
3卷引用:2022年江苏省镇江市市区中考二模化学试题
选择题-单选题
|
适中(0.65)
5. 在“粗盐的初步提纯”实验中,下列操作正确的是( )
A.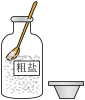 取用粗盐 取用粗盐 | B. 溶解粗盐 溶解粗盐 |
C.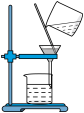 过滤粗盐水 过滤粗盐水 | D. 蒸干滤液 蒸干滤液 |
您最近一年使用:0次
2019-06-26更新
|
2797次组卷
|
64卷引用:江苏省苏州市2019年中考化学试题
江苏省苏州市2019年中考化学试题苏州市工业园区2019-2020学年九年级上学期期中化学试题考点04 化学实验基本操作-备战2020年中考化学考点天天刷江苏省苏州市常熟市2019-2020学年九年级上学期期中化学试题(已下线)专题14 实验操作与仪器使用《备战2020年中考化学真题分类汇编》(江苏省)湖北省黄冈市麻城市思源实验学校2019-2020学年九年级下学期4月在线考试化学试题(实验班)2020年广东省东莞市东莞中学初中部中考一模化学试题湖北省黄冈市罗田县万密斋初级中学2019-2020学年九年级下学期3月网络测试化学试题(已下线)课题11.1 生活中常见的盐 第1课时(练)-2019-2020学年九年级化学下册同步精品课堂(人教版)2020年江苏省苏州市昆山市九校联考中考模拟化学试题2020年福建省百校联合模拟中考化学试题(已下线)【万唯原创】2020年河北省中考化学面对面卷讲解册九年级第一部分九~十一单元(已下线)2020-2021学年九年级上学期第1章 化学的魅力 单元检测-九年级化学沪教版第一学期(试用本)同步精品课堂(上海专用)(已下线)主题 盐 化肥·基础必练2(已下线)主题 常见的酸碱盐·满分特训1(已下线)【万唯原创】2020年山西省中考化学面对面卷讲解册模块一第7-10讲(已下线)主题 盐 化肥·满分特训2(已下线)主题 盐 化肥?满分特训2(已下线)专题16: 常见仪器和基本实验操作(测试)--2021年中考化学一轮复习讲练测(人教版)(已下线)2020-2021学年人教版化学九年级下期末模拟卷-2020-2021学年九年级化学下册同步单元AB卷(人教版)(已下线)专题7.4 结晶现象(练习)——九年级化学下册同步精品课堂(科粤版)(已下线)考点04 化学实验基本操作-备战2021年中考化学考点天天刷(已下线)2021年中考化学全真模拟试卷(二)-2020-2021学年九年级化学下册同步单元AB卷(人教版)(已下线)2021中考广东省化学模拟试题(四)江苏省苏州市吴中区木渎实验中学2020-2021学年九年级上学期10月月考化学试题江苏省南京市栖霞区南京伯乐中学2020-2021学年九年级下学期月考化学试题2021年江苏省苏州市昆山市中考一调化学试题(已下线)必刷卷02-2021年中考化学考前信息必刷卷(扬州专用)福建省福州市鼓楼区福州二十二中2020-2021学年九年级下学期4月月考化学试题福建省泉州市永春县永春第一中学2019-2020学年九年级下学期4月月考化学试题(已下线)课题11.1.1 氯化钠和粗盐提纯-2021-2022学年九年级化学下册同步分层作业(人教版)江苏省苏州工业园区五校2021-2022学年九年级下学期3月线上教学评估化学试题福建省厦门市外国语学校2021-2022学年九年级下学期4月摸底练习化学试题2022年江苏省南京市玄武区中考一模化学试题(已下线)化学-(苏州卷)【试题猜想】2022年中考考前最后一卷2022年湖北省孝感黄冈咸宁三市中考适应性考试化学试题(三)2022年江西省南昌市中考第二次调研检测化学试题2022年江苏省镇江市市区中考二模化学试题2022年湖北省武汉市二中广雅中学5月月考化学试题2022年湖南省永州市蓝山县部分学校中考仿真模拟化学试题(二)2022年江苏省镇江市区中考二模化学试题2021年吉林省长春市汽车经济开发区中考三模化学试题2022年江苏省镇江市丹徒区中考模拟化学试题 (5)科粤版化学九年级下册课时练习:7.4 结晶现象第七章溶液检测卷---2021-2022学年九年级化学科粤版(2012)下册2023年吉林省长春市二道区英俊中学中考一模化学试题2023年重庆市中考押题化学试题(一)(已下线)金榜卷02-2023年中考化学考前一模名师押题金榜卷(南京专用)2023年3月山东省滨州市惠民县知识竞赛化学试题安徽省六安市金安区皋城中学2022-2023学年九年级下学期期中化学试题2023年江苏省淮安市淮安区中考一模化学试题2023年江苏省盐城市建湖县中考二模化学试题2023年江苏省盐城市滨海县中考二模化学试题(已下线)卷03-2023年中考化学考前押宝卷(陕西卷)2023年福建省泉州市泉港区教学质量检测化学试题2023年湖北省黄冈孝感咸宁三市初中学业考试适应性试化学试题(三)江苏省淮安市淮阴区2022-2023学年九年级下学期期中化学试题2023年陕西省西安市雁塔区陕西师范大学附属中学第九次模拟化学试题2023年6月湖北省襄阳市老河口市竹林桥中学中考模拟化学试题(已下线)第一章 化学的魅力(单元测试)-2023-2024学年九年级化学第一学期同步精品课堂(沪教版·上海)(已下线)专题08 盐 化肥(测试)-2024年中考化学一轮复习讲练测(全国通用)江苏省高邮市2023-2024学年九年级上学期期末联考化学试题2024年陕西省西安市滨河学校中考三模化学试题(已下线)黄金卷05(南京专用)-【赢在中考·黄金8卷】备战2024年中考化学模拟卷(南京专用)
6. 下列实验设计正确的是
| A.用过滤法将硬水软化 | B.用浓硫酸干燥 NH3 |
| C.用托盘天平称取 5.32g 氢氧化钠 | D.用灼烧法区分羊毛和棉花 |
您最近一年使用:0次
2022-06-15更新
|
78次组卷
|
3卷引用:2022年江苏省镇江市市区中考二模化学试题
选择题-单选题
|
适中(0.65)
解题方法
7. 下列排序正确的是
A.Mn 元素的化合价: |
B.物质的溶解性: |
C.溶液的pH: |
D.地壳中元素的含量: |
您最近一年使用:0次
选择题-单选题
|
适中(0.65)
解题方法
8. 下列应用和相应的原理(用化学方程式表示)都正确的是
A.金属铝放罝在空气中形成氧化膜  |
B.用氢氧化钠溶液吸收二氧化硫: |
C.比较铜和银的活动性强弱  |
D.镁粉着火不能用二氧化碳灭火: |
您最近一年使用:0次
2022-06-14更新
|
109次组卷
|
3卷引用:2022年江苏省镇江市市区中考二模化学试题
选择题-单选题
|
较易(0.85)
解题方法
9. 下列关于实验现象的描述,正确的是
| A.红磷在空气中燃烧时,产生大量白色烟雾 |
| B.碘化钾和硝酸银溶液混合,生成黑色沉淀 |
| C.电解水时负极产生的气体能使火星的木条复燃 |
| D.用粗砂纸打磨后的铝片放入硫酸铜溶液中,一段时间后,划痕处出现红色物质 |
您最近一年使用:0次
选择题-单选题
|
适中(0.65)
解题方法
10. 二氧化氯可杀灭新型冠状病毒,下列说法不正确的是


| A.乙的溶液应避光保存 | B.整个转化过程中,氯元素化合价保持不变 |
| C.反应前后原子的种类和个数不变 | D.转化 2 中丙和丁的分子个数比为 2:1 |
您最近一年使用:0次
2022-06-14更新
|
145次组卷
|
4卷引用:2022年江苏省镇江市市区中考二模化学试题
选择题-单选题
|
适中(0.65)
解题方法
11. 在航天飞船中常用铝粉与高氯酸铵(NH4ClO4)的混合物为固体燃料。发射时,点燃的铝粉产生大量的热引发高氯酸铵发生下列反应: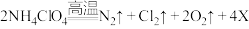 。下列说法不正确的是
。下列说法不正确的是
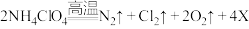 。下列说法不正确的是
。下列说法不正确的是| A.X 的化学式为 H2O | B.该反应属于分解反应 |
| C.反应过程中共有 3 种单质 | D.反应前后所有元素的化合价都发生了变化 |
您最近一年使用:0次
2022-06-14更新
|
115次组卷
|
3卷引用:2022年江苏省镇江市市区中考二模化学试题
12. 如图为 NaHCO3分解实验装置。下列说法不正确的是
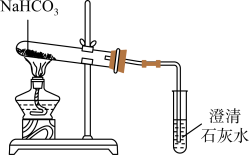

| A.试管内固体逐渐消失 | B.石灰水混浊,说明反应生成了 CO2 |
| C.充分加热后的固体溶于水,滴加酚酞,变红 | D.加热时试管口应略向下倾斜 |
【知识点】 碳酸氢钠、碳酸钠、碳酸钙解读 物质的加热解读
您最近一年使用:0次
2022-06-13更新
|
198次组卷
|
5卷引用:2022年江苏省镇江市市区中考二模化学试题
2022年江苏省镇江市市区中考二模化学试题2022年江苏省镇江市区中考二模化学试题2022年江苏省镇江市丹徒区中考模拟化学试题 (5)(已下线)课题11.1 生活中常见的盐 第1课时(练习)-2022-2023学年九年级化学下册同步精品课堂(人教版)2023分层教学_人教版_第十一单元 课题1生活中常见的盐第2课时_中等题(已审)
选择题-单选题
|
适中(0.65)
解题方法
13. 下列各组转化中,一定条件下能一步实现的组合是
A.Fe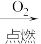 Fe2O3 Fe2O3 FeCl3 FeCl3 |
B.CaCl2 溶液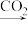 CaCO3 CaCO3 CaO CaO |
C.O2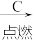 CO2 CO2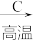 CO CO |
D.NaOH NaNO3 NaNO3 KNO3 KNO3 |
您最近一年使用:0次
选择题-单选题
|
适中(0.65)
解题方法
14. 下列实验操作能达到实验目的的是
| 选项 | 物质 | 目的 | 主要实验操作 |
| A | 蔗糖溶液和蛋白质溶液 | 鉴别 | 加入饱和(NH4)2SO4溶液,观察现象 |
| B | NaCl溶液是否混有MgCl2 | 检验 | 取样滴加AgNO3溶液,观察是否产生沉淀 |
| C | 铁粉中混有铜粉 | 除杂 | 加入足量的稀硫酸,过滤 |
| D | KNO3和Ba(NO3)2的混合溶液 | 分离 | 加入过量的Na2CO3溶液,过滤,洗涤,再分别向滤渣和滤液中加适量的稀盐酸 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-06-16更新
|
127次组卷
|
3卷引用:2022年江苏省镇江市市区中考二模化学试题
选择题-单选题
|
较难(0.4)
解题方法
15. 一种提纯白磷样品(杂质不参与如图反应)的工艺流程如图所示。下列说法不正确的是
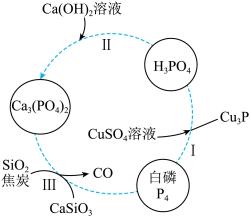
| A.过程Ⅰ中,P 元素的化合价既升高又降低 |
| B.过程Ⅱ中,发生复分解反应 |
C.过程Ⅲ中,反应的化学方程式为:  |
| D.理论上,通过本提纯工艺不会产生白磷损失 |
您最近一年使用:0次
2022-06-13更新
|
523次组卷
|
9卷引用:2022年江苏省镇江市市区中考二模化学试题
2022年江苏省镇江市市区中考二模化学试题2022年江苏省镇江市区中考二模化学试题2022年江苏省镇江市丹徒区中考模拟化学试题 (1)(已下线)专题17 化学工艺流程题- 决胜2023年中考化学一轮地毯式复习(全国通用)2023年江苏省常州市中考模拟化学试题12023年江苏省扬州市江都区第三中学中考二模化学试题2023年江苏省扬州市仪征市中考二模化学试题(已下线)化学(无锡卷)-学易金卷:2024年中考考前押题密卷黑龙江省大庆市肇源县五校联考2023-2024学年九年级下学期5月期中化学试题
选择题-单选题
|
适中(0.65)
解题方法
16. 下列叙述正确的是
| A.原子失去电子可以得到阳离子 |
| B.饱和溶液中有晶体析出时,溶质质量分数一定减小 |
| C.某化肥与熟石灰研磨,无刺激性气味,该化肥一定不是氮肥 |
| D.向露置在空气中的 NaOH 溶液滴加几滴稀盐酸,无气泡,则 NaOH 溶液未变质 |
您最近一年使用:0次
2022-06-13更新
|
104次组卷
|
4卷引用:2022年江苏省镇江市市区中考二模化学试题
选择题-单选题
|
适中(0.65)
解题方法
17. K2CO3和 KNO3在不同温度时的溶解度数据如表,对应的溶解度曲线如图1,30℃时,向两个分别盛有相同质量的 K2CO3和 KNO3的烧杯中各加入 50.0g 水,充分溶解,恢复至 30℃,结果如图 2 所示。下列说法正确的是

| 温度/℃ | 20 | 30 | 50 | 60 | 80 | |
| 溶解度 (g/100g 水) | K2CO3 | 110 | 114 | 121 | 126 | 139 |
| KNO3 | 31.6 | 45.8 | 85.5 | 110 | 169 | |

| A.甲表示 K2CO3的溶解度曲线 |
| B.t 1应介于 50℃~60℃ |
| C.30℃时,饱和KNO3溶液的溶质质量分数为 45.8% |
| D.30℃时所加入的K2CO3和 KNO3质量 m 应满足 22.9g<m≤57.0g |
【知识点】 固体溶解度曲线的应用解读 溶解度的相关计算解读
您最近一年使用:0次
选择题-单选题
|
较难(0.4)
解题方法
18. 下列各组物质的溶液,不另加试剂就能将他们鉴别出来的是
| A.KCl KNO3 Na2CO3 Na2SO4 | B.BaCl2 Na2SO4 Na2CO3 NaCl |
| C.AgNO3 HCl NaCl HNO3 | D.CuCl2 NaOH HCl MgCl2 |
【知识点】 复分解反应的实质与应用解读
您最近一年使用:0次
2022-06-14更新
|
155次组卷
|
3卷引用:2022年江苏省镇江市市区中考二模化学试题
选择题-单选题
|
较难(0.4)
19. 在 MgSO4、H2SO4的混合溶液中先后加入 8%的 NaOH 溶液、BaCl2溶液,产生沉淀质量与滴加溶液质量关系如图所示。已知当 NaOH 溶液滴加至 m 时,MgSO4、H2SO4恰好完全反应。下列说法正确的


| A.a 点时溶液的 pH<7 |
| B.m=150 |
| C.BaCl2溶液溶质的质量分数是 23.4% |
| D.在 b 点溶液中加 AgNO3溶液,出现白色沉淀,证明加入 BaCl2溶液已过量 |
您最近一年使用:0次
2022-06-13更新
|
250次组卷
|
6卷引用:2022年江苏省镇江市市区中考二模化学试题
2022年江苏省镇江市市区中考二模化学试题2022年江苏省镇江市区中考二模化学试题2022年江苏省镇江市丹徒区中考模拟化学试题 (2)(已下线)黄金卷04-【赢在中考·黄金8卷】备战2023年中考化学全真模拟卷(南京专用)(已下线)选择专练05 化学方程式的计算(25题)-2023年中考化学总复习高频考点必刷题(苏州专用)2023年安徽省六安市金寨县东片七校联考中考模拟化学试题(二)
选择题-单选题
|
困难(0.15)
解题方法
20. 在 Cu(NO3)2 和 AgNO3混合溶液中加入 9.6gCu 粉,充分反应后过滤得到 17.2g 固体和滤液,滤液中加入 100g16%NaOH 溶液恰好完全反应得蓝色沉淀。下列说法正确的是
| A.17.2g 固体是纯净物 |
| B.滤液比原混合溶液中铜元素质量小 |
| C.原混合溶液中 Cu(NO3)2、AgNO3的质量比是 141:85 |
| D.使蓝色沉淀完全溶解至少需加入 9.8%的稀硫酸 100g |
【知识点】 含杂质的化学方程式计算解读 金属与盐溶液反应 盐类参与的反应解读
您最近一年使用:0次
2022-06-13更新
|
295次组卷
|
3卷引用:2022年江苏省镇江市市区中考二模化学试题
二、填空与简答 添加题型下试题
填空与简答-填空题
|
容易(0.94)
解题方法
21. 用化学符号表示:
(1)水银____________ ;
(2)相对分子质量最小的氧化物____________ ;
(3)2 个亚铁离子____________ ;
(4)儿童缺少____________ 元素,严重时会得侏儒症。
(1)水银
(2)相对分子质量最小的氧化物
(3)2 个亚铁离子
(4)儿童缺少
您最近一年使用:0次
2022-06-13更新
|
182次组卷
|
3卷引用:2022年江苏省镇江市市区中考二模化学试题
22. 选择下列适当的物质填空(填字母)
A.硝酸铵 B.武德合金 C.硝酸钾 D.活性炭 E.纯碱 F.石灰石 G.熟石灰 H.维生素
(1)可做冰箱除味剂的是____________ ;
(2)可用作复合肥料的是____________ ;
(3)可用作电路保险丝的是____________ ;
(4)侯氏制碱法得到的“碱”是____________ ;
(5)蔬菜中富含的营养物质是____________ ;
(6)用于制造水泥、玻璃的矿石是____________ 。
A.硝酸铵 B.武德合金 C.硝酸钾 D.活性炭 E.纯碱 F.石灰石 G.熟石灰 H.维生素
(1)可做冰箱除味剂的是
(2)可用作复合肥料的是
(3)可用作电路保险丝的是
(4)侯氏制碱法得到的“碱”是
(5)蔬菜中富含的营养物质是
(6)用于制造水泥、玻璃的矿石是
您最近一年使用:0次
2022-06-13更新
|
88次组卷
|
3卷引用:2022年江苏省镇江市市区中考二模化学试题
填空与简答-流程题
|
容易(0.94)
解题方法
23. 医用消毒酒精为 75%的乙醇溶液,化工生产中可用 A(主要成分的化学式为 C8H18)作原料,经以下流程制取乙醇:

(1)步骤①的转化属于____________ (填“化学”或“物理”)变化。
(2)步骤②是乙烯和含两种元素的化合物B发生化合反应,则B的化学式是____________ 。

(1)步骤①的转化属于
(2)步骤②是乙烯和含两种元素的化合物B发生化合反应,则B的化学式是
【知识点】 化学变化与物理变化判断解读 用质量守恒定律确定物质组成解读
您最近一年使用:0次
2022-06-13更新
|
166次组卷
|
3卷引用:2022年江苏省镇江市市区中考二模化学试题
三、综合应用题 添加题型下试题
24. 化学就在我们身边,人类的生活离不开化学。
(1)CO2过度排放对环境造成的影响是____________ 。下列有利于实现“碳中和”的是____________ 。(选填序号)
A.植树造林 B.使用太阳能等清洁能源 C.加大煤和石油的使用 D.提倡绿色出行
(2)2022 北京冬奥会场馆使用了二氧化碳跨临界直冷循环制冰技术。利用液态二氧化碳蒸发吸热完成制冰。 下列关于液态二氧化碳蒸发过程的说法正确的是 。(选填序号)
(3)煤、石油和____________ 是常见的化石燃料。在煤中加入 X 可有效防止煤燃烧时生成的SO2对大气造成污染,发生反应的化学方程式是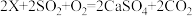 ,则 X 的化学式是
,则 X 的化学式是 ____________ 。
(4)科学家研究利用催化剂实现了 CO2 与 H2反应制取 CH3OH,理论上参加反应的CO2和H2的质量比为____________ 。
(1)CO2过度排放对环境造成的影响是
A.植树造林 B.使用太阳能等清洁能源 C.加大煤和石油的使用 D.提倡绿色出行
(2)2022 北京冬奥会场馆使用了二氧化碳跨临界直冷循环制冰技术。利用液态二氧化碳蒸发吸热完成制冰。 下列关于液态二氧化碳蒸发过程的说法正确的是 。(选填序号)
| A.二氧化碳分子间的间隔增大 | B.二氧化碳分子的大小发生了变化 |
| C.二氧化碳分子的质量发生了变化 | D.二氧化碳分子不再运动 |
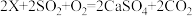 ,则 X 的化学式是
,则 X 的化学式是 (4)科学家研究利用催化剂实现了 CO2 与 H2反应制取 CH3OH,理论上参加反应的CO2和H2的质量比为
您最近一年使用:0次
2022-06-13更新
|
192次组卷
|
4卷引用:2022年江苏省镇江市市区中考二模化学试题
四、填空与简答 添加题型下试题
填空与简答-流程题
|
较易(0.85)
解题方法
25. 某兴趣小组回收废旧锌锰电池制备皓矾晶体(ZnSO4·xH2O),请回答下列问题:

(1)试剂 X 可用 (选填序号)。
(2)操作I中,所用的玻璃仪器有____________ 、玻璃棒、烧杯。
(3)操作 II 为蒸发浓缩、____________ 、过滤、洗涤干燥。
(4)洗涤时不可选用的试剂为 (选填序号)。

(1)试剂 X 可用 (选填序号)。
| A.稀HCl | B.稀H2SO4 | C.稀HNO3 |
(2)操作I中,所用的玻璃仪器有
(3)操作 II 为蒸发浓缩、
(4)洗涤时不可选用的试剂为 (选填序号)。
| A.冰水 | B.ZnSO4饱和溶液 | C.热水 |
您最近一年使用:0次
填空与简答-填空题
|
适中(0.65)
解题方法
26. 观察如图实验,回答问题:双隔膜电解池的结构简图如图所示,利用铅蓄电池电解 Na2SO4溶液可以制取 H2SO4和 NaOH。

(1)装置中电能转化为____________ 能;
(2)该电解反应的总方程式可以表示为________ (H2SO4和 NaOH 的化学计量数之比为 1:2)。

(1)装置中电能转化为
(2)该电解反应的总方程式可以表示为
【知识点】 化学方程式的书写解读 化学反应中能量变化的实际应用解读
您最近一年使用:0次
2022-06-13更新
|
95次组卷
|
3卷引用:2022年江苏省镇江市市区中考二模化学试题
五、实验题 添加题型下试题
27. 某化学兴趣小组根据如图所示装置进行实验室制取气体的探究。回答下列问题:

(1)写出图中带有标号仪器的名称:①________ ;② ________ 。
(2)用高锰酸钾制取氧气时,选择发生装置为________ (选填序号,下同),反应方程式为________ 。
(3)实验室制取氢气的反应方程式为________ ,将气体的发生装置由 B 改为 F,优点是________ 。
(4)某同学为比较不同形状的碳酸钙与稀盐酸反应的速率,利用数据传感技术测得瓶内气压随时间的变化如图所示。

①写出碳酸钙与稀盐酸反应的化学方程式________ ,将产生的二氧化碳气体通入澄清石灰水,石灰水没有变浑浊,原因可能是 ________ 。
②对比分析 a、b 点可知,曲线甲表示________ (填“块状碳酸钙”或 “碳酸钙粉末”)的反应。
③下列说法正确的是________ (选填序号)。
A.碳酸钙粉末产生的 CO2质量多
B.对比分析 c、d 点可知,相同的气压时,碳酸钙粉末比稀盐酸反应速率更快

(1)写出图中带有标号仪器的名称:①
(2)用高锰酸钾制取氧气时,选择发生装置为
(3)实验室制取氢气的反应方程式为
(4)某同学为比较不同形状的碳酸钙与稀盐酸反应的速率,利用数据传感技术测得瓶内气压随时间的变化如图所示。

①写出碳酸钙与稀盐酸反应的化学方程式
②对比分析 a、b 点可知,曲线甲表示
③下列说法正确的是
A.碳酸钙粉末产生的 CO2质量多
B.对比分析 c、d 点可知,相同的气压时,碳酸钙粉末比稀盐酸反应速率更快
您最近一年使用:0次
2022-06-13更新
|
160次组卷
|
4卷引用:2022年江苏省镇江市市区中考二模化学试题
实验题
|
适中(0.65)
28. 实验是学习化学的重要方法。根据如图实验,回答问题。

【实验一】
(1)Ⅲ中为 Ca(HCO3)2澄清溶液,则浑浊消失所发生反应的化学方程式为_____________ 。
(2)取少量Ca(HCO3)2溶液缓缓加热,发现其很快变浑浊,说明Ca(HCO3)2的热稳定性比CaCO3___________ (填“强”或“弱”)。
【实验二】加入一定量 NH4Cl 溶液后加热锥形瓶,完全反应,瓶内出现浑浊且有气泡放出。
(3)V 中石灰水变浑浊说明Ⅳ中产生的气体是___________ ,在 V 中烧杯口放湿润的红色石蕊试纸,试纸___________ ,说明还生成了 NH3。
(4)Ⅳ中反应后的混合物经过滤、洗涤、干燥得白色固体 3g,将滤液蒸发得 CaCl2固体 1.11g。
结论:① 加入 NH4Cl 溶液前Ⅳ中 Ca 元素的质量为___________ g;
② Ⅳ中反应的化学反应方程式为___________ 。
【拓展】
(5)如实验二改加入过量 NH4Cl 溶液加热,则锥形瓶中有气泡放出且不变浑浊,其余现象与实验二相同,此时Ⅳ中反应的化学方程式为___________ 。

【实验一】
(1)Ⅲ中为 Ca(HCO3)2澄清溶液,则浑浊消失所发生反应的化学方程式为
(2)取少量Ca(HCO3)2溶液缓缓加热,发现其很快变浑浊,说明Ca(HCO3)2的热稳定性比CaCO3
【实验二】加入一定量 NH4Cl 溶液后加热锥形瓶,完全反应,瓶内出现浑浊且有气泡放出。
(3)V 中石灰水变浑浊说明Ⅳ中产生的气体是
(4)Ⅳ中反应后的混合物经过滤、洗涤、干燥得白色固体 3g,将滤液蒸发得 CaCl2固体 1.11g。
结论:① 加入 NH4Cl 溶液前Ⅳ中 Ca 元素的质量为
② Ⅳ中反应的化学反应方程式为
【拓展】
(5)如实验二改加入过量 NH4Cl 溶液加热,则锥形瓶中有气泡放出且不变浑浊,其余现象与实验二相同,此时Ⅳ中反应的化学方程式为
您最近一年使用:0次
2022-06-13更新
|
115次组卷
|
4卷引用:2022年江苏省镇江市市区中考二模化学试题
实验题
|
适中(0.65)
解题方法
29. 现有一包不纯的 Na2SO4 固体,可能含有 Fe(NO3)3 、CaCO3、NaCl、MgCl2、Ba(OH)2中的一种或几种。现做如下实验:
(1)取少量固体溶于足量水,过滤得白色固体 A 和无色滤液 B,则原固体一定不含___________ 。
(2)取固体 A,加入足量稀HCl,固体完全溶解,则原固体一定不含___________ ,固体溶解的化学反应方程式为___________ 。
(3)取少量滤液 B,滴加 NaOH 溶液,无明显现象,则原固体一定不含___________ 。
(4)另取少量滤液 B,先滴加过量 Ba(NO3)2 溶液,静置,再滴加___________ 溶液,出现白色沉淀,则原固体中还含有 NaCl。
(1)取少量固体溶于足量水,过滤得白色固体 A 和无色滤液 B,则原固体一定不含
(2)取固体 A,加入足量稀HCl,固体完全溶解,则原固体一定不含
(3)取少量滤液 B,滴加 NaOH 溶液,无明显现象,则原固体一定不含
(4)另取少量滤液 B,先滴加过量 Ba(NO3)2 溶液,静置,再滴加
您最近一年使用:0次
2022-06-13更新
|
121次组卷
|
3卷引用:2022年江苏省镇江市市区中考二模化学试题
六、综合应用题 添加题型下试题
综合应用题
|
较难(0.4)
30. 铁及其化合物在生产生活中有广泛的应用。
(一)铁的应用
(1)如图,市售“加铁酱油”中的铁是指 。(选填序号)

(2)加铁酱油的包装中不含有的材料是 。(选填序号)
(3)某面粉中含微量铁粉,食用后铁粉与胃酸反应转化为人体可吸收的铁,反应的化学方程式为___________ 。已知在酱油中添加了乙二胺四乙酸铁钠(化学式为 C10H12FeN2NaO8·xH2O,C10H12FeN2NaO8的相对分子质量是 367),铁锈味弱、铁吸收率高,是适宜于酱油中食用的理想补铁 剂,它属于___________ (填无机物或有机物),已知在乙二胺四乙酸铁钠中铁的质量分数约为 13.3%,则 X≈___________ (保留到整数)。
(二)黄钾铵铁矾的制取

黄钾铵铁矾[KNH4Fex(SO4)y(OH)z]不溶于水和稀硫酸,制取黄钾铵铁矾的示意图如下:
(4)在实验室中可以用铁红(Fe2O3)来制取 Fe2(SO4)3,发生反应的化学方程式为_______ 。
(5)溶液 X 是 。(选填序号)
(6)加入溶液 X 后反应时温度不宜过高的原因是_______ 。
(7)检验黄钾铵铁矾已洗净的方法是_______ 。
(三)黄钾铵铁矾组成确定
称取 9.81g 黄钾铵铁矾,用下图装置进行热分解实验。

【资料】KNH4Fex(SO4)y(OH)z 在 300℃分解生成 NH3、SO3和水蒸气(NH3与 SO3分子数之比为 2:1),此时 A 中剩余固体为 KFe(SO4)2、Fe2O3、Fe2(SO4)3;提高温度至 550℃继续分解产生 SO3,并得到 Fe2O3和 K2SO4。
(8)装配好实验装置后,先要_________ 。
(9)分别控制温度在 300℃、550℃对 A 中固体加热。
①控制温度在 300℃加热,实验后测得 B 装置质量增加 1.57 g,C 装置质量增加 0.17 g。
②控制温度在 550℃,加热至反应完全,B 装置质量又增加 2.4 g。
300℃时,需缓缓通入 N2,其目的是__________ 。
(10)反应完全后,将 A 装置中固体溶于足量水,过滤,洗涤,烘干,得固体和滤液,将滤液蒸干得 0.87g 固体(不含结晶水),则 550℃ 时完全反应后 A 中剩余固体的质量是__________ g。
(11)黄钾铵铁矾的化学式是_______ ,300℃ 时黄钾铵铁矾发生反应的化学方程式为_______ 。
(一)铁的应用
(1)如图,市售“加铁酱油”中的铁是指 。(选填序号)

| A.铁单质 | B.铁原子 | C.铁元素 |
(2)加铁酱油的包装中不含有的材料是 。(选填序号)
| A.合成材料 | B.无机非金属材料 | C.金属材料 |
(3)某面粉中含微量铁粉,食用后铁粉与胃酸反应转化为人体可吸收的铁,反应的化学方程式为
(二)黄钾铵铁矾的制取

黄钾铵铁矾[KNH4Fex(SO4)y(OH)z]不溶于水和稀硫酸,制取黄钾铵铁矾的示意图如下:
(4)在实验室中可以用铁红(Fe2O3)来制取 Fe2(SO4)3,发生反应的化学方程式为
(5)溶液 X 是 。(选填序号)
| A.烧碱溶液 | B.石灰水 | C.氨水 |
(6)加入溶液 X 后反应时温度不宜过高的原因是
(7)检验黄钾铵铁矾已洗净的方法是
(三)黄钾铵铁矾组成确定
称取 9.81g 黄钾铵铁矾,用下图装置进行热分解实验。

【资料】KNH4Fex(SO4)y(OH)z 在 300℃分解生成 NH3、SO3和水蒸气(NH3与 SO3分子数之比为 2:1),此时 A 中剩余固体为 KFe(SO4)2、Fe2O3、Fe2(SO4)3;提高温度至 550℃继续分解产生 SO3,并得到 Fe2O3和 K2SO4。
(8)装配好实验装置后,先要
(9)分别控制温度在 300℃、550℃对 A 中固体加热。
①控制温度在 300℃加热,实验后测得 B 装置质量增加 1.57 g,C 装置质量增加 0.17 g。
②控制温度在 550℃,加热至反应完全,B 装置质量又增加 2.4 g。
300℃时,需缓缓通入 N2,其目的是
(10)反应完全后,将 A 装置中固体溶于足量水,过滤,洗涤,烘干,得固体和滤液,将滤液蒸干得 0.87g 固体(不含结晶水),则 550℃ 时完全反应后 A 中剩余固体的质量是
(11)黄钾铵铁矾的化学式是
您最近一年使用:0次
2022-06-13更新
|
246次组卷
|
3卷引用:2022年江苏省镇江市市区中考二模化学试题
试卷分析
整体难度:适中
考查范围:物质构成的奥秘、身边的化学物质、化学与社会发展、化学实验、物质的化学变化
试卷题型(共 30题)
题型
数量
选择题
20
填空与简答
5
综合应用题
2
实验题
3
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、选择题 | |||
| 1 | 0.65 | 纯净物和混合物的判断 常见金属矿石 碳酸氢钠、碳酸钠、碳酸钙 | 单选题 |
| 2 | 0.94 | 空气中各成分的用途 二氧化碳的用途 金属的物理通性与用途 金属与氧气反应 | 单选题 |
| 3 | 0.94 | 对人体健康危害的物质 火灾的预防及自救措施 空气污染及其保护 垃圾分类(上海) | 单选题 |
| 4 | 0.65 | 氧化物的定义 常见酸、碱的俗称及化学式 蛋白质 人体内的微量元素——碘、铁元素 | 单选题 |
| 5 | 0.65 | 粗盐提纯 量筒的正确使用方法和注意事项 酒精灯的正确使用方法和注意事项 固体药品的取用 | 单选题 |
| 6 | 0.94 | 硬水的危害及软化方法 浓硫酸做干燥剂 羊毛、合成纤维、棉的鉴别 托盘天平的正确使用方法和注意事项 | 单选题 |
| 7 | 0.65 | 地壳中元素的含量 化合价代数和的计算与应用 溶液酸碱性及pH相关关系 常见酸碱盐的溶解性 | 单选题 |
| 8 | 0.65 | 化学方程式配平 金属与氧气反应 金属与盐溶液反应 碱的通性 | 单选题 |
| 9 | 0.85 | 测定空气中氧气的含量实验的过程 金属与盐溶液反应 电解水生成物的验证 盐类参与的反应 | 单选题 |
| 10 | 0.65 | 质量守恒定律的微观解释 微粒图像的分析及应用 化合价代数和的计算与应用 | 单选题 |
| 11 | 0.65 | 分解反应 根据方程式推测化学式 单质和化合物的判断 常见元素、原子团的化合价 | 单选题 |
| 12 | 0.85 | 碳酸氢钠、碳酸钠、碳酸钙 物质的加热 | 单选题 |
| 13 | 0.65 | 复分解反应发生的条件 铁在氧气中燃烧及其实验 碳单质与某些氧化物的反应 盐类参与的反应 | 单选题 |
| 14 | 0.65 | 金属与酸反应原理 盐类参与的反应 蛋白质 转化为沉淀 | 单选题 |
| 15 | 0.4 | 复分解反应的实质与应用 化学方程式的书写 化合价代数和的计算与应用 | 单选题 |
| 16 | 0.65 | 同一元素的离子与原子相互转化 晶体与非晶体 碱的通性 铵根离子的验证 | 单选题 |
| 17 | 0.65 | 固体溶解度曲线的应用 溶解度的相关计算 | 单选题 |
| 18 | 0.4 | 复分解反应的实质与应用 | 单选题 |
| 19 | 0.4 | 溶质质量分数结合化学方程式的计算 溶液和化学方程式的综合计算 溶液酸碱性及pH相关关系 几种常见阴、阳离子的鉴别 | 单选题 |
| 20 | 0.15 | 含杂质的化学方程式计算 金属与盐溶液反应 盐类参与的反应 | 单选题 |
| 二、填空与简答 | |||
| 21 | 0.94 | 元素符号书写及含义 化学式、分子式及涵义 化学符号周围数字的含义 某些元素的缺乏症 | 填空题 |
| 22 | 0.94 | 活性炭的吸附性 合金的认识 常见化肥的种类及性质 维生素的来源 | 填空题 |
| 23 | 0.94 | 化学变化与物理变化判断 用质量守恒定律确定物质组成 | 流程题 |
| 25 | 0.85 | 金属与酸反应原理 过滤 蒸发结晶 | 流程题 |
| 26 | 0.65 | 化学方程式的书写 化学反应中能量变化的实际应用 | 填空题 |
| 三、综合应用题 | |||
| 24 | 0.85 | 根据方程式推测化学式 微粒的共性 二氧化碳对生活环境的影响 常见几种燃料使用对环境的影响 | |
| 30 | 0.4 | 有机物定义和常见的有机物 元素的概念 盐类参与的反应 设计实验探究物质的成分 | |
| 四、实验题 | |||
| 27 | 0.65 | 高锰酸钾制取氧气实验 二氧化碳制取的综合考查 气体发生、收集装置 根据图像分析结论 | |
| 28 | 0.65 | 化学方程式的书写 不含杂质的化学方程式计算 二氧化碳与碱的反应及实验 盐类参与的反应 | |
| 29 | 0.65 | 碱的通性 盐类参与的反应 几种常见阴、阳离子的鉴别 设计实验探究物质的成分 | |



